
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Короткі теоретичні відомості. Господарсько-питного призначення
|
|
|
|
Господарсько-питного призначення
Контроль якості води. Визначення твердості води
Лабораторна робота 5
Тестові запитання для контролю самостійної роботи
1. В чому полягає очистка стічних вод методом електрокоагуляції?
2. Вкажіть особливості очистки води методом електрофлотації.
3. Для очистки води від яких забруднювачів доцільно застосовувати електрофлотацію?
4. Яким чином проводиться очистка стічних вод методом
електролізу?
5. Які матеріали використовують для виготовлення катодів і анодів?
6. Які окисно–відновні процеси протікають на катоді і аноді при електролізі води, забрудненої СuSО4, NaС1, КNОз, Ns2S?
7. Яким методом можна визначити кількісний вміст міді у стічній
воді?
8. Наведіть приклади енергозберігаючих і матеріалозберігаючих
технологічних процесів при електролізі водних розчинів.
9. Наведіть приклади ресурсозберігаючих технологій в процесі
електролізу розчину сульфату міді (СuSО4) з розчинним анодом -
чорновою міддю.
10. Наведіть приклади рекуперації, регенерації, хімічних забруднень
води, утилізації відходів при застосуванні електрохімічних методів
очистки.
Література [8-11, 13-16, 18-20, 35, 46, 48, 49].
5.1 Мета роботи. Вивчити основні санітарно-гігієнічні вимоги до якості води та експериментально визначити твердість води, до та після іонітної очистки.
Вода широко використовується в техніці: в хімічних виробництвах як розчинник і реагент, для промивання різноманітних речовин, для парових котлів, для охолодження різноманітних агрегатів і т.д.
Одним з основних показників якості води, важливим для багатьох водокористувачів (промисловість, сільське господарство, побут і т.і.), є мінералізація води. Суттєвий вплив на властивості води мають розчинені в ній домішки (табл.. 5.1). Так, вода морів і океанів непридатна для поливу грунту (вода вважається придатною для зрошення, якщо кількість розчинених в ній солей не перевищує 1000 мг/л), для пиття і для багатьох технічних цілей, так як в ній вміщується велика кількість солей. Загальна солоність, наприклад, морської води складає близько 3.5%. З них лише два компоненти (хлориди та натрій) присутні в кількості більше 1%, концентрація ж двох інших: сульфатів та магнію складають біля 0.1%, а таких чотирьох компонентів, як кальцій, гідрокарбонат, калій та бром, складають близько 0.001%. Інші елементи присутні в морській воді в дуже малих концентраціях, для багатьох з них вони нижче межі виявлення. Прісна річна та артезіанська вода також має різні домішки, але в значно менших кількостях. Ці домішки дуже необхідні для життя людини, тварин та рослин, але часто є дуже шкідливими при використанні води в техніці. Так, вміст у воді солей марганцю навіть у малих дозах робить її непридатною для використання у виробництві волокон, так як марганець окисляється киснем з повітря і випадає у вигляді діоксиду, фарбуючи волокна в бурий колір. Для парових котлів особливо шкідливими домішками є солі кальцію та магнію, а також кремнієва кислота. Ці домішки при високій температурі утворюють осад на стінках котла (накип), що погано проводить тепло, тому відбувається місцевий перегрів котла, що може привести до вибуху. Ці ж речовини осідають на внутрішніх стінках труб в системах водяного охолодження, погіршують теплообмін та виводять систему з ладу. В залежності від твердості води з певною інтенсивністю проходять процеси корозії енергетичного обладнання.
Таблиця 5.1 – Найважливіші домішки води
| Група | Назва та загальна характеристика домішок | Концентрація домішок, мг/л |
| І | Макродомішки, що характерні для природних вод: Ca2+, Mg2+, Na+, K+, HCO3-, SO42-, Cl- | 1 – 105 |
| II | Макродомішки неорганічні малотоксичні: Fe2+, Fe3+, Al3+, CO32-, F-, I-, Mg2+, Cu2+, HSiO3–, HS- та ін. | 10-1 – 10 |
| ІІІ | Біогенні домішки: NH4+, NH3, NO3-, NO2-, HPO42-, H2PO4- | 10-1 – 102 |
| IV | Мікродомішки неорганічні сильнотоксичні (в т.ч. сполуки важких металів): Cd2+, Pb2+, Hg2+, Co2+, AsIII,V, Mn2+, SeVI, Be2+, Ag+, CN-, CSN- та ін. | 10-4 – 1 |
| V | Біологічно нестійкі органічні сполуки і проміжні продукти їх розпаду, що порушують кисневий режим водойм, погіршуючи запах та смак води | 10-3 – 10 |
| VI | Біологічно тверді органічні та гетероциклічні сполуки з специфічними токсичними (мутагенними, канцерогенними, алергенними та ін.) якостями | 10-5 – 10-1 |
| VII | Бактерії, віруси та інші патогенні мікроорганізми | – |
| VII | Домішки радіоактивних ізотопів, сильнотоксичні (90Sr, 137Cs, 131I, 60Co, 106Ru та ін.) | 10-10 – 10-4 |
Присутність солей кальцію та магнію у воді визначає її твердість. В природних умовах утворення гідрокарбонатів проходить при взаємодії вугільної кислоти з вапняком, доломітом, згідно реакціям:
CaCО3 + CО2 + H2O ↔ Ca(HCO3)2 (5.1)
CaCО3 + MgCO3 + 2H2O + 2CO2 ↔ Ca(HCO3)2 + Mg(HCO3)2 (5.2)
Розрізняють карбонатну твердість (Тк), яка зумовлюється вмістом гідрокарбонатів кальцію та магнію; некарбонатну твердість (Тнк), яка зумовлюється вмістом хлоридів, сульфатів Са, Mg.
Загальна твердість (Тзаг) – визначається загальним вмістом солей твердості:
Тзаг = Тк + Тнк (5.3)
При тривалому кипінні твердість води зменшується за рахунок видалення карбонатної твердості:
Ca(HCO3)2 ® CaCO3¯ + CO2 + H2O (5.4)
Mg(HCO3)2 ® MgCO3¯ + CO2 + H2O (5.5)
2Mg(HCO3)2 ® (MgOH)2CO3 + 3CO2 + H2O (5.6)
Кип’ятінням не можливо видалити всю карбонатну твердість (розчинність СаСО3 – 0.01 г/л, (MgOH)2CO3 – 0.04 г/л), тому іноді використовують термін тимчасова твердість, розуміючи під цим концентрацію солей Ca(HCO3)2 та Mg(HCO3)2, що видаляються з води після кип’ятіння її протягом двох годин. Твердість, що залишилася після кип’ятіння води називається постійною чи залишковою твердістю.
Розрізняють кальцієву твердість води, зумовлену присутністю кальцієвих солей та магнієву твердість, що пов'язана з присутністю магнієвих солей. Сумарна кальцієва та магнієва твердість називається загальною твердістю.
Твердість води виражається в ммоль-екв/дм3 (моль/м3), раніше – мг-екв/л. Таким чином, 20.04мг кальцію Са2+ зумовлюють 1 мг-екв/л кальцієвої твердості; 12.16 мг магнія Mg2+ - 1 мг-екв/л магнієвої твердості. Загальну твердість води визначають по формулі:
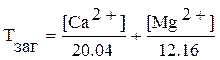 ,ммоль-екв./л (5.7)
,ммоль-екв./л (5.7)
де Са2+, Mg2+ - вміст кальцію та магнію в одному літрі води в мг.
Твердість природної води залежить від джерела та пори року. Під час весняних паводків твердість води поверхневих басейнів зменшується, а в зимній період зростає. В зв'язку з різноманіттю води в природі та природно-антропогенним характером формування її якості класифікація вод має велике значення.
В основу ранніх класифікацій вод, що розроблялися В.І.Вернадським, О.А.Алекіним, було положено загальне солевміщення (ступінь мінералізації) та вміст іонів: 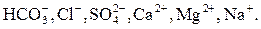
В таблицях 5.2- 5.6 та на рисунку 5.1 наведені різноманітні класифікації вод, які цікаві тим, що дозволяють орієнтовно оцінити можливість та область використання тих чи інших методів очистки, в тому числі іонообмінного та електролізу.
Таблиця 5.2– Класифікація природно-антропогенних вод за загальним солевмістом та твердістю
| По солевмісту | г/л | По загальній твердості | ммоль-екв./л |
| Слабомінералізована | 0.1–5.0 | Дуже м’яка М’яка | 1.5 1.5...3.0 |
| Середньомінералізована | 5.0–30.0 | Середньої твердості Доволі тверда Тверда | 3.0...4.5 4.5...6.0 6.0...10.0 |
| Сильномінералізована | Дуже тверда | 10.0..12.0 та більше12 | |
| Примітка: морська вода характеризується загальною твердістю більше 65 ммоль-екв./л. |
Таблиця 5.3 – Класифікація природно-антропогенних вод за загальним вмістом солі та за переважним вмістом аніонів
| Прісні води | Солоні води | ||||||||||||||
| Ультрапрісна 0.2мг/л | Прісна 0.2–0.5 мг/ л | Прісна з підвищеною мінералізацією 0.5-1мг/л | Солонувата 1-3 мг/ л | Слабосолона 3-10 мг/ л | Солона з підвищеною солоністю 10-35 мг/ л | Дуже солона – перехідна до розсолу 35-50 мг/ л | Ропна 50-400 мг/ л | ||||||||
| Гідрокарбонатна | Гідрокарбонатно-сульфатна | Сульфатно-хлоридна | Переважно хлоридна | Хлоридна | |||||||||||
| Вода рік і прісних озер, підземна вода | Вода солоних озер, болотна та підземна води | Вода океанів та більшості морів | Природні розсоли (ропа), вода деяких морів | ||||||||||||
| Економічно прийнятні варіанти очистки | |||||||||||||||
| 1. Повне іонообмінне знесолювання. 2. Пом'якшення іонним обміном. | 1. Повне іонообмінне знесолення 2. Те ж саме, в поєднанні з декарбонізацією. 3. Пом'якшення іонним обміном 4. Селективний відбір окремих домішок іонним обміном | 1. Часткове чи повне іонообмінне знесолювання, в тому числі з коагуляцією та декарбонізацією. 2. Іонообмінне знесолювання в поєднанні з електродіалізом. 3. Пом'якшення іонним обміном. | 1.Опріснення іонним обміном (Сиротермпроцес). 2.Опріснення електродіалізом 3.Опріснення іонним обміном в поєднанні з електродіалізом 4.Cелективний відбір окремих домішок іонним обміном | 1.Опріснення електродіалізом 2.Опріснення іонним обміном в поєднанні з електродіалізом 3.Опріснення зворотним осмосом в поєднанні з іонним обміном. 4.Селективний відбір окремих домішок іонним обміном. | 1.Опріснення електродіалізом або зворотним осмосом з використанням іонообмінної обробки в якості допоміжної операції 2.Селективний відбір цінних компонентів іонним обміном | 1.Селективний відбір цінних компонентів (наприклад, брому) іонним обміном | |||||||||
Таблиця 5.4 – Класифікація вод за фазово-дисперсним станом домішок
| Група | Назва домішок | Розмір частинок, мкм | Характеристика домішок | |
| Гетерогенна система | ||||
| I | Суспензії | 10-1 | Суспензії та емульсії, які обумовлюють каламутність води: мікроорганізми, планктон та глинисті домішки. | |
| II | Колоїдно-розчинені речовини | 10-1 – 10-2 | Колоїди (високомолекулярні сполуки та ін.), які обумовлюють окисність кольоровість води; віруси. | |
| Гомогенна система | ||||
| III | Молекулярно-розчинені речовини | 10-2 – 10-3 | Гази, розчинні в воді; низькомолекулярні органічні речовини, які надають запах та присмак. | |
| IV | Речовини, дисоційовані на іони (електроліти) | 10-3 | Солі, кислоти, основи, що надають воді твердість, лужність та певну мінералізацію. | |
| Класифікація вод по трофності: 1. Дистрофна, тобто з дуже малим вмістьм біогенних речовин (така вода не може забезпечити розвиток гідробіонтів); 2. Мезотрофна – з середнім вмістом біогенних речовин; 3. Евтотрофна – з великим вмістом біогенних речовин (не може бути використана не тільки в якості питної, але і в промисловому водопостачанні, так як значно ускладнює функціонування систем оборотного водопостачання, відбувається біологічне обростання обладнання). Ця вода важче піддається очищенню при іонообмінному знесолюванні; аніонообмінні фільтри швидко виходять з ладу. Вода, яка містить органічні речовини, так звана сапробна, підрозділяється, в свою чергу на: 1. Олігосапробну, тобто з малим вмістом органічніх речовин (з перманганатною окисністю <10 мг О2/л); 2. Мезосапробну, тобто з середнім вмістом органічних речовин (10... 30 мг О2/л); 3. Полісапробну, тобто з великим вмістом органічних речовин (>30 мг О2/л). Іонообмінному знесолюванню підлягає, як правило, олігосапробна вода і в деяких випадках – мезосапробна. Полісапробна вода створює істотні труднощі при знесолюванні іонітами і тому попередньо повинна бути переведена в олігосапробну або в мезосапробну шляхом відповідної обробки (коагуляція, озонування, адсорбція на активованому вугіллі, сорбція на спеціальних іонітах). Класифікація вод по трофності і, перед усім, по сапробності може бути розповсюджена і на стічні води. В цьому випадку господарсько-побутові стічні води, а також забруднені органічними сполуками стічні води хімічних підприємств, в тому числі які пройшли біологічну очистку, очистку озонуванням, потрібно вважати полісапробними. Тільки стічні води, які пройшли, крім того ще і доочистку із застосуванням сорбентів, можуть вважатися мезо- або олігосапробними. | ||||
Таблиця 5.5 – Гігєнічна класифікація водних об’єктів за ступенем забруднення
| Ступінь забруднення | Показники забруднення для водних об'єктів І та ІІ категорій | Індекс забруднення | ||||||
| органо-лептич | токсикологіч. | санітарний режим | бактеріологічний | |||||
| Зап. присмак (бали) | ГДКорг (ступ. перев.) | ГДКтокс (ступінь перевищ.) | БПК20 мг/дм3 | Розчинений кисень мг/дм3 | Кількість лактозопозитивних кишкових паличок в 1 дм3 | |||
| І | ІІ | |||||||
| Допустима | менше 104 | |||||||
| Помірна | 104... 105 | |||||||
| Висока | 105... 106 | |||||||
| Надзвичайно висока | >4 | >8 | >8 | >10 | більше 106 | |||
| Примітка: Допустимий ступінь забруднення – визначає придатність водного об'єкта для всіх видів водокористування без обмежень. Помірний ступінь забруднення – свідчить про певну небезпеку для населення культурно-побутового водокористування на водному об'єкті. Його використання як джерела господарсько-питного водопостачання, без зниження рівня хімічного забруднення на очисних водопровідних спорудах може призвести до появи різних симптомів інтоксикації у частини населення (особливо при наявності токсичних речовин 1 і 2 класів небезпеки). Високий ступінь забруднення – вказує на безумовну небезпеку культурно-побутового водокористування на водному об'єкті. Неприпустимо використання такого водного об'єкту як джерела господарсько-питного водопостачання. Надзвичайно високий ступінь забруднення – визначає абсолютну непридатність водного об'єкту для всіх видів водокористування. |

Таблиця 5.6 – Класифікація стічних вод за умовами їх утворення і методи очистки
| Методи попередньої очистки | Методи іонообмінної очистки | Марки іонітів, що застосовуються | Шляхи доцільного повторного використання |
| Група1. Господарчо-побутові, міські стічні води, слабко мінералізовані. Утворюються в процесі використання питної води (підготовленої річної або підземної) для господарчих потреб. Основні забруднення – механічні, хімічні (органічні і неорганічні), мікробіологічні. Основні домішки – завислі і колоїдні речовини, віруси, бактерії; розчинні солі (в тому числі: фосфати, солі амонію, нітрати і нітрити), токсичні речовини, органічні сполуки (продукти метаболізму, пестициди, фарбники, ПАР). | |||
| Механічні (відстоювання), біологічні, реагентні (хлорування або озонування); (оброблені вапном з метою видалення фосфатів). | Пом'якшення | Катіоніти типу КУ-2, сульфовугілля, КУ-1 та ін. в Н-формі (з наступною декарбонізацією) або в Na-формі. | Енергетична вода для живлення котлів низького і середнього тисків. |
| Механічні (відстоювання), біологічні, реагентні (хлорування) з фільтрацією. | Дво- або трьох- ступеневе знесолювання, в тому числі ступінчато-протиточним іоніруванням. | Катіоніти КБ-12П і КУ-2, аніони типу АН-31, АН-18, АН-22, або ЕДЕ-10П, а також аніоніти типу АВ-17. | Енергетична вода для живлення котлів високого тиску. |
| Механічні (відстоювання), біологічні, реагентні (хлорування) і реагентні (оброблені вапном з метою видалення фосфатів). | Одноступінчате знесолювання (до рівня складу додаткової охолоджуючої води). | Катіоніти типу КУ-2 в Н-формі і аніоніти типу АН-18, АН-31 в ОН-формі. | Додаткова охолоджуюча вода безпродувних систем оборотного водопостачання. |
| Те ж саме. | Селективне вилучення біогенного азоту (нітратів). | Аніоніти типу ЕДЕ-10П або АВ-17 в солевій (сульфатній) формі. | Додаткова охолоджуюча вода продувних систем оборотного водопостачання. |
| Те ж саме. | Пом'якшення селективне вилучення нітратів і нітритів. | Катіоніти типу КУ-2 і аніоніти типу ЕДЕ-10П або АВ-17 в солевій формі. | Енергетична вода для живлення котлів низького і середнього тисків. |
| Група2. Промислові стічні води, що утворюються в процесі використання технічної води. Підгрупа 2.1. Продувні слабко-мінералізовані води. Утворюються при продуві систем оборотного водопостачання підприємств (відпрацьована охолоджуюча вода, що була підігріта, зконцентрована при випаровуванні і додатковому забрудненню в результаті контакту з повітрям в градирнях, через негерметичності в теплообмінному обладнанні). Основні забруднення – хімічне (неорганічне) і теплове. Основні домішки – завислі речовини, розчинні солі (хлориди і сульфати Na, Mg, Ca та ін.). Солевміст 1.2 г/л. Склад відповідає граничному (за індексом насичення) складу оборотної охолоджуючої води. |
Продовження таблиці 5.6
| Механічні (фільтрування), реагентні (обробка вапном з коагуляцією). | Дво- або трьох-ступінчате знесолювання, в тому числі із ступінчато-протиточним іоніруванням. | Катіоніти КБ-12П, КУ-2 в Н-формі, аніоніти типу АН-22, АН-31, ЕДЕ-10П в ОН-формі і аніоніти типу АВ-17 в ОН-формі. | Енергетична вода для живлення парових котлів високого тиску. |
| Те ж саме. | Одноступінчате знесолювання (до рівня складу додаткової охолоджуючої води). | Катіоніти КУ-2 в Н-формі, аніоніти типу АН-22, АН-31, ЕДЕ-10П в ОН-формі. | Додаткова охолоджуюча вода безпродувних систем оборотного водопостачання або технологічна вода. |
| Те ж саме. | Опріснення до солевмісту 0.5-0.6 г/л з попереднім пом'якшенням. | Сіротерм-іоніти і катіоніти типу КУ-2. | Те ж саме. |
| Те ж саме. | Одноступінчате знесолювання до рівня солевмісту питної води, з наступним глибоким пом'якшенням. | Катіоніти КУ-2 в Н-формі, аніоніти типу АН-22, АН-31, ЕДЕ-10П в ОН-формі і катіоніти типу КУ-1, КБ-4 в Na-формі. | Енергетична вода для живлення парових котлів низького і середнього тиску. |
| Підгрупа 2.2. Конденсат нагрітого і турбінного пару, слабомінералізовані. Утворюються при конденсації пару в конденсаторах (відпрацьована енергетична вода, знесолена, нагріта, яка містить специфічні забруднення через корозію і негерметичність в теплообмінному обладнанні). Основні забруднення – теплове (60-1300С) і хімічне (неорганічне і органічне). Основні домішки – продукти корозії теплообмінного обладнання (залізо, мідь) і леткі розчинні сполуки. Солевміст – 0.003-0.05 г/л. | |||
| Механічні (фільтрування). | Глибоке знесолювання на фільтрах змішаної дії. | Катіоніти КУ-2-8, КУ-23, КУ-2-8Ф в Н-формі і аніоніти АВ-17-8, АВ-17-8П, АВ-17-8Ф в ОН-формі (змішане завантаження). | Енергетична або технологічна вода. |
| Те ж саме. | Очистка на намивних іонітних або целюлозних фільтрах. | Порошкоподібні катіоніти типу ПКУ-2 в Н-формі або NH-формі і аніоніти ПАВ-17 в ОН-формі або порошкові целюлозні іоніти. | Те ж саме. |
| Те ж саме. | Очистка на сульфовугільних фільтрах. | Сульфовугілля. | Те ж саме. |
Продовження таблиці 5.6
| Підгрупа 2.3. Технологічні стічні води неорганічних виробництв. Утворюються при використанні технологічної води. 2.3.1. Конденсат сокового пару, слабо- і середньо-мінералізований. Утворюються при конденсації пару в процесі випарювання продуктів, що містять середовище - утворюючу воду. Основні забруднення – теплове (до 100оС), механічне, хімічне (неорганічне). Основні домішки – завислі, колоїдні речовини в невеликих кількостях (внаслідок краплеуноса), розчинні леткі неорганічні сполуки. Вміст 1-8 г/л. | |||
| Механічні (фільтрування). | Одноступінчате знесолювання. | Катіоніти КУ-2 в Н-формі, аніоніти типу АН-31 в ОН-формі. | Технологічна вода. |
| Те ж саме. | Двох- або трьох-ступінчате знесолювання. | Катіоніти КУ-2 в Н-формі, аніоніти типу АН-22, АН-31, ЕДЕ-10П в ОН-формі і аніоніти типу АВ-17 в ОН-формі. | Енергетична вода для живлення парових котлів високого тиску. |
| 2.3.2. Маточні розчини, середньо- та сильно-мінералізовані. Утворюються в процесі кристалізації та відокремлення продуктів з розчинів, що містять воду. Основні забруднення – теплове (до 100оС), механічне та хімічне (неорганічне). Основні домішки – завислі, колоїдні та розчинені неорганічні сполуки (в тому числі токсичні). Солевміст > 5 г/л. | |||
| Механічні (відстоювання), коагуляція та фільтрування через зернисту загрузку. | Опріснення до солевмісту 1-2 г/л методом електродіалізу. | Іонообмінні мембрани. | Технологічна (наприклад, середовищеутворююча) вода. |
| Те ж саме (але без попередньої очистки). | Селективневилучення. | Іоніти з комплексо утворюючими властивостями (фосфорно кислотні та карбоксильні катіоніти, аніоніти піридинієвого ряду, поліамфоліти) чи звичайні іоніти з попереднім перетворенням вилучаємих домішок в комплексний іон з високою сорбуємістю. | Те ж саме. |
| 2.3.3. Абсорбційні води, слабо- та середньо-мінералізовані. Утворюються в процесі абсорбції викидних газів виробництва (відпрацьована промивна вода). Основні забруднення див. 2.3.2. | |||
| Механічні (відстоювання), коагуляція та фільтрування. | Селективне вилучення цільових домішок. | Іоніти КУ-2, АВ-17, а також комплексоутворюючі іоніти. | Промивна (абсорбційна) вода. |
| 2.3.4. Промивні води слабомінералізовані. Утворюються в процесі промивання твердих продуктів та виробів (відпрацьована промивна вода). Основні забруднення – механічне, хімічне (неорганічне). Основні домішки – завислі та розчинені неорганічні сполуки, в т.ч. токсичні (важкі метали, хромати, ціаніди та ін.). |
Продовження таблиці 5.6
| Механічні (відстоювання), коагуляція та фільтрування через зернисту загрузку. | Селективне вилучення цінних та токсичних домішок. | Іоніти з комплексо утворюючими властивостями (фосфорно- кислотні та карбоксильні катіоніти, аніоніти пиридінієвого ряду, поліамфоліти), неорганічні синтетичні іоніти, іоніти типу КУ-2, АВ-17. | Промивні води. |
| Підгрупа 2.4. Технологічні стічні води органічних виробництв. Утворюються при використанні технологічних вод. Основні забруднення – механічне, теплове, хімічне. Основні домішки – завислі, колоїдні та розчинені органічні сполуки, в т.ч. токсичні. | |||
| Механічні та біологічні. | Адсорбційна доочищення на іонітах та опріснення. | Іоніти типу ІА-1, АВ-17П, а також катіоніти типу КУ-2, КУ-1, сульфовугілля в Н-формі та аніоніти типу АН-31, АН-22, АВ-17 в ОН-формі. | Технологічна вода для органічних виробництв. |
| Група 3. Поверхневі (дощові, талі) стічні води, слабомінералізовані. Утворюються при випаданні атмосферних опадів на забруднену територію. Основні забруднення – механічне, хімічне (органічне та неорганічне). Основні домішки – завислі, колоїдні, розчинені органічні та неорганічні сполуки, в т.ч. нафтопродукти. | |||
| Механічний (відстоювання в ставках-накопичувачах та фільтрування через зернисту загрузку). | Одноступінчате знесолювання, в т.ч. разом з річною водою, до рівня складу додаткової охолоджуючої води безпродувних систем оборотного водопостачання. | Катіоніти типу КУ-2 в Н-формі та аніоніти типу АН-31, АН-22 в ОН-формі. | Додаткова охолоджуюча вода безпродувних систем оборотного водопостачання. |
| Те ж саме. | Опріснення, в т.ч. разом з продувними стічними водами, до солевмісту додаткової охолоджуючої води продувних систем оборотного водопостачання. | Те ж саме. | Додаткова охолоджуюча вода продувних систем оборотного водопостачання. |
| Група 4. Колекторно-дренажні (сільськогосподарські) стічні води, слабомінералізовані, слабосолоні. Утворюються при зрошуванні землі поливними водами чи в результаті підйому і забруднення грунтових вод. Основні забруднення – див. гр.3; основні домішки – завислі та колоїдні речовини, розчинні солі (хлориди та сульфати натрію, магнію та ін.), органічні сполуки (пестициди, продукти неповного розкладу рослин), біогенні сполуки. Солевміст 3...5, іноді до 10 г/л. |
Продовження таблиці 5.7
| Механічний (відстоювання), реагентний (коагуляція та вапнування), біологічний та реагентний (хлорування чи озонування). | Іонообмінне глибоке пом'якшення з подальшим опрісненням до солевмісту 0.3-1.0 г/л по методу Сиротерм (коли сорбуються і катіони, і аніони) чи електродіалізом. | Катіоніти типу КУ-2 в Na-формі і Сиротерм-іоніти чи іонообмінні мембрани. | Поливні (с/г) води. |
| Те ж саме. | Опріснення до солевмісту 0.3-1.0 г/л. | Катіоніти типу КУ-2 в Н-формі і аніоніти типу АН-22, АН-31 в ОН-формі. | Те ж саме. |
| Група 5. Рудникові води, слабомінералізовані. Утворюються в результаті підйому і забруднення грунтових вод, а також накопичення атмосферних опадів. Основні забруднення – див. гр.3. Основні домішки – завислі та колоїдні речовини, розчинні солі (в т.ч. важких металів), біогенні сполуки, нафтопродукти. Солевміст 0.4...2.0 г/л. | |||
| Механічний (відстоювання та фільтрування через зернисту загрузку). | Одноступінчате знесолювання та селективне вилучення біогенних елементів та токсичних металів. | Іоніти типу КУ-2, АН-22, АН-31, АВ-17, а також іоніти з коплексноутворюючими властивостями. | Додаткова охолоджуюча вода систем оборотного водопостачання замість свіжої річної води. |
| Механічний та реагентний (вапнування з метою видалення важких металів та фосфатів). | Доочищення від біогенних та токсичних сполук. | Іоніти з комплексноутворюючими (селективними) властивостями. | Спуск у водоймища (при відсутності споживачів). |
| Те ж саме. | Глибока іонообмінне очищення від катіонів 2-х та 3-х валентних металів та подальше опріснення методом Сиротерм до залишкового солевмісту 0.3...0.6 г/л. | Катіоніти типу КУ-2 чи комплексоутворюючі іоніти та Сиротерм-іоніти. | Додаткова охолоджуюча вода систем оборотного водопостачання чи технологічна вода. |
Для пом'якшення води використовують два методи: осадження та іонний обмін.
Для осадження кальцію та магнію найбільш широко використовують соду, вапно, фосфат натрію та ін. Вапно взаємодіє з солями магнію та осаджує магній у вигляді гідрооксиду:
MgCl2 + Ca(OH)2 = Mg(OH)2↓ + CaCl2 (5.8)
Сода взаємодіє з солями кальцію, утворюючи важкорозчинний карбонат кальцію:
CaSO4 + Na2CO3 = CaCO3¯ + Na2SO4 (5.9)
Для видалення карбонатної твердості методом осадження використовують вапняковий, натронний та содовий методи.
Вапняковий метод використовують при високій карбонатній твердості (Тк), малій некарбонатній (Тнк):
Ca(HCO3)2 + Ca(OH)2 = 2CaCO3¯ + 2H2O (5.10)
Mg(HCO3)2 + 2Ca(OH)2 = 2CaCO3¯ + Mg(OH)2¯ + 2H2O (5.11)
Підвищення температури, створення надлишкової кількості Са(ОН)2, перемішування – покращують ефект зниження Тк, а також зниження загального солевмісту та вільного СО2.
Натронний метод.
Ca(HCO3)2 + 2NaOH = CaCO3¯ + Na2CO3 + 2H2O (5.12)
Mg(HCO3)2 + 4NaOH = Mg(OH)2¯ + 2Na2CO3 + 2H2O (5.13)
Содовий метод.
Ca(HCO3)2 + Na2СO3 = CaCO3¯ + 2NaНCO3 (5.14)
Mg(HCO3)2 + Na2СO3 = MgСO3¯ + 2NaНCO3 (5.15)
На практиці часто використовують вапняково-содовий метод (Тк>>Тнк). Максимальна ступінь пом'якшення вапняково-содовим методом 0,3...0,5 ммоль-екв./л.
Для видалення некарбонатної твердості використовують содовий та фосфатний методи.
Содовий метод.
CaSO4 + Na2CO3 = CaCO3¯ + Na2SO4 (5.16)
MgSO4 + Na2CO3 = MgCO3¯ + Na2SO4 (5.17)
Фосфатний метод.
3CaSO4 + 2Na3РO4 = Ca3(РO4)2¯ + 3Na2SO4 (5.18)
3MgSO4 + 2Na3РO4 = Mg3(РO4)2¯ + 3Na2SO4 (5.19)
При фосфатному методі пом'якшення води максимальна ступінь пом'якшення 0.05 ммоль/л.
Останнім часом для очистки води, зниження твердості води стали широко використовують іоннообмінний метод
Іоніти - це неплавкі та нерозчинні (чи малорозчинні) речовини, які обмежено набухають у воді. У своїй структурі мають функціональні групи кислотного та основного характеру, що здатні обмінюватись на іони речовин, розчинених в воді. Частіше іоніти представляють собою тверді високомолекулярні полікислоти і поліоснови чи їх солі. В залежності від характера функціональних груп іоніти можуть обмінюватися катіонами (катіоніти) чи аніонами (аніоніти). (Див. таблиці 5.6–5.8, рис. 5.1, де представлені марки іонітів, приведені дані по регенерації відпрацьованих іонітів та схема катіонітового фільтру).
Механізм іонітної очистки.
Тверда вода пропускається через шар катіоніта. При цьому проходить, наприклад, такий процес:
CaSO4 + 2HR ↔ CaR2 + H2SO4 (5.20)
Ca2+ + 2HR ↔ CaR2 + 2H+ (5.21)
 |
де R – залишок молекули катіоніта (смоли, що містять карбоксильні групи – СООН, або сульфогрупи – SO3H та ін.). для водоочищення використовують не тільки органічні, а й неорганічні катіоніти – цеоліти (мінерали) чи пермутити (штучно отримані сполуки), що відповідають Na-катіоніту – Na2O × Al2O3 × 3SiO2 × nH2O і звичайно позначаються Na2R (є й Н+-катіоніти – H2R).
При проходженні води через катіоніт в Н+-формі іони кальцію та магнію обмінюються на іони водню і вода стає кислою. Таку воду не можна використовувати для технічних цілей, бо вона буде викликати корозію труб, руйнувати арматуру і т.д. Тому далі цю воду пропускають через аніоніт в ОН--формі:
H2SO4 + 2ROH Û (R)2SO4 + 2H2O (5.22)
Таблиця 5.7 – Іонообмінна характеристика деяких цеолітів.
| Назва | Обмінні іони | Повна обмінна ємність, ммоль-екв./г |
| Содаліт | Na+ | 7.04 |
| Канкриніт | Na+ | 7.04 |
| Фотазит | Na+, Ca2+, Mg2+ | 5.02 |
| Анальцит | Na+ | 4.95 |
| Шабазит | Ca2+ | 4.95 |
| Гмелініт | Na+, Ca2+ | 4.95 |
| Еріоніт | Na+, Ca2+ | 3.86 |
| Морденіт | Na+ | 2.62 |
| Стильбит | Na+ | 4.24 |
| Гейландит | Ca2+ | 3.45 |
| Кліноптилоліт | Na+, K+, Ca2+ | 2.64 |
| Натроліт | Na+ | 5.30 |
Таблиця 5.8 – Характеристика деяких марок іонітів
| Марка іоніту (іонообмінної смоли). | Характеристика, одержання. | Застосування. | |
| в промисловості | в аспекті охорони навколишнього середовища | ||
| Катіоніти КУ-2-8 | Монофункціональний сильнокислотний сополімеризаційний катіоніт, містить один вид фіксованих іонів - сульфо-групи, приєднані до ароматичних кілець.
 Одержується сульфуванням (сірчаною або хлорсульфоновою кислотою) зерен сополімера з 8% дівинилбензолу (ДВБ). Одержується сульфуванням (сірчаною або хлорсульфоновою кислотою) зерен сополімера з 8% дівинилбензолу (ДВБ).
| В водопідготовці для пом'якшення та знесолювання води; в гідрометалургії для відокремлення та виділення кольорових, рідких металів з пульп поліметалевих руд і розчинів; в гальванотехніці та металообробці для генерації рідких відходів і очистки стічних вод; в хімічній промисловості для очистки і відокремлення різних речовин та розчинів, в якості каталізаторів хімічних реакцій. | 1. Для пом'якшення та знесолювання (разом з аніонітами) господарчо-побутових стічних вод; 2. Для пом'якшення та опріснення чи знесолювання слабомінералізованих продувних та поверхневих стічних вод промислових підприємств; 3. Для глибокої очистки гарячих конденсатів пару від продуктів корозії теплообмінних поверхонь; 4. Для очистки гарячих конденсатів сокового пару хімічних виробництв від домішок катіонів розчинних летких неорганічних сполук та продуктів корозії обладнання; 5. Для очистки промивних вод гальванічних виробництв та металообробки від домішок катіонів рідких та кольорових металів; 6. Для очистки стічних вод від органічних основ (ароматичних амінів) та ін.. Може використовуватися в технології очистки вентиляційних газів хімічних виробництв. |
Продовження таблиці 5.8
| КУ-2-20 | Має гелеву структуру, відрізняється від КУ-2-8 більш високим вмістом ДВБ. Випускається в Н-формі. | Для очистки від домішок розчинів антибіотиків, зокрема стрептоміцину, від домішок неорганічних катіонів та для очистки розчинів гальванічних виробництв. | Для очистки стічних вод кольорової металургії та машинобудування від домішок двох- і трьохзарядних катіонів кольорових та важких металів. |
| КУ-23 | Багатофункціональний сильно кислотний сульфокатіоніт макропористої структури, що містить сульфогрупи. Одержуються сульфуванням гранульованого макропористого сополімера стиролу з ДВБ. | Для пом'якшення та знесолення води в різноманітних галузях промисловості, регенерації відходів в гальванотехніці та металообробці, розділення та очистки різноманітних розчинів в хімічній промисловості; в якості каталізаторів. | Для очистки стічних вод від кольорових та рідких металів; для очистки денатурованих і стічних вод всіх видів (див. КУ-2-8); для оборотної сорбції великих органічних катіонів з водних, неводних та газових середовищ. Може використовуватися для очистки газів від летких основних сполук. |
| КУ-1 | Поліконденсаційний сильнокислотний біфункціональний катіоніт; містить два види іоногенних груп: сульфогрупи і фенольні гідрооксидні. Одержується конденсацією сульфованого фенолу з формальдегідом у кислому середовищі. | Для пом'якшення та знесолення води у водопідготовці; для освітлення цукрових сиропів та гідролізатів; для вилучення іонів міді, цинку з рідкої фази пульпи при збагаченні мідно-цинкових поліметалічних руд. | Для очистки гос.-побут. стічних вод, денатурованих вод; стічних вод органічних виробництв та промивних вод гальванічних виробництв від катіонів важких і лужноземельних металів, домішок, що обумовлюють кольоровість. |
| КБ-2-7П КБ-2-10П | Сополімеризаційні слабокислотні монофункціональні карбоксильні катіоніти макропористої структури. Випускаються і застосовуються в Na-формі. | Для сорбції антибіотиків з нативних розчинів, для відокремлення амінокислот, очистки нікелевих та кобальтових електролітів від домішок заліза, очистки розсолів хлориду натрію від катіонів кальцію та магнію, ін. | Для вилучення катіонів кольорових та важких металів з природно антропогенних та стічних вод, для очистки газів від кислих компонентів, ін. |
Продовження таблиці 5.8
| Аніоніти АВ-17-8 | Сополімеризаційний сильноосновний монофункціональний; гелевої структури, що містить четвертинні бензилтриметиламонійні функціональні групи. Одержується шляхом хлорметилуванням сополімера стиролу з 8% ДВБ із наступним амінуванням триметиламіном. | У водопідготовці для видалення з води іонів слабких кислот (вугільної, кремнієвої); для глибокого знесолювання води та конденсатів у фільтрах змішаної дії разом з катіонітом КУ-2-8; в хімічній та фармацевтичній промисловості для очистки різних речовин та ін. процесів аніонного обміну. | Для очистки стічних вод від аніонних домішок (в т.ч. від аніонних комплексів кольорових та рідких металів); від силікатів, нітратів, нітритів, ціанідів, боратів та ін. аніонних домішок стічних вод хімічної промисловості, кольорової металургії; для очистки газів вентиляційних пристроїв від НF, SiF4 та SO2, SO3 та ін. |
| АВ-17П (АВ-17-10П/0.6 АВ-17-10П/0.8 АВ-17-10П/1.0) | Сополімеризаційні сильноосновні монофункціональні аніоніти з четвертинними бензилтриметиламонійними групами. | У водопідготовці для видалення аніонів слабких кислот; від органічних домішок; для знебарвлення та деіонізації розчинів в цукровому виробництві. | Для вилучення неорганічних та органічних аніонів (в т.ч. аніонних ПАВ, пестицидів та ін.) різних стічних вод; для очистки вентиляційних газів від кислих компонентів та ін. |
| АВ-29-12П | Сополімеризаційний сильноосновний монофункціональний аніоніт макропористої структури; містить четвертинні бензилдиметилетаноламонійні функціональні групи. | У водопідготовці при невисоких вимогах до знесоленої води за залишковим вмістом аніонів кремнієвої та вугільної кислот. | Для очистки госп.-побут. та промислових стічних вод від домішок аніонів неорганічних та органічних кислот, сполук; для очистки повітря від кислих газів. |
| Регенерація відпрацьованих іонітів. Н+-катіоніт висипають з колонки в велику банку з 5% розчином НCl і залишають на 24 години. Потім кислоту зливають, катіоніт переносять у воронку Бюхнера і промивають дистильованою водою до негативної реакції на іон Cl- з AgNO3. Промитий катіоніт знову вводять в колонку. Реакція на присутність іонів Cl-. Іони Cl- з AgNO3 утворюють білий осад Ag Cl, нерозчинний в мінеральних кислотах, але розчинний в водних розчинах NН3, карбонату амонію, ціаніду калію та тіосульфату натрію: Cl– + Ag+ ® AgCl¯ AgCl+2NH3 ® [Ag(NH3)2]+ + Cl– Виконання реакції. До 2-3 крапель досліджуваного фільтрату у пробірці, добавляють 1 краплю розчину НNO3 та 2-3 краплі розчину AgNO3. В присутності Cl–-іонів утворюється білий осад. Аніоніт регенерують 5% розчином NaOH, промивають водою до негативної реакції по фенолфталеїну (відсутність рожевого забарвлення). Промитим аніонітом знову заповнюють колонку. |
Після такої послідовної очистки воду можна використовувати для різних цілей в техніці.
Для парових котлів твердість води повинна бути £0.017 моль/м3 (H2SiO3 £ 30; Fe £ 100, O2 £ 30; мастила £ 0.5 мг/л).
Наприклад, для промислової електроніки використовують демінералізовану воду, яка за якістю перевищує бідистилят (воду подвійної перегонки). Вміст солей Са2+ та Mg2+ - 10-1...10-2 мг/л. Вимоги до якості енергетичної води наведені в таблиці 5.9.
Таблиця 5.9 – Нормативні вимоги до якості енергетичної води
| Показники якості води | Для випарників | Для живлення барабанних котлів з Рпара, МПа | Для живлення прямоточних парогенераторів з параметрами пару | |||
| 4 – 10 | докритич | надкрит | ||||
| Вміст ефіророзчинних речовин, мг/л | 0.3 | 0.3 | 0.3 | 0.3 | ||
| Запах, бали | ||||||
| рН | 6.5-9.5 | 9.1 | 9.1 | 9.1 | 9.5*/9.5 | 9.1*/9.5 |
| Загальна твердість, ммоль–екв./л | 0.5 | 0.2 | ||||
| Вміст, мкг/л | ||||||
| SiO2 | – | – | 40**/ 120 | |||
| SO42– | – | – | – | |||
| NH3 | 800*/ 2000 | 800*/ 3000 | ||||
| N2H4 (вільн.) | ||||||
| NO2– | ||||||
| Fe (заг.:+2,+3) | 100-200 | 50-100 | 20-30 | |||
| Сu2+ | 10-20 | 10-20 | ||||
| Na+ | – | – | – | – | – | |
| O2 | ||||||
| * в чисельнику при наявності в пароводяному тракті сплавів, що мають у своєму складі мідь, в знаменнику – при їх відсутності; ** в чисельнику – для КЕС та опалювальних ТЕЦ, в знаменнику – для ТЕЦ з виробничим відбором пару. |
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 496; Нарушение авторских прав?; Мы поможем в написании вашей работы!