
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема 4. Химическая кинетика и равновесие
|
|
|
|
95. Две реакции при 283 К протекают с одинаковой скоростью. Температурный коэффициент скорости первой и второй реакции равны соответственно 2,5 и 3,0. Как будут относится скорости реакций, если первую из них провести при 350 К, а вторую при 330 К?
96. В начальный момент протекания реакции N2 + 3H2  2NH3 концентрации были равны (моль/л): азота - 1,5; водорода - 2,5; аммиака - 0. Каковы концентрации азота и водорода при концентрации аммиака равной 0,5 моль/л?
2NH3 концентрации были равны (моль/л): азота - 1,5; водорода - 2,5; аммиака - 0. Каковы концентрации азота и водорода при концентрации аммиака равной 0,5 моль/л?
97. Начальные концентрации веществ в реакции СО + Н2О  СО2 + Н2 были равны (моль/л): С(СО) = 0,05; С(Н2Огаз) = 0,06; С(СО2) = 0,4; С(Н2) = 0,2. Вычислите концентрации всех реагирующих веществ после того, как прореагировало 60 % Н2О.
СО2 + Н2 были равны (моль/л): С(СО) = 0,05; С(Н2Огаз) = 0,06; С(СО2) = 0,4; С(Н2) = 0,2. Вычислите концентрации всех реагирующих веществ после того, как прореагировало 60 % Н2О.
98. Реакция идет по уравнению 4NH3 + 5O2  4NO + 6H2O. Как изменится скорость реакции, если увеличить давление в 2 раза?
4NO + 6H2O. Как изменится скорость реакции, если увеличить давление в 2 раза?
99. Реакция протекает по уравнению Na2S2O3 + H2SO4 = Na2SO4 + H2SO3 + S. Как изменится скорость реакции после разбавления реагирующей смеси в 4 раза?
100. Вычислите при какой температуре реакция закончится за 45 минут, если при 293 К на это требуется 3 часа. Температурный коэффициент равен 3,2.
101. Для практической остановки реакции применяют быстрое охлаждение реакционной смеси. Определите, во сколько раз изменится скорость реакции при охлаждении реакционной смеси с 40 до -10 градусов Цельсия, если температурный коэффициент реакции равен 2.7
102. На сколько градусов нужно повысить температуру, чтобы скорость реакции возросла в 90 раз? Температурный коэффициент равен 2,7.
103. Определите равновесную концентрацию водорода в реакции 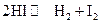 , если
, если
104. исходная концентрация HI составляет 0,55 моль/л, а константа равновесия равна 0,12.
105. При синтезе фосгена имеет место равновесие реакции Сl2 + CO  COCl2. Определите исходные концентрации хлора и оксида углерода, если равновесные концентрации в моль/л равны: [Cl2] = 2,5; [CO] = 1,8; [COCl2] = 3,2.
COCl2. Определите исходные концентрации хлора и оксида углерода, если равновесные концентрации в моль/л равны: [Cl2] = 2,5; [CO] = 1,8; [COCl2] = 3,2.
106. Реакция протекает по уравнению 2А  В. Исходная концентрация вещества А равна 0,2 моль/л. Константа равновесия реакции 0,5. Вычислите равновесные концентрации реагирующих веществ.
В. Исходная концентрация вещества А равна 0,2 моль/л. Константа равновесия реакции 0,5. Вычислите равновесные концентрации реагирующих веществ.
107. В каком направлении сместится равновесие реакции 2СО + 2Н2  СН4 + СО2, если концентрации всех реагирующих веществ уменьшить в 3 раза?
СН4 + СО2, если концентрации всех реагирующих веществ уменьшить в 3 раза?
108. Равновесие в системе 2 NO2  2NO + O2 при некоторой температуре установилось при концентрациях в моль/л: [NO2] = 0,06; [NO] =0,24; [O2] = 0,12. Определите константу равновесия и рассчитайте исходную концентрацию NO2.
2NO + O2 при некоторой температуре установилось при концентрациях в моль/л: [NO2] = 0,06; [NO] =0,24; [O2] = 0,12. Определите константу равновесия и рассчитайте исходную концентрацию NO2.
109. Определите равновесные количества веществ в реакции СО2 + Н2  СО + Н2О(газ), если константа равновесия при некоторой температуре равна 1 и для реакции было взято 1 моль углекислого газа и 3 моль водорода.
СО + Н2О(газ), если константа равновесия при некоторой температуре равна 1 и для реакции было взято 1 моль углекислого газа и 3 моль водорода.
110. При некоторой температуре константа равновесия реакции Н2+ Вr2  2НВr равна 1. Определите состав равновесной смеси, если для реакции были взяты 1 моль водорода и 2 моль брома.
2НВr равна 1. Определите состав равновесной смеси, если для реакции были взяты 1 моль водорода и 2 моль брома.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 811; Нарушение авторских прав?; Мы поможем в написании вашей работы!