
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Потенціометричний метод аналізу
|
|
|
|
Контрольні запитання для самопідготовки
1. Охарактеризуйте потенціометричний метод аналізу за чутливістю та вибірковістю.
2. Що таке рівноважний потенціал(Ер)? Поясніть чому Ер вимірюють за умови нульової іонної сили (І =0)?
3. Що таке гальванічний елемент? Що таке електрорушійна сила (ЕРС) гальванічного елементу?
4. *Чи можна виміряти рівноважний потенціал електролітичної комірки за допомогою вольтметру постійного струму?
5. Потенціал яких окисно-відновних систем можна можна розрахувати за рівнянням Нернста?
6. Поясніть відмінності між стандартним і формальним окисно- відновним потенціалами?
7. Що таке гальванічний елемент? Як розрахувати його електрорушійну силу (ЕРС)?
8. Назвіть основні вимоги до індикаторного електрода та електрода порівняння. Поясніть призначення кожного з них в комірці.
9. Які типи індикаторних електродів застосовуються в потенціометрії?
10. Опишіть принцип роботи хлорид-срібного та насиченого каломельного електродів порівняння.
11. Опишіть принцип роботи стандартного водневого електроду.
12. *За яких умов срібний електрод працює як електрод І роду, а за яких - як електрод ІІ роду? Напишіть рівняння залежності потенціалу електрода від концентрації потеціалутворюючого іону для обох випадків.
13. *Чи доцільно застосовувати такі метали: а) ртуть; б) свинець; в) кадмій; г) платина; д) хром для виготовлення індикаторних електродів? Якщо недоцільно, напишіть рівняння, які перешкоджають їх застосуванню.
14. *Чи доцільно застосовувати такі метали: а) ртуть; б) свинець; в) кадмій; г) платина; д) хром для виготовлення допоміжних електродів? Якщо недоцільно, напишіть рівняння, які перешкоджають їх застосуванню.
15. Чому цинковий електрод можна застосовувати як електрод першого роду лише в нейтральному середовищі? Напишіть рівняння реакцій, які перешкоджають застосуванню цинкового електроду першого роду в сильно кислому та лужному середовищі.
16. Поясніть відмінності утворення потенціалу на металічному електроді першого роду та іонселективному електроді (ІСЕ)?
17. Які основні типи мембран застосовують для виготовлення ІСЕ?
18. Поясніть механізм виникнення потенціалу в мембранах ІСЕ: а) скляних б) кристалічних, в) рідких,.
19. Що таке коефіцієнт селективності іонселективного електрода? Якими величинами kA/B характеризуються вибіркові до іону А електроди?
20. Запишіть рівняння Нікольського для ІСЕ, зануреного в розчин іону А (визначуваний) та В (заважаючий). Які сталі в ньому характеризують саме ІСЕ?
21. Що означає термін «електродна функція»? Від чого залежить крутизна електродної функції? Як її величина пов’язана із чутливістю визначення.
22. Поясніть чому рівноважний потенціал електроду залежить від log a i, а не від log [i]?
23. Поясніть принцип дії скляного електроду. Зобразіть схематично його будову
24. Як потрібно готувати скляний електрод рН-чутливий електрод до першого застосування? В яких умовах необхідно зберігати скляний електрод, щоб він не втратив водневу функцію? Чому скляний електрод періодично слід калібрувати за розчинами з відомим рН?
25. В якому інтервалі доцільно застосовувати скляний електрод для вимірювання рН розчину? Назвіть причини виникнення похибок поза межами цього інтервалу.
26. В чому відмінність між прямою потенціометрією та потенціометричним титруванням? Назвіть переваги кожного методу.
27. Особливості застосування реакцій нейтралізації, окиснення-відновлення та осадження в потенціометричному титруванні. Перерахуйте фактори, які впливають на величину стрибка титрування в кожному випадку.
Вправи для самопідготовки
1. Напишіть рівняння катодної та анодної реакцій, які відповідають за виникнення різниці потенціалів в комірці: Ag | AgCl(нас), HCl (0,100 M) || FeCl2 (0,01 M), FeCl3 (0,05 М) | Pt. Розрахуйте ЕРС комірки, Е0AgCl/Аg,Cl- = 0,224 В, E0Fe3+/Fe2+ = 0,771 B.
2. Розрахуйте потенціал мідного електроду в розчині, що містить 0,01 М купруму (ІІ)
нітрату та 0,01 М купрум (ІІ) сульфату. Оцініть помилку, що буде внесено в розрахунки, якщо не враховувати іонну силу розчину.
3. Виведіть залежність від рН формального потенціалу електрохімічної системи 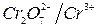 за умови
за умови 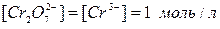 . В якому середовищі (кислому чи лужному) біхромат-іон є сильнішим окисником?
. В якому середовищі (кислому чи лужному) біхромат-іон є сильнішим окисником?
4. Який з вказаних напівелементів буде катодом, а який анодом при їх об’єднанні в гальванічного елементу в поєднанні один з одним? Наведіть схему елементу та розрахуйте його ЕРС. а). 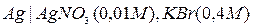 ; б).
; б). 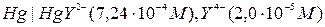 .
.
5. Схематично зобразіть комірку для визначення [S2-] із срібним індикаторним електродом (катод) та 1 моль-екв.л-1 каломельним електродом порівняння. Виведіть рівняння, що пов`язує ЕРС комірки з концентрацією сульфід-іона (якщо Ej =0).
6. Розрахуйте стандартний потенціал напівреакції Ag2S(тв)+2e«2Ag(тв)+S2-. Відомо, що стандартний потенціал напівреації Ag++1e«Ag дорівнює 0,799 В, КS0(Ag 2 S)=6,3.10-50.
7. Розрахуйте потенціал скляного рН-чутливого електрода (К = 0,28 В, S = 0,05 В), зануреного в 10 мл розчину 0,1 М ацетатної кислоти, відтитрованої 0,1 М розчином NaOH до точки еквівалентності.Для HAc pKа = 4,8.
8. *Які експериментальні дані необхідно отримати при визначенні pKа ацетатної кислоти. Запишіть рівняння за яким їх обробляють. В яких координатах будують отриману пряму? Як з графіку визначити величину pKа?
|
|
|
|
|
Дата добавления: 2015-05-29; Просмотров: 629; Нарушение авторских прав?; Мы поможем в написании вашей работы!