
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Н - глу Арг энкефалины лей тре тре лей глу ом 4 страница
|
|
|
|
В физиотерапи боли широко используются воздействия электрического тока на центральную и периферическую нервные системы. Например, снятие боли возможно методом центральной анальгезии - электронаркозом. Предполагается, что импульсные токи, спользуемые при электронаркозе блокируют проведение нервных импульсов в лобных долях, уменьшают активность эмоциогенных зон гипоталамуса и лимбической системы. При хронических болях используется электростиуляция серого околоводопроводного вещества, ядер шва при помощи вживленных в эти образования электродов. В основе развивающейся при этом воздействии анальгезии лежит запуск серотонинергических механизмов.
Существенного эффекта можно добиться путем чрезкожной транскраниальной электроаналгезии, при которой электроток действует на головноймозг через кожные покровы и кости чеpeпa. При этом способе имеет место электрическая стимуляция антиноцицептивных образований ствола мозга, активация которых, помимо аналгетического эффекта, приводит и к другим положитель-ным проявлениям науровне целостного организма: оптимизации кровообращения, стимуляции заживления ран, повышения неспецифической резистентности. Всё это обусловлено увеличением образования эндогенных опиоидных пептидов. Обоснованность этого предположения косвенно подтверждается налоксон - чувствительностью данного способа обезболивания.
Транскраниальная электроаналгезия может быть использована как компонент анестезиологического пособия. Список болевых синдромов, при которых этот методприводит к хорошим результатам достаточно обширен, хотя в ряде случаев, например, при болях центрального генеза его использоване малоэффективно. Помимо этогo транскраниальная электроаналгезия может быть использована для купирования абстинентного алкогольного синдрома или опиоидной абстиненции.
4.3.3. Акупункурные методы исследования.
Отдельного разбора заслуживает акупунктурное обезболивание, которое в настоящее время применяется в его классическом варианте - иглорефлексотерапия и современном - электроаку-пунктурном. Этот вид аналгетического пособия может быть использован при проведении операти-
вных вмешательств, в послеоперационном периоде, для лечения болевых синдромов различной этиологии (травматического, сосудистого, полиневритического и т.д.). Возможности акупунктурного обезболивания позволяют выбрать такой тип воздействия, при котором будет не только купи-роваться болевой синдром, но и стимулироваться механизмы саногенеза.
Считается, что в основе акупунктурной аналгезии лежат два механизма: нейрональный и ней-рохимический, благодаря которым реализация антиноцицептивных вляний происходит на самых различних уровнях: в спинном мозге, таламусе, реткулярной формации и т.д.
Нейрональный механизм акупунктурного аналгетического эффекта состоит в изменении фун-кционирования нейронов ответственных за проведение болевых импульсов, в увелчении поступ-ления неноцицептивной информации в ретикулярную формацию и другие образования ствола, что, в свою очередь, приводит к стимуляции нейронов, ответственных за антиноцицептивную активность.
Нейрохимический механизм акупунктурной аналгезии в основном сводится к влиянию на образование эндогенных опиоидных пептидов. При этом отмечается корреляция между обезболивающим эффектом и концентрацией эндорфинов и энкефалинов. Предполагается, что акупункту-ра, стимулируя нейроны гипоталамуса, повышает выработку опиоидов и выделению их в кровь и спино-мозговую жидкость, что приводит к блокированию проведения болевых импульсов, начиная со спинного мозга и, кончая корой. Отмена аналгезирующего эффекта акупунктуры налоксаном является косвенным подтверждением этого положения.
Помимо активации опиоидной системы предполагается также запуск адренергических механизмов обезболивания и стимуляция нисходящих тормозных влияний. Помере нарастания продолжительности акупунктурного воздействия доминирующее значение приобретают серотонин-ергические механизмы, не исключается также и подключение ГАМК-ергических систем.
Среди способов акупунктурного воздействия следует выделить традиционное механическое воздействие вращающихся игл. Следует отметить, что это достаточно сложная процедура, требующая большого количества участвующих в обезпечении аналгезии. В современной медицине используется также электроакупунктура, при которой на введенные иглы подаётся электрический ток различного характера. Обладая рядом пpеимуществ, этот способ, тем нe менее, не лишён недостатков: быстрая адаптация к воздействию, необходимость установки нескольких аппаратов, электролиз игл и т. д.
4.4. Хирургические методы аналгезии.
Xиpуpгичeкиe методы коррекции были неоднозначны по своим механизмам. Это могут быть воздействия на зону повреждения с целыо устранения причины вызвавшей боль: вскрытие гнойни-ка, вправление вывиха, иммобилизация перелома, удаление камней желчного пузыря или мочевы-водящих пyтей, декомпрессия спинномозговых корешков при радикулитах и ряд дpyгиx хирурги-ческих манипуляций.
Нейрохирургические вмешательства пpeполагают воздействия на нервные структуры: удале-ние неврином, иссечение pyбцов, десимпатизацию и ганглиоэктомию. В тяжёлых случаях при на-личии сильнейших болей, как правило, в инокурабильных ситуациях возможно прoведение операций на центральной нервной системе с пересечением проводящих путей или разрушением отдель-ных структурных образований головного мозга:
- спинно - таламическая хордотомия;
- фронтальная лейкотония;
- разрушение таламических ядер при фантомных болях;
- различные виды трактотомий и химический невролиз (некроз нервных волокон спиртом, фенолом);
- алкоголизация гипофифиза.
Показаниями к этим операциям являются хронические нестерпимые боли, при которых не удаётся облегчить страдания пациента другими способами.
4.5. Лекарственная терапия болевого синдрома.
Фармакологические препараты могут влиять на восприятие боли на различных уровнях структурной организации периферической и центральной нервной системы: рецепторном, проводниковом, в задних рогахспинного мозга, на ypoвне стволовых oбpaзований мозга, в коре больших полушарий. Всю совокупность обезболивающих препаратов можно разделить на три группы: средства общего, местного и комбинированного воздействия.
4.5.1. Лекарственные методы общей аналгезии.
Общий аналгетический эффект присущ препаратам с различными механизмами действия, что накладывает отпечаток на проявления их обезболивающего действия.
Это могут быть cpедcтва для наркоза, под влиянием которых происходит выключение созна-ния и всех видов чувствительности, в том числе и болевой. При этом воздействии сохраняется только регуляторная деятельность жизненно важных центров нервной системы, предполагается что в основе действия лекарственных препаратов используемых для наркоза лежит блокада прове-дения восходящей импульсации в высшие отделы коры. К этой группе относятся средства для ингаляционного наркоза - эфир, фторотан, закись азота, циклопропан, а также препараты для неинга ляционного наркоза - тиопентал натрия, натрий оксибутират, кетамин.
Развитие наркотического сна под влиянием кетамина, тиопентала, оксибутирата натрия или сочетаний типа диазепам-кетамин, дроперидол-фентанил обусловлено влиянием на адрен-, дофамин-, опиатергические и в меньшей степени серотонин-, ацетилхолин- и ГАМК-ергическими системы.
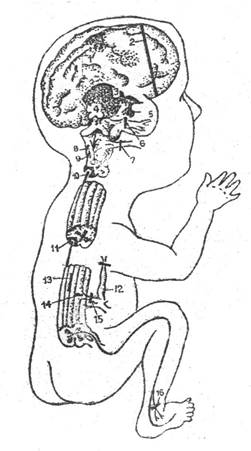
Рис- 5. Нейрохирургические вмешательства, применяемые для облегчения боли.
1 – гиперэктомия, 2 – префронтальная лоботомия, 3 – таламотомия, 4 – мезэнцефальная трактотомия, 5 – гипофизэктомия, 6 – перерезка корешков V черепного нерва, 7 – перерезка IX черепного нерва, 8 – бульбарная трактотомия, 9 – тригеминальная трактотомия, 10 – цервикальная хордотомия, 11 – торакальная хордотомия, 12 – симпатэктомия, 13 – миелотомия, 14 – перерезка тракта Лиссауэра, 15 – перерезка заднего корешка, 16 – перерезка нерва. (по Р. Мельзак, 1981).
4.5.2. Наркотические аналегтики в терапии боли.
Ряд аналгезирущих препаратов могут снижать болевую чувствительность, не выключая созна-ние и не угнетая другие виды чувствительности. Особое место среди них занимает группа опиа-тов, объединённых под общим названием - наркотеческие аналгетики. Ведущим механизмом их обезболиваюшего эффекта, как уже было сказано выше, является способность связываться с опиатными рецепторами, например, морфин связывается с μ- и кси- опиатными рецепторами. Предполагается, что морфин и его аналоги уменьшают интенсивность прохождения болевых импульсов в супраспинальные отделы, усиливают нисходящее антиноцицептивное влияние на cтрyктуры спинного мозга.
Классическим представителем наркотических анальгетиков-опиатов является морфин. На ос-нове его химической структуры были созданы высокоактивные болеутоляющие аналоги, а также его функциональный антагонист - налоксон. По избирательности и характеру взаимодействия с рецепторами наркотические аналгетики подраделяются:
- морфиноподобные агонисты: морфин и его производные (гидроморфин, оксиморфин);
- фентанил и его производные (суфентанил, карфентанил и др.);
- метадон (долофин) и др.;
- кодеин, героин.
Это далеко не полный перечень препаратов этой группы. Особенности аналгетических эф- фектов и краткие характеристики наиболее типичных представителей этого класса препаратов, широко используемых в медицинской практике, представлены ниже.
М о р ф и н действует наиболее эффективно при внутримышечном и подкожном введении. Его фармакологические эффекты непостоянны и зависят от возраста пациента (пожилые люди чувствительнее), фаз менструального цикла и т.п., помимо этого активность морфина и его анало-гов может измениться пoчти на порядок в зависимости от времени суток, сезона.
Главный недостаток препарата - высокий наркогенный потенциал, то есть возможность развития лекарственной зависимости, а также большоe число побочных реакций - угнетение дыхания, тошнота, рвота, спазмы гладкомышчных органов.
П р о м е д о л - в 5 - 6 раз менее активен, чем морфин. Исполъзуется при болевых синдромах средней выраженности, применяется вакушерской практике.
Ф е н т а н и л - обладает очень высокой болеутоляющей активностью. Его использование положило начало нейролептаналгезии, синаптоаналгезии и другим вариантам комбинированного влияния на ноци- и анти- ноцицептивные системы. Легко и быстро фентанил проникает через гемато-энцэфалический барьер.
Несмотря на достаточно большой выбop пpепаратов этой группы с высоким потенциалом действия, всё же в 70% случаев не удаётся добится аналгезирующего результата. Это объясняется неправильным подбором дозы, нарушением режима и способа введения, недостаточно эффектив-ной концентрацией аналгетика в крови.
Широкое применение наркотических аналгетиков ограничивается рядом их побочных эффек-тов. Важнейшим из них являются опиатная толерантность и опиатная зависимость.
Т о л е р а н т н о с т ь или п р и в ы к а н и е - пониженная реакция организма на повторное введение препарата. Развитие привыкания приводит к необходимости повышения дозы. Предполагается, что формирование толерантности к действию лекарств происходит по двум механизмам: согласно первому систематическое потребление препарата снижает его концентрацию в зоне рецепторов, через которые инициируется фармакологический эффект. Это происходит из-за активации матаболизма или элиминации препарата, а также увеличения распределения. Второй механизм предполагает, что, несмотря на высокую концентрацию препарата у peцептopa, чувствительность к нему снижается, вероятно, это более характерно для наркотических аналгетиков.
Наркотические аналгетики - это психоактивные соединения, вызывающие патологическое пристрастие и наркоманию. При систематическом применении их формируется синдром з а в и - с и м о с т и, которая может носить психический и физический характер. При этом психический компонент является самым мощным фактором в формировании непреодолимого стремления к повторным приёмам препарата во всё возрастающих дозах из-за развивающейся толерантности.
Синдром отмены, возникающий при прекращении приёма наркотических препаратов на фоне сформировавшейся зависимости к ним, характеризуется у человека сложным комплексом проявлений:
- вегетативные нарушения - мидриаз, усиление секреции (слёзо- и слюнотечение, потливость), тошнота, рвота, диарея, гипертермия, тахикардия, гипергликемия, повышение артериального давления, отсутствие аппетита, уменьшение массы тела, зевота, насморк с чиханием, жар и озноб, парестезии, мышечные боли;
- психические отклонения проявляются нарушениями сна, формированием тревоги, безпокой-ства, дисфории, влечение к наркотику.
Опиатная зависимость является преувеличенной копией естественной зaвисимocти от эндогенных опиоидов. Она объясняется подпороговым возбуждением нейронов, имеющих опиатные рецепторы, которое формируется при прекращении действия опиоидов.
4.5.3. Ненаркотические аналгетики в терапии боли.
Ненаркотические аналгетики представляют собой достаточно пёструю группу соединений, от-личающихся друг от друга как по структуре, так и по фармакологическим эффектам. К ним относятся: производные пирозалона - антипирин, амидопирин, анальгин, бутадион; салициловой кислоты - салицилат натрия, ацетилсалициловая кислота, салициламид и др.; индола - индометацин; анилина - фенацитин, парацетамол. Все эти препараты обладают комплексным влиянием на организм человека, однако, как правило, преобладает одно из возможных воздействий: аналгезирующее, жаропонижающее или противовоспалительное действие. Обезболивающий эффект может быть результатом совокупности эти влияний.
Противовоспалительное действие ряда нестероидных препаратов (аспирина, бутадиона, индометацина, вольтарена и др.) предполагает их аналгетический эффект, но это не исключает возможности прямого влияния на болевые механизмы, например, ацетилсалицилаты блокируют циклооксигеназу и, тем самым, снижают синтез медиаторов боли простагланднов, тормозя помимо этого активацию компонентов кининовой системы.
Анальгин и амидопирин, вероятно, действуют на уровне подкорковых образований, снижая прохождение болевых импульсов на уровне 3-го релейного переключения. Косвенно этот механизм подтверждается тем, что их эффект усиливается в комбинации с барбитуратами, кодеином и др.

Рис. 6. виды местной анестезии (Л.В. Авдей, И.К. Данусевич, 1976)
Как правило, ненаркотичсские аналгетики эффективны только при невралгических, мышечных, суставных, зубных и головных болях и неэффективны при травмах, ожогах, заболеваниях внутренних органов.
В дополнение к основным обезболивающим препаратам используются лекарственные вещес-тва других фармакологических групп, которые, не оказывая непосредственного анализирующего действия, влияют на тот или иной компонент механизмов боли:
- можно управлять психоэмоциональным состоянием пациента, используя седативные или снотворные средства, нейролептики, психотропные препараты бензодиазепинового ряда или анти-депресанты. Достигаемый при этом эффект снижения психоэмоционального напряжения, облегчает ожидание боли, изменяет субъективное отношение к ней. Установлено таже, что антидепресан-ты повывают уровень серотонина.
- антигистаминные препараты, уменьшая образование гистаминов или разрушая его, снижают тем самым его алгогенный эффект.
- аналгетическое действие клофелина связано с его мощным гипотензивным влиянием.
- противосудорожные препараты (тегритон, финлепсин, диазепам) подавляют гиперреактивность болевой системы.
4.5.4. Местная анестезия в лечении боли.
В особую группу следует выделить средства местной анестезии, которые, не нарушают сознание и мышление, устраняют боль за счёт местного влияния на нервные окончания или проводники. Выделяют следующие виды местной анестезии: поверхностную или терминальную, инфильтрационную, проводниковую и спинно-мозговую. К местным анестетикам относятся: анестезин, новокаин, бентаин, лидокаии, тримекаин, совкаин и др.
Механизмы действия местных анестетиков разнообразны: они подавляют формирование по-тенциала действия, угнетают ионную проницаемость, тормозят аксональный транспорт белков. Некоторые из них, например, дикаин и кокаин являются антагонистами алгогенов типа гистамина и серотонина. Аналгетический эффект местных анестетиков снижается по мере их инактивации при обезвреживании в печени в ферментативных реакциях гидролиза или выведении из организма в неизмененном виде.
4.5.5. Перспективные направления в альгологии.
Одним из перспективных направлений в альгологии является регионарная анальгезия, которая предполагает целенаправленное введение опиатов или опиоидов в различные структурные образо-вания ЦНС. Выраженный и стойкий анальгетический эффект, который наблюдается при этом, обусловлен созданием высокой концентрации анальгетиков в зонах непосредственно отвечающих за прохождение ноцицептивной информации. При других же способах введения только около 0,01% от общего количества поступивших в организм опиатов попадает в головной мозг. Традиционное для медицинской практики нашего времени использование для анальгезии высоких доз опиатов, объясняет обилие и выраженность побочных эффектов и осложнений при их применении. Дело в том, что при обычных способах введения обезболивающих препаратов для достижения анальгетического эффекта человеку вводятся заведомо завышенные дозы того же морфина (энтерально - 30 мг, внутримышечно или внутривенно - 10 мг), хотя действенная концентрация может быть получена при введении всего 2-5 мг морфина эпидурально или 0,25-0,5 мг интратектально.
При локальном целенаправленном введении препаратов выявляются ещё целый ряд преимуществ, например, при эпидуральном введении морфина анальгетический эффект развивается уже в первые пять минут и длится 8-12 часов и более, интратектaльное введение характеризуется ещё большей длительностью анальгезии. В принципе, этим путём возможно введение любых опиатов, причём установлено, что они не оказывают токсического влияние на нервную ткань в месте инъекции.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 502; Нарушение авторских прав?; Мы поможем в написании вашей работы!