
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Полный термодинамический анализ процесса получения этилена
|
|
|
|
В своем расчете мы хотели бы рассмотреть реакцию получения этилена, основанную на реакции пиролиза пропана, так как она является наиболее распространенной и важной для промышленного производства этилена.
Термодинамический анализ начинают выполнять для основного превращения в газовой фазе. При этом необходимо установить влияние температуры, давления, мольного соотношения реагентов, инертного разбавителя на положение равновесия в системе, то есть на равновесную степень конверсии исходного этилена и выход целевого продукта этанола (его содержание в равновесной смеси).
Проведем предварительный расчет процесса. Для этого необходимо ввести допущение, что побочных реакций не протекает, селективность процесса по целевому продукту 100% (хотя в промышленности и так достигается такой подбор условий, что вероятность протекания побочных процессов крайне мала и селективность процесса 95% и выше). Упрощенная схема реакции имеет вид: 
Для определения параметров процесса необходимо владеть надёжными термодинамическими характеристиками веществ, участвующих в реакции
Расчитываем энтальпийный эффект протекающих реакций
∆rH˚T,g=∆fH˚(пропан),g -∆fH˚(этилен),g -∆fH˚(метан),g
В нашем расчете проводим качественный термодинамический анализ протекающих превращений (по принципу Ле-Шателье)влияние параметров процесса на положение равновесия.
Определяем влияние температуры на константу реакции и
вычисляем равновесную степень конверсии как функцию температуры.
Термодинамические свойства в состоянии идеального газа:
Пропан:
| Т,К | ∆fH0т кДж/моль | S 0 Т Дж/моль*К | Ср,Дж/моль*К |
| -103,85 | -23,49 | 74,84 | |
| -110,184659 | 1,46825037 | 94,73 | |
| -115,410059 | 24,804603 | 114,43 | |
| -119,724909 | 47,0396284 | 129,48 | |
| -126,187709 | 88,0084324 | 155,34 | |
| -129,693509 | 124,89964 | 175,31 | |
| -130,4248869 | 139,919429 | 180,85752 | |
| -132,914259 | 202,167305 | 206,83 |
Этилен:
| Т,К | ∆fH0т кДж/моль | S 0 Т Дж/моль*К | Ср,Дж/моль*К |
| 52,3 | -23,4900 | 39,3400 | |
| 49,1933 | -5,7105 | 56,9200 | |
| 47,0497 | 7,7393 | 70,3200 | |
| 45,5413 | 17,7942 | 80,3600 | |
| 43,7281 | 32,0658 | 94,6000 | |
| 43,3817 | 42,9565 | 105,4800 | |
| 43,6280 | 45,6108 | 108,1341 | |
| 42,5438 | 58,0489 | 120,5600 |
Метан:
| Т,К | ∆fH0т кДж/моль | S 0 Т Дж/моль*К | Ср,Дж/моль*К |
| -74,8500 | -50,7200 | 35,6900 | |
| -77,9244 | -45,7731 | 40,6300 | |
| -80,7392 | -39,7636 | 46,6300 | |
| -83,2387 | -33,6459 | 52,7400 | |
| -87,1923 | -22,2701 | 64,0800 | |
| -89,6257 | -12,5841 | 73,7500 | |
| -90,2532 | -9,5724 | 76,7614 | |
| -90,8109 | 4,5596 | 90,8600 |
| Т,К | ∆rH,кДж/моль | ∆rS*T, Дж/моль*к | ∆G,Кжд/мольк | Kp | x1(общ) | x2(общ) |
| -15114,56 | 96414,56 | 0,961832521 | 0,700195 | -0,70019 | ||
| 81453,51 | -21180,75 | 102634,3 | 0,969609489 | 0,70163 | -0,70163 | |
| 81720,51 | -28414,44 | 110134,9 | 0,97385403 | 0,702408 | -0,70241 | |
| 82027,51 | -37734,77 | 119762,3 | 0,976277748 | 0,70285 | -0,70285 | |
| 82723,51 | -62570,16 | 145293,7 | 0,978392139 | 0,703235 | -0,70323 | |
| 83449,51 | -94527,25 | 177976,8 | 0,978820626 | 0,703313 | -0,70331 | |
| 83799,66 | -113022,6 | 196822,2 | 0,978476199 | 0,70325 | -0,70325 | |
| 110766,4 | -153514,6 | 0,971515847 | 0,70198 | -0,70198 |
График зависимости Константы равновесия от температуры.
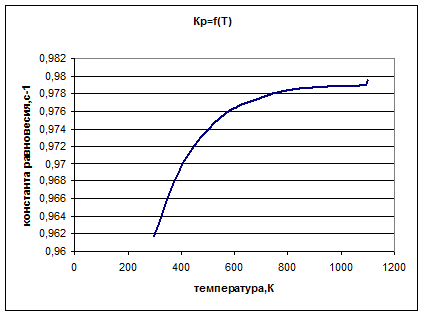
График показывает, что при увеличении температуры происходит увеличение константы равновесия.
| компонент | Количество моль | ||
| исх см | равн см | мольн доля в равн | |
| пропан | 1-X-У | (1-X-У)/(1+n) | |
| метан | У | У/(1+n) | |
| этилен | X | X/(1+n) | |
| ин р | n | n | n/(1+n) |
| Σ | 1+n | 1+n |
Где Х-количество моль этилена полученного по реакции.
У - Количество моль метана полученного по реакции.
n- Количество моль инертного разбавителя.
| PA= | (1-X-У)/(1+n) |
| PB= | У/(1+n) |
| PC= | X/(1+n) |
| Kp= | (PB*PC)/PA |
| Pобщ= | 1 атм |
| n= | 0 моль |
Расчет равновесной степени конверсии и константы реакции при варьировании давления и фиксированных прочих параметров процесса.
| T,К | Pобщю,атм | n,моль | Kp,с-1 | X |
| 0,978476 | 0,77754585 | |||
| 0,496119743 | ||||
| 0,37998278 | ||||
| 0,282992099 | ||||
| 0,186566035 | ||||
| 0,171300271 | ||||
| 0,159295615 |
График зависимости равновесная степени конверсии от давления.

Таким образом, при увеличении общего давления уменьшается равновесная степень конверсии
Расчет константы реакции и степени конверсии при изменении количества молей инертного разбавителя.
| T,К | Pобщ.,атм | n,моль | Kp,с-1 | X |
| 0,978476 | 0,496119743 | |||
| 0,555907123 | ||||
| 0,634685379 | ||||
| 0,662941947 | ||||
| 0,724314069 | ||||
| 0,753290717 | ||||
| 0,803613539 | ||||
| 0,836322822 |
График зависимости степени конверсии от инертного разбавителя.
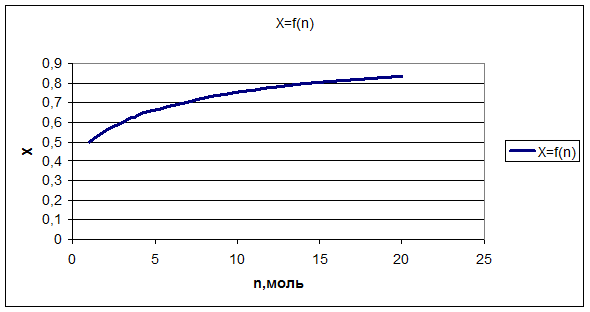
Как показывает график зависимости равновесной степени конверсии от количества инертного разбавителя, что при дальнейшем разбавлении степень конверсии увеличивается.
Расчет степени конверсии и константы равновесия при варьировании температуры.
| T,К | Pобщ.,атм | n,моль | Kp,с-1 | x |
| 0,961832521 | 0,509727507 | |||
| 0,969609489 | 0,507714857 | |||
| 0,97385403 | 0,506623076 | |||
| 0,976277748 | 0,50600175 | |||
| 0,978392139 | 0,505460965 | |||
| 0,978820626 | 0,505351514 | |||
| 0,978476199 | 0,50543949 | |||
| 0,97931562 | 0,505325134 |
График зависимости степени конверсии от температуры.

Как показывает график, увеличение температуры ведёт к снижению степени конверсии этилена.
Вывод: Таким образом, на процесс пиролиза пропана влияют следующие параметры: инертный разбавитель, давление, температура.
|
|
|
|
|
Дата добавления: 2015-06-26; Просмотров: 2077; Нарушение авторских прав?; Мы поможем в написании вашей работы!