
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диссоциация воды. Водородный показатель
|
|
|
|
Вода служит не только наиболее распространенным растворителем для многих веществ, но и сама является очень слабым амфотерным электролитом:
Н2О ↔ H+ + ОH-; ∆Н°298 = 56 кДж /моль,
в воде присутствуют катионы водорода и гидроксид - анионы в строго эквивалентных количествах. Константа ионизации воды (Кu)
Ku = [H][OH-]/[H2O],
определена по электрической проводимости и равна 1,8∙10-16 при 22 °С. Так как вода - очень слабый электролит, то концентрация недиссоциированных молекул может быть принята
равной общему числу молей в 1 дм3 воды, то есть: [Н2О] = 1000/18 = 55,56 моль/дм3.
Тогда Ки [Н20] = [H+] [ОН-] или [H+][ОН-] = 1,8∙10-16 ∙55,56 = 10-14 = Кw
Величина [Н+ ][ОН-] = 10-14 называется ионным произведением воды. Так как в воде концентрации гидратированных ионов равны, то
____
[H+]= [ОH-] = √10-14 = 10-7 моль/дм3
При добавлении кислоты концентрация ионов водорода увеличивается и соответственно уменьшается концентрация гидроксид – ионов, поскольку при данной температуре ионное произведение воды – величина постоянная. При добавлении щелочи наблюдается обратная зависимость. Таким образом, концентрация ионов водорода в растворе может служить мерой кислотности или щелочности среды. В кислых растворах [Н+]>10-7, в щелочных [Н+]<10-7.
В 1909 г. Сёренсен ввел значение отрицательного десятичного логарифма концентрации водородных ионов, которое называют водородным показателем рН
рН= - lg[H+].
Тогда для нейтральной среды рН = - lg10-7 = 7, для кислых растворов рН < 7, а для щелочных рН > 7. Аналогичным образом реакция среды может быть охарактеризована так называемым гидроксильным показателем рОН
рОН = -lg[OH-].
Для воды рН = рОН = 7, а изменение рОН в кислых и щелочных растворах противоположно изменению рН. Прологарифмировав ионное произведение воды, получим
lg[H+] + lg[OH-] = -14.
Заменив отрицательные логарифмы, получим соотношение
рН + рОН = 14.
Наглядно зависимость между концентрацией ионов водорода, значением рН и реакцией раствора можно выразить схемой:
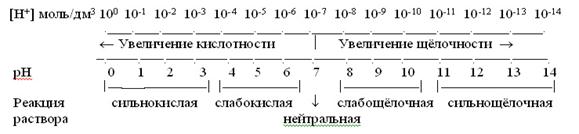
Из схемы видно, что чем меньше рН, тем больше концентрация ионов Н+, т.е. тем выше кислотность среды; и наоборот, чем больше рН, тем меньше концентрация ионов Н+, т.е. тем выше щелочность среды. Исключительно важна роль реакции среды в самых различных явлениях и процессах, как в природе, так и в медицинской практике. Многие процессы, протекающие в живых организмах, требуют определенной реакции среды.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 1023; Нарушение авторских прав?; Мы поможем в написании вашей работы!