
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Почвенная коррозия. Катодная, протекторная защита
|
|
|
|
Лекция 6.
Почвенная коррозия является наиболее распространенным видом электрохимической коррозии, оказывающей воздействие на подземные металлические сооружения. Почвы и грунты чрезвычайно разнообразны не только в пределах больших регионов, но даже и в пределах одного небольшого участка. Между почвой, самым поверхностным слоем земли, и грунтом четкой границы нет.
На коррозионную характеристику грунтов и почв, как почвенно–грунтового электролита большое влияние оказывает ее структура, от которой зависит содержание влаги и газов в почве.
Влажность оказывает большое влияние на коррозионную активность почвы и грунта. В воздухопроницаемых почвах и грунтах скорость коррозии стали максимальна при содержании влаги 30 – 50% их влагоемкости.
При дальнейшем повышении влажности скорость коррозии снижается и становится равномерной. Такое явление можно объяснить условием протекания анодной и катодной реакций на стальной поверхности, находящейся в контакте с капиллярно – пористой средой, каковой является грунт.
Процесс анодного растворения железа во влажных грунтах начинается с перехода в почвенный электролит ион–атома металла, несущего положительный заряд. В дальнейшем происходит гидратирование ион– атома полярными молекулами воды и превращение его в нейтральную частицу. При недостатке полярных молекул воды происходит накапливание положительных ион–атомов в приэлектродном слое, т.е. сдвиг потенциала в положительную сторону (анодная поляризация).
На поверхности металлических изделий, находящихся в контакте с почвенным электролитом, вследствие местных неоднородностей состава металла или электролита возникает большое количество коррозионных элементов, природа которых аналогична природе гальванических элементов. При этом коррозионному разрушению подвергаются анодные участки, имеющие более отрицательный электрохимический потенциал по сравнению с близрасположенными катодными участками, имеющими более положительный потенциал.
Электрохимическая коррозия-результат работы гальванических элементов. Она происходит следующим образом: на анодных участках протекает реакция окисления с образованием ионов металла Fe2+, а на катодных участках под влиянием кислорода образуется гидроокись. Ионы Fe2+ и OH- направляются друг к другу и образуют нерастворимый осадок Fe(OH)2 который может разлагаться на окись железа и воду (Fe(OH)2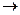 Fe2O3+H2O). Высвобождающиеся при реакции окисления электроны от анодного участка по металлу изделия перетекают к катодному участку и участвуют в реакции восстановления.
Fe2O3+H2O). Высвобождающиеся при реакции окисления электроны от анодного участка по металлу изделия перетекают к катодному участку и участвуют в реакции восстановления.
Основными условиями возникновения почвенной коррозии металлов являются:
- наличие разности потенциалов двух разноименных металлических изделий или их деталей, а также отдельных участков поверхности одного и того же металла;
- наличие контакта двух металлов или двух участков металла с электролитом;
- соединение анода и катода металлическим проводником, которым является металл сооружения, если на его поверхности возникли анодные и катодные участки;
- наличие в электролите диссоциированных ионов.
Такие условия всегда наблюдаются на поверхности любого металла, находящегося в контакте с почвенным электролитом.
Коррозионная активность грунта, характеризуется показателем удельного электрического сопротивления почвы.
Под удельным электрическим сопротивлением почвы принято понимать сопротивление протеканию электрического тока в условном почвенном проводнике площадью поперечного сечения 1м2 и длиной 1м (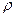 ,Ом
,Ом 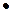 м2).
м2).
Удельное электрическое сопротивление почвы находится в зависимости от её влажности и содержания водорастворимых солей в почвенном электролите. Практически удельное электрическое сопротивление почвы изменяется в широких пределах (от десятых долей до тысяч омметров).
Между удельным электрическим сопротивлением почвы и опасностью коррозии существует прямая зависимость: чем меньше 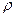 , тем больше возможность коррозии.
, тем больше возможность коррозии.
Для предотвращения разрушения оборудования и, в частности, трубопроводов применяют защиту.
Катодная защита заключается в создании отрицательного потенциала на поверхности трубопровода, благодаря чему предотвращается возможность выхода электрического тока из трубы, сопровождаемое её коррозионным разъеданием.
С этой целью трубопровод превращают в катод путем подключения трубопровода к отрицательному полюсу постороннего источника постоянного тока, положительный полюс которого (анод) присоединяют к специальному электроду-заземлителю, установленному в стороне от трассы трубопровода. В результате достигается, так называемая катодная поляризация, при которой токи входят из грунта в трубу, так как она является в данном случае катодом по отношению к грунту. Под воздействием электрического поля источника начинается движение свободных валентных электронов в направлении- анодное заземление-источник тока-защищаемое сооружение.
В результате вместо трубопровода разрушается анодный заземлитель.
Принципиальная схема катодной защиты и механизм действия представленый на рисунке 2 и 3
1-вдольтрассовая ЛЭП;
2- трансформаторный пункт;
3-станция катодной защиты;
4-защищаемый трубопровод;
5-анодное заземление;
6-кабель.
Протекторная защита имеет те же основы, что и катодная защита. Разница заключается лишь в том, что необходимый для защиты ток создается крупным гальваническим элементом, в котором роль катода играет металлическая поверхность сооружения, а роль анода -более электроотрицательный металл.
Принципиальная схема протекторной защиты представлена на рисунке 4.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 1565; Нарушение авторских прав?; Мы поможем в написании вашей работы!