
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Первое начало термодинамики. Первое начало термодинамики представляет собой по сути обобщенный закон сохранения энергии
|
|
|
|
Первое начало термодинамики представляет собой по сути обобщенный закон сохранения энергии.
Этот закон содержит три величины: внутреннюю энергию U, работу А и теплоту Q. Внутренняя энергия. Внутренней энергией U макросистемы называют величину, состоящую из:
суммарной кинетической энергии хаотического движения молекул (в этой системе отсчета суммарный импульс всех молекул равен нулю, и система как целое покоится);
собственной потенциальной энергии взаимодействия всех молекул;
внутренней энергии самих молекул, атомов, ядер.
Внутренняя энергия U является функцией состояния и не зависит от того, каким путем мы привели систему в данное состояние. При изменении состояния приращение внутренней энергии определяется только конечным и начальным состояниями ж не зависит от процесса, который перевел систему из одного состояния в другое.
 Внутренняя энергия является величиной аддитивной.
Внутренняя энергия является величиной аддитивной.
Работа и количество тепла. Внутреннюю энергию макросистемы можно изменить, совершив над системой работу А' внешними макроскопическими силами, либо путем теплопередачи.
Совершение работы сопровождается перемещением внешних тел, действующих на систему (так, например, ведет себя поршень в цилиндре с газом).
Первое начало термодинамики утверждает, что приращение внутренней энергии макросистемы при ее переходе из начального состояния 1 в конечное 2 равно сумме совершенной над системой работы А' всех внешних сил и количества переданного системе тепла Q:
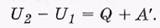
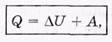 Обычно рассматривают не работу А' над системой, а работу А, производимую самой системой над внешними телами. Имея в виду, что А' = -А, перепишем выражение в виде
Обычно рассматривают не работу А' над системой, а работу А, производимую самой системой над внешними телами. Имея в виду, что А' = -А, перепишем выражение в виде
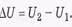 где
где
Это уравнение и выражает первое начало тер-модинамики: количество теплоты Q, сообщенное макросистеме, идет на приращение 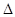 U её внутренней энергии и на совершение системой работы А над внешними телами.
U её внутренней энергии и на совершение системой работы А над внешними телами.
Все величины являются алгебраическими, т.е. могут иметь как положительные, так и отрицательные знаки. Если Q < О, то это значит, что тепло отводится от системы, если А < 0, то работа производится над системой. Приращение 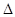 U внутренней энергии может иметь любой знак, в частности быть равной нулю.
U внутренней энергии может иметь любой знак, в частности быть равной нулю.
Первое начало термодинамики в дифференциальной форме имеет вид
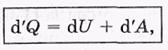
где штрих означает, что мы имеем дело не с приращением какой-либо функции, а с элементарными значениями теплоты (d'Q) и работы (d'A).
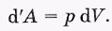 Работа, совершаемая макросистемой. Если объем макросистемы (например, газа) получает приращение dV, а давление, оказываемое ею на соседние тела (стенки), равно р, то элементарная работа сил, действующих со стороны газа на стенки,
Работа, совершаемая макросистемой. Если объем макросистемы (например, газа) получает приращение dV, а давление, оказываемое ею на соседние тела (стенки), равно р, то элементарная работа сил, действующих со стороны газа на стенки,
Работа, совершаемая газом при конечных изме-  нениях объема, например от V1 до V2, должна быть представлена в виде интеграла:
нениях объема, например от V1 до V2, должна быть представлена в виде интеграла:
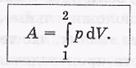
Работа А зависит от процесса (или «пути»), по которому система переводится из состояния 1 в 2.
На рисунке изображен процесс изменения объема
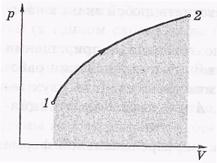
на диаграмме p-V. Геометрическая интерпретация интеграла — это «площадь» под кривой 1-2, а эта площадь зависит от вида кривой, т. е. от процесса.Если в результате изменений макро-система возвращается в исходное состояние, то говорят, что она совершила круговой процесс или цикл. На диаграмме p-V такой процесс имеет вид замкнутой кривой, представленной на рисунке.
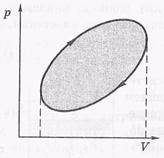
Работа, совершаемая системой за цикл, численно равна площади внутри цикла, тонированной на рисунке. При этом, если точка, изображающая состояние системы, описывает цикл по часовой стрелке (как на рисунке), то работа системы А > 0. Если же против часовой стрелки, то А < 0.Знак работы зависит от знака dV:
на тех участках процесса, где dV > 0,работа А > 0, на тех же участках, где dV < 0, и А < 0.
Запишем первое начало термодинамики, в виде
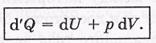
В такой форме этот закон использовать наиболее удобно для решения ряда вопросов.
Рассмотрим важные следствия, вытекающие из первого начала. В качестве объекта исследования возьмем идеальный газ, уравнение состояния которого имеет наиболее простой вид.
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 713; Нарушение авторских прав?; Мы поможем в написании вашей работы!