
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Зонна теорія електропровідності. Опір провідника у квантовій теорії
|
|
|
|
Електричні властивості кристалічних твердих тіл визначаються будовою їх кристалічної ґратки і характером сил, які діють між частинками твердого тіла, тобто типом хімічного зв'язку.
В залежності від того, які частинки перебувають у вузлах кристалічної ґратки та яка природа сил взаємодії між ними, розрізняють такі основні типи кристалів: іонні, атомні, металічні та молекулярні.
У вузлах ґратки іонних кристалів розміщуються іони різних знаків, сили взаємодії між якими переважно є електростатичними. Прикладом є гратка кам'яної солі NaCl, при створенні якої натрій віддає свій єдиний валентний електрон хлорові, якому не вистачає одного електрона для заповнення валентної оболонки (рис. 1).
| +Na |
| -Cl |
| + |
| + |
Рис 1 Рис. 2
Внаслідок цього обидва атоми стають іонами протилежних знаків та набувають стійких зовнішніх оболонок. Відсутність вільних носіїв заряду пояснює низьку електропровідність іонних кристалів.
У більшості випадків такі кристали є ізоляторами.
У вузлах ґратки атомних кристалів розташовані нейтральні атоми, зв'язок між якими здійснюється шляхом створення спільної пари валентних електронів (по одному електрону від кожного атома) і називається ковалентним. Такий зв'язок має місце, наприклад, між атомами в молекулі водню. При зближенні двох атомів водню траєкторії їхніх електронів перекриваються (рис. 2).
В області перекриття електрони перебувають під дією сильного притягання з боку обох ядер і починають рухатись по складним орбітам навколо обох ядер, тобто атоми виявляються зв'язаними спільною парою електронів.
При цьому виникає так звана обмінна взаємодія, вона лежить в основі ковалентного зв'язку і має квантову природу. Не зважаючи на те, що енергія зв'язку в атомних кристалах є значною, в багатьох з них можливе вивільнення електронів з ковалентних зв'язків. Під дією електричного поля вивільнені електрони стають носіями струму. Чим вища температура кристалу, тим більше виникає електронів провідності. Багато з таких кристалів (елементи з середньої групи таблиці Менделєєва, наприклад, германій та кремній і різні сполуки) є напівпровідниками.
У вузлах гратки металічних кристалів розташовані позитивні іони, між якими рухаються електрони. Вони створюють так званий електронний газ, який рівномірно заповнює простір між іонами. Цей тип гратки характерний для елементів (металів), у яких валентні електрони слабко зв'язані з ядром. При виникненні кристалічної гратки ці електрони легко відокремлюються від атомів і стають спільними для всього кристала.
Електронний газ зв'язує в міцну систему позитивно заряджені іони кристалу. Під впливом сил притягання з боку електронного газу і сил відштовхування між іонами останні розташовуються на деякій рівноважній відстані один від одного. Ця відстань відповідає мінімуму енергії в кристалі. Тіла з такою кристалічною граткою відзначаються високою електропровідністю, оскільки навіть слабке електричне поле викликає переміщення вільних електронів. При підвищені температури кристалу збільшується інтенсивність теплового коливального руху іонів, що затруднює напрямлений рух електронів в електричному полі.
У вузлах ґратки молекулярних кристалів знаходяться нейтральні молекули. Вони утримуються вандерваальсівськими силами, природа яких визначається взаємодією молекулярних диполів. За звичайних умов такі кристали електропровідністю не володіють і при підвищенні температури легко руйнуються. Молекулярну кристалічну гратку мають більшість органічних сполук.
Згідно з квантовою теорією енергія електронів в атомах квантується, тобто може приймати лише дискретні значення. Ці значення енергії відповідають енергетичним рівням. Якщо однакові атоми ізольовані один від одного, то вони мають однакові енергетичні рівні. При виникненні кристала відбувається зміна енергетичних рівнів у зв'язку із взаємодією атомів між собою. Якщо кристал складається з N атомів, то замість одного однакового для всіх атомів рівня виникає N дуже близьких за значеннями енергії рівнів, які не співпадають між собою. Так відбувається розщеплення енергетичного рівня на низку енергетичних рівнів.
Сукупність цих рівнів називається зоною енергетичних рівнів. Розщеплення енергетичних рівнів і виникнення зони енергетичних рівнів, яке має місце при зближенні атомів і виникненні кристала, здійснюється згідно з принципом Паулі, за яким на одному енергетичному рівні може перебувати не більше двох електронів з різною орієнтацією спінів.
Сукупність значень енергій, які можуть мати електрони в даному атомі (зони дозволених енергій) чергуються зі значеннями енергій, які електрони в даному атомі мати не можуть (зони заборонених енергій).
Ступінь розщеплення для різних рівнів неоднаковий. Рівні, заповнені близькими до ядра внутрішніми електронами, розщеплюються незначно, оскільки ці електрони слабко взаємодіють з електронами і ядрами інших атомів кристала. Така взаємодія є значною для валентних електронів, внаслідок чого їхні рівні розщеплюються сильніше, утворюючи так звану валентну зону. Ще помітнішим є розщеплення більш високих, ніж валентні, енергетичних рівнів, не зайнятих електронами в основному стані атома.
У кристалів різних типів ступінь заповнення валентної зони електронами різний, тому енергетичні зони розташовані по-різному, чим пояснюється різна за величиною їхня електропровідність.
При абсолютному нулі температури енергія кристала мінімальна, що відповідає заповненню електронами валентної зони, починаючи з найбільш низьких її рівнів. При підвищенні температури енергія теплового руху електронів зростає і вони стають здатними займати більш високі енергетичні рівні.
Класична теорія провідності металів грунтується на тому, що вільні електрони (електронний газ) поводять себе так, як молекули ідеального газу. Вони рухаються зі швидкістю 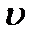 , співударяються переважно зіонами гратки, пробігаючи між зіткненнями відстань
, співударяються переважно зіонами гратки, пробігаючи між зіткненнями відстань 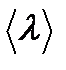 , яка називається середньою довжиною вільного пробігу і дорівнює значенню міжатомної відстані в кристалі. На основі цих уявлень, можна отримати наступний вираз для питомої електропровідності металів:
, яка називається середньою довжиною вільного пробігу і дорівнює значенню міжатомної відстані в кристалі. На основі цих уявлень, можна отримати наступний вираз для питомої електропровідності металів:
 , n - концентрація електронів, е - заряд електрона, m - маса електрона.
, n - концентрація електронів, е - заряд електрона, m - маса електрона.
В цьому виразі величини n, m, е, λ - сталі, а  прямопропорційна до
прямопропорційна до  , де Т - температура. Таким чином, за класичною теорією питома електропровідність залежить від природи металу і обернено пропорційна
, де Т - температура. Таким чином, за класичною теорією питома електропровідність залежить від природи металу і обернено пропорційна  . Однак, досліди показують, що в широкому інтервалі температур опір металів прямопропорційний до Т.
. Однак, досліди показують, що в широкому інтервалі температур опір металів прямопропорційний до Т.
| Т |
| R |
| Тк |
 , де R і R0 - опір при температурах t°С і 0° С відповідно, α - температурний коефіцієнт опору (ТКО), який визначається експериментально.
, де R і R0 - опір при температурах t°С і 0° С відповідно, α - температурний коефіцієнт опору (ТКО), який визначається експериментально.
За величиною ТКО:
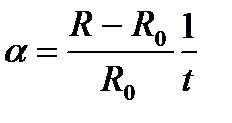 , тобто фізичний зміст ТКО полягає у відносній зміну кожної початкової одиниці опору при зміні температури на один градус. Вимірюється ТКО в град-1.
, тобто фізичний зміст ТКО полягає у відносній зміну кожної початкової одиниці опору при зміні температури на один градус. Вимірюється ТКО в град-1.
За низьких температур для багатьох металів залежність R = f(T) має інший характер (рис. 3).
Тобто при певній для даного металу низькій температурі Тк, яка називається критичною, опір падає практично до нуля. Це явище називається надпровідністю, в межах класичної теорії воно не пояснюється.
Причиною розходжень результатів класичної теорії з експериментальними фактами є те, що в цій теорії не враховуються квантові властивості електронів.
Явище надпровідності пояснюється обмінною взаємодією між електронами і має квантову природу.
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 765; Нарушение авторских прав?; Мы поможем в написании вашей работы!