
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гибель клеток
|
|
|
|
Наряду с описанными выше делением, сортировкой и миграцией клеток, важную роль в индивидуальном развитии организмов играет процесс программированной гибели клеток, или апоптоза. В эмбриогенезе он является одним из основных механизмов органогенеза и метаморфоза, способствует достижению характерных для определенного биологического вида черт его морфофункциональной организации. В постнатальном развитии апоптоз обеспечивает гибель клеток на терминальных стадиях дифференцировки (например, эритроцитов), стареющих и поврежденных клеток, уничтожение аутореактивных, т.е. действующих против собственных клеток, клонов лимфоцитов и т.д. Помимо этого на протяжении всего развития механизм программированной клеточной гибели обеспечивает регуляцию численности клеток, а именно - установление нужного равновесия между процессами пролиферации и гибели клеток, что в одних ситуациях обеспечивает стабильное состояние организма, в других - рост, в-третьих - атрофию тканей и органов.
В настоящее время различают два принципиально различных типа клеточной гибели: апоптоз (в переводе с греческого «отпадающий») и некроз (см. п. 3.1.2).
Некроз представляет собой патологическую форму смерти клеток в результате их острого повреждения. Он характеризуется разрывом ци-топлазматической и внутриклеточных мембран, что приводит к разрушению органелл, высвобождению лизосомальных ферментов и выходу содержимого цитоплазмы в межклеточное пространство, при этом часто развивается воспалительный процесс, захватывающий территорию от части клетки до целого органа (см. рис. 3.5).
В отличие от некроза, апоптоз - генетически контролируемая клеточная гибель, которая приводит к «аккуратной» разборке и удалению клеток. Он широко распространен и типичен для физиологических условий. В процессе апоптоза наблюдаются следующие морфологические изменения (см. рис. 3.5). Клетка уменьшается в размерах, цитоплазма уплотняется, органеллы располагаются более компактно. Происходит конденсация хроматина под мембраной ядра, при этом образуются четко очерченные плотные массы различной формы и размеров. Ядро может разрываться на два или несколько фрагментов. Затем в апоптоти-ческой клетке формируются глубокие впячивания мембраны, что приводит к фрагментации клетки и формированию окруженных мембраной апоптотических телец, состоящих из цитоплазмы и плотно расположенных органелл, с фрагментами ядра или без них. После чего очень быстро происходит их фагоцитоз, который осуществляется как макрофагами, так и окружающими здоровыми клетками. Очень важно, что при апоптозе не развивается воспалительный процесс и гибель отдельных клеток или их групп происходит избирательно, без повреждения окружающих здоровых клеток.
Выделяют два вида программированной клеточной гибели: апоптоз «изнутри» и апоптоз «по команде».
В первом случае задача процесса - убрать поврежденные клетки. Апоптоз запускается сигналами, возникающими внутри самой клетки при неудовлетворительном ее состоянии - повреждении хромосом, внутриклеточных мембран и т.д.
Второй вариант апоптоза наблюдается во вполне нормальных и жизнеспособных клетках, которые с позиции целого организма оказываются ненужными или вредными. В этом случае клетка получает из внеклеточной среды, например от окружающих клеток, сигнал «погибнуть», который передается через мембранные или, реже, цитоплазма-тические рецепторы. Иногда сигналом для начала апоптоза может быть и отсутствие необходимого сигнала. В результате контакта сигнальных молекул с наружной частью белка-рецептора последний претерпевает структурные изменения, что тем или иным способом приводит к запуску реакций клеточной гибели.
Механизмы апоптоза многообразны. Они представляют собой сложнейшие молекулярные каскады, изучением которых занимаются многие лаборатории по всему миру. Остановимся на роли некоторых основных участников этих каскадов.
Реализуемые в организме схемы осуществления апоптоза различаются в основном своими начальными стадиями (рис. 8.18). Большинство из них осуществляется с участием белка р53 и лишь небольшая часть, например запускаемая с рецепторов ФНО, реализуется без его участия (см. п. 3.1.2).
Какими бы сигналами ни запускалась программируемая клеточная гибель - разнообразными внешними или внутренними, - если в схеме принимает участие белок р53, то происходит его накопление и увеличение активности.
Белок p53 в норме присутствует во всех типах клеток. Он локализуется в ядре, где функционирует как транскрипционный фактор. В его молекуле у человека - 392 аминокислотных остатка, образующих шесть различных по размеру и функции доменов (блоков).
Центральный и самый большой домен (включающий около 200 остатков) отвечает за узнавание энхансеров генов-мишеней и связывание с ними. В результате изменяется активность нескольких групп генов и среди них - генов, продукты которых принимают участие в реализации апоптоза. К последним относятся гены, кодирующие белки, стабилизирующие мембраны митохондрий (BCL2, BCLK и др.) и наоборот, повышающие их проницаемость (например, ВАХ, ВАD, BAK). Изменение соотношения этих белков в цитоплазме клетки вызывает повышение проницаемости мембран митохондрий, вследствие чего ее покидают белки, активирующие каспазный каскад через каспазу 9 (Aif, Цит C). Включение апоптозного пути через рецепторы без вовлечения белка р53 активирует этот же каскад, но через каспазу 8.
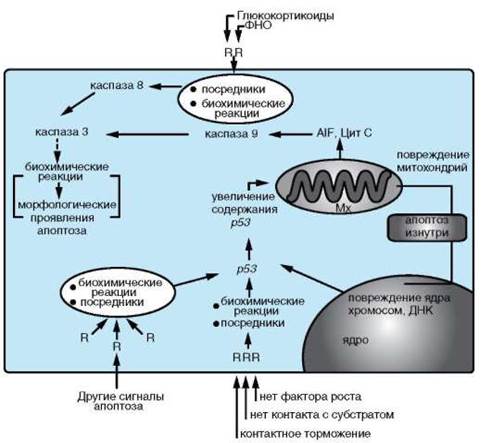
Рис. 8.18. Обобщающая схема некоторых механизмов апоптоза: R - рецептор; ФНО - фактор некроза опухолей
Каспазы - семейство белков, являющихся непосредственными участниками внутриклеточных реакций, обеспечивающих апоптоз. Кас-пазы представляют собой ферменты - сериновые или цистеиновые ци-топлазматические протеазы, в зависимости от наличия в их активном центре соответствующей аминокислоты. В своих белках-мишенях каспазы разрывают те пептидные связи, которые образованы с участием остатка аспарагиновой кислоты. Считают, что эти ферменты находятся в цитоплазме практически всех клеток, и до инициации реакций клеточной гибели они присутствуют в виде неактивных предшественников - прокаспаз. Последние активируются путем ряда модификаций. Известно 14 каспаз, которые подразделяются на инициаторы, эффекторы и стимуляторы. Каспазы способны в определенной последовательности активировать друг друга, образуя своего рода каскад, причем разветвленный. Инициаторы (каспаза 8 и 9) расщепляют и активируют каспазы-эффекторы. Одна из них - узловое звено каспазного каскада - каспаза 3. Ее мишени - как другие участники этого каскада, так и, возможно, некаспазные белки. Функция завершающих членов каскада - ограниченный протеолиз (разрушение) некоторых цитоплазматических и ядерных белков, что и приводит к развитию морфологических проявлений апоптоза.
В эмбриональном периоде развития основным видом программированной клеточной гибели является апоптоз «по команде».
Особое значение этот клеточный механизм имеет для многих формообразовательных процессов. Так, разделение пальцев на руках или ногах зародыша, разделение локтевой и лучевой костей предплечья, формирование суставов основано на гибели клеток, которая осуществляется избирательно, в определенных участках зачатков конечностей (рис. 8.19). Образование полостей сосудов (кавитация), которые первоначально представляют собой тяжи клеток, разделение верхнего и нижнего век и многие другие процессы развития имеют в своей основе механизм избирательной клеточной гибели.
Апоптоз обеспечивает также и исчезновения органов. Таким образом происходит резорбция личиночных органов животных при метаморфозе, например жаберных лепестков, хвоста и кишечника у головастиков.
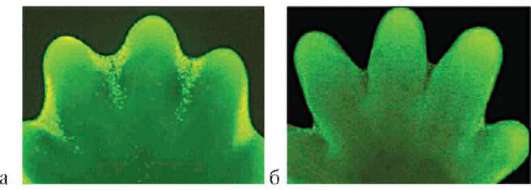
Рис. 8.19. Апоптоз во время нормального развития конечности мыши: а - клетки, подвергающиеся апоптозу, мечены желтым; б - та же конечность через 1 сут
Подобные примеры имеют место и в эмбриональном развитии человека. Как и у других млекопитающих, у человека закладываются 9-10 хвостовых позвонков, волосяной покров, шесть или семь зачатков пальцев. Наблюдаемая в последующем развитии гибель клеток в этих закладках приводит к тому, что в копчике остается 4-5 позвонков, редуцируется большинство волосяных зачатков, а конечности становятся пятипалыми. В ходе развития мочеполовой системы погибают клетки предпочки и туловищной почки, в центральной нервной системе происходит гибель части нейронов, что в большинстве случаев обусловлено отсутствием контакта с клетками-мишенями.
Нарушение механизма программированной клеточной гибели приводит к формированию аномалий развития, таких как синдактилия (сращение пальцев), гипертрихоз (повышенное оволосение), полидактилия (многопалость) (рис. 8.20).
Как уже было сказано, процесс апоптоза требует скоординированной регуляции экспрессии многих генов. Нарушения синтеза белковых продуктов любого из них влекут за собой сбои в развитии и функционировании различных клеточных популяций. Так, к настоящему времени установлено, что активность гена белка bcl-2 требуется для поддержания жизнеспособности лимфоцитов, меланоцитов, эпителия кишечника и клеток почек во время развития эмбриона. Продукт гена bcl-x необходим для ингибирования смерти клеток в эмбриогенезе, особенно в нервной системе. Экспрессия гена Bax требуется для апоптоза тимоцитов и поддержания жизнеспособности мужских половых клеток в ходе гаметогенеза. Как в раннем, так и в постнатальном развитии механизм клеточной гибели используется организмом для предотвращения несанкционированной пролиферации поврежденных или патологически измененных клеток. Мутации гена p53 обнаруживаются примерно в половине опухолей, независимо от их происхождения или типа. Мыши, у которых отсутствовали оба этих гена, проявляли чрезвычайно высокую склонность к развитию злокачественных образований в результате полного или частичного нарушения апоптоза предопухолевых клеток.
Таким образом, программированная клеточная гибель является естественным, эволюционно обусловленным и генетически контролируемым механизмом развития, активно реализуемым организмом на различных стадиях онтогенеза для решения широкого спектра задач.
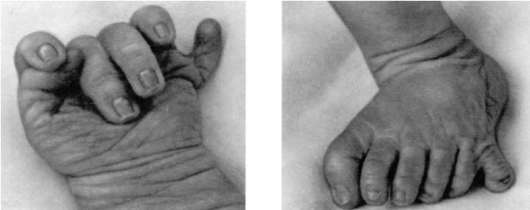
Рис. 8.20. Полидактилия кисти и стопы
|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 1405; Нарушение авторских прав?; Мы поможем в написании вашей работы!