
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Биологическая роль
|
|
|
|
Углеводы
Углеводы – это соединения, структура которых выражается общей формулой 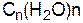 , где n больше или равно 4.
, где n больше или равно 4.
Углеводы широко распространены как в растительном, так и в животном мире. До 90% сухого вещества растений приходится на углеводы, в животных организмах – около 2% сухого вещества.
В растениях углеводы образуются в результате фотосинтеза из диоксида углерода и воды с участием солнечной энергии и хлорофилла:
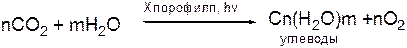
Животные не способны сами синтезировать углеводы и используют углеводы, синтезируемые растениями.
Классификация углеводов
Углеводы в зависимости от строения, величины молекул и физических, химических свойств подразделяются на моносахариды, олигосахариды и полисахариды, расщепляющиеся при гидролизе на моносахариды.
Моносахариды (монозы)
Моносахариды – соединения, в основе которых лежит неразветвленная углеродная цепь, при одном из атомов углерода которой находится карбонильная группа, а при всех остальных – по одной гидроксигруппе.
Моносахариды обычно имеют названия с суффиксом – оза, например, глюкоза, фруктоза, рибоза и т. д.
Обычно моносахаридами называют соединения с длиной углеродной цепи не менее трех атомов. В зависимости от числа углеродных атомов в молекуле различают триозы (n=3), тетрозы (n=4), пентозы (n=5) и т. д. В зависимости от того, входит в состав моносахарида альдегидная или кетогруппа, их разделяют на альдозы и кетозы.
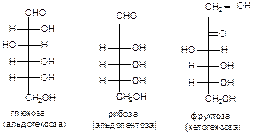
Для изображения строения моносахаридов используют проекционные формулы Фишера. В формулах Фишера цепь углеродных атомов располагается в одну линию. Нумерация цепи начинается с атома углерода альдегидной группы или с крайнего атома углерода, к которому ближе располагается кетогруппа.
Циклические формулы принято изображать формулами Хеуорса.
Для перехода от формул Фишера к формулам Хеуорса нужно знать следующие правила:
1. Изобразить цикл в виде плоского многоугольника. Нумерацию атомов углерода в цикле производить по часовой стрелке.
2. Атомы и группы атомов, которые в формуле Фишера находятся справа от цепи, в формуле Хеуорса располагаются под плоскостью цикла, и наоборот.
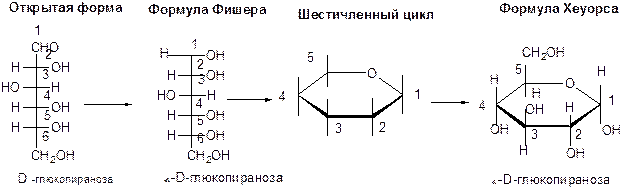
Направление оптического вращения обозначают знаками плюс и минус, а буквами D и L обозначают принадлежность данного моносахарида к D- или L-ряду.
физические свойства
Моносахариды – кристаллические бесцветные вещества. Имеют сладкий вкус. Хорошо растворимы в воде и Нерастворимы в эфире, плохо растворимые в спирте.
химические свойства
1. Мутаротация.
В водных растворах монозы существуют в виде оксо-циклотаутомеров. Реакция сопровождается появлением a- и b- аномеров.
Кристаллические формы 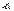 -и b-глюкозы вполне устойчивы, но в растворе каждая из них медленно превращается в равновесную смесь обеих форм. За этим процессом легко проследить по уменьшению оптического вращения a-аномера (+112 градусов) или по возрастанию оптического вращения b-аномера (+18,7 градусов) до равновесного значения, составляющего 52,5 градусов.
-и b-глюкозы вполне устойчивы, но в растворе каждая из них медленно превращается в равновесную смесь обеих форм. За этим процессом легко проследить по уменьшению оптического вращения a-аномера (+112 градусов) или по возрастанию оптического вращения b-аномера (+18,7 градусов) до равновесного значения, составляющего 52,5 градусов.
Из этого следует, что процесс изменения оптического вращения при установлении равновесия называется мутаротацией.
Это явление обычно наблюдается для восстанавливающих сахаров (т. е. таких, в которых карбонильная функция существует в форме полуацеталя).
Мутаротация катализируется кислотами и солями. В твердом состоянии монозы находятся исключительно в циклической форме.
2. Эпимеризация.
Называется также перегруппировкой Лобри-де-Брюина – Ван-Экейнштейна. Протекает при обработке моноз слабыми (меньше 1 %) растворами щелочей. В ходе перегруппировки возникает промежуточное соединение – ендиол
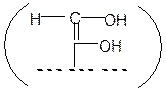 .
.
Превращения ендиола могут привести к образованию кетозы или к двум альдозам, различающимся только конфигурацией атома 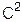 . Так из D-глюкозы при обработке слабощелочными растворами образуется смесь D-глюкозы, D- маннозы и D-фруктозы.
. Так из D-глюкозы при обработке слабощелочными растворами образуется смесь D-глюкозы, D- маннозы и D-фруктозы.
Альдозы, отличающихся только конфигурацией атома углерода, ближайшего к альдегидной группе, называются эпимерами, поэтому вся реакция получила название эпимиризации. Образующаяся при реакции кетоза (фруктоза) является структурным, а не пространственным изомером, то есть не относится к эпимерам.
3. Ретроальдольное расщепление
Происходит под влиянием более концентрированных, чем для эпимеризации, водных растворов щелочей и, как правило, при нагревании. При таком расщеплении получается сложная смесь соединений, молекулы которых состоят, в основном, из трех атомов углерода (глицериновый альдегид, диоксиацетон) и более коротких молекул (формальдегид, гликолевый альдегид).
Реакция идет по механизму, обратному механизму альдольной конденсации.
4. Образование фенилозазонов
Наблюдается при действии на монозы трехкратного количества фенилгидразина.
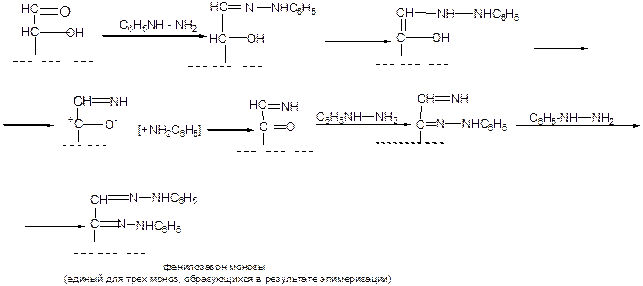
При кислотно-католизируемом гидролизе или обработке бензальдегидом фенилозазоны превращаются в озоны, восстановление которых амальгамой натрия в слабокислой среде позволяет перейти от альдоз к кетозам:
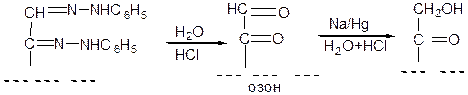 .
.
5. Окисление
а) Окисление под действием слабых (мягких) окислителей с образованием глюконовой кислоты.
В качестве слабых окислителей используют аммиачный раствор гидроксида серебра (реактив Толленса); реактив Фелинга – смесь 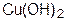 с калий-натрий-тартратом; раствор брома в воде (бромную воду); разбавленный раствор
с калий-натрий-тартратом; раствор брома в воде (бромную воду); разбавленный раствор 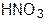 .
.
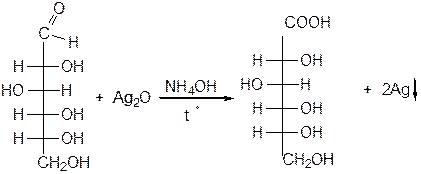
D-глюкоза D-глюконовая
кислота
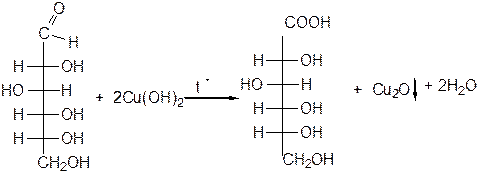
Глюкоза глюконовая
Кислота
Реакции с реактивом Толленса («реакция серебряного зеркала») и реактивом Фелинга являются качественными реакциями на альдозы.
б) Окислители со средней окисляющей способностью, например концентрированная 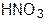 , превращающуют в карбоксильную группу не только альдегидную, но и первично-спиртовую группу, окисляя альдозы до сахарных кислот:
, превращающуют в карбоксильную группу не только альдегидную, но и первично-спиртовую группу, окисляя альдозы до сахарных кислот:
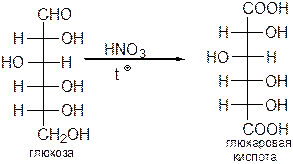
в) Окисление 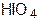 приводит к образованию смеси формальдегида с муравьиной кислотой, т. е. происходит деструкция цепи:
приводит к образованию смеси формальдегида с муравьиной кислотой, т. е. происходит деструкция цепи:
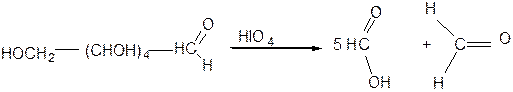
г) Окисление моноз, имеющих защищенную (не способную реагировать) альдегидную групп, например простых эфиров с группировкой 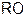 у первого углеродного атома, концентрированной
у первого углеродного атома, концентрированной 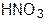 приводит к образованию уроновых кислот:
приводит к образованию уроновых кислот:
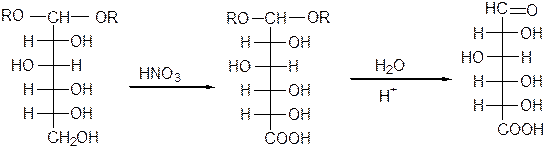
Гликозид D-глюкуроновая
D-глюкозы кислота
6. Восстановление моноз
При восстановлении моноз получаются полиолы, называемые сахарными спиртами. Так, из глюкозы и фруктозы получают шестиатомный спирт сорбит, из маннозы – манит, из галактозы – дульцит, из ксилозы – пятиатомный спирт ксилит и т. д.
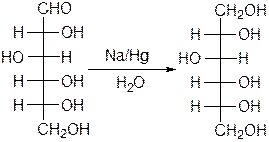
D-глюкоза D-Сорбит
(глюцит)
Для восстановления используют амальгаму натрия в водной, водно-спиртовой или спиртовой среде; водород в присутствии катализаторов (Ni, Pt, Pd) и гидриды металлов.
При восстановлении альдоз образуется один спирт, а при восстановлении кетоз – два стереоизомерных полиола:
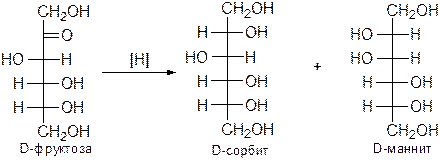
7. Дегидратация
Идет плд действием минеральных кислот и приводит к производным фурана.
Пентозы теряют три молекулы воды, превращаясь в фурфурол (2-фуран-альдегид):
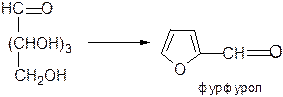
Гексозы также дают производные фурана – 5-гидроксиметилфурфурол, который, теряя молекулу муравьиной кислоты, превращается в левулиновую кислоту (2-оксопентановую):
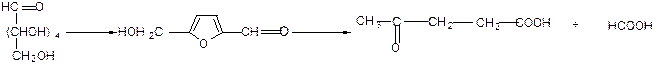 левулиновая кислота
левулиновая кислота
8. Укорочение цепи (синтез Воля)
Позволяет перейти от монозы с большим числом атомов углерода в цепи к соединениям с более короткой цепью вплоть до глицеринового альдегида. 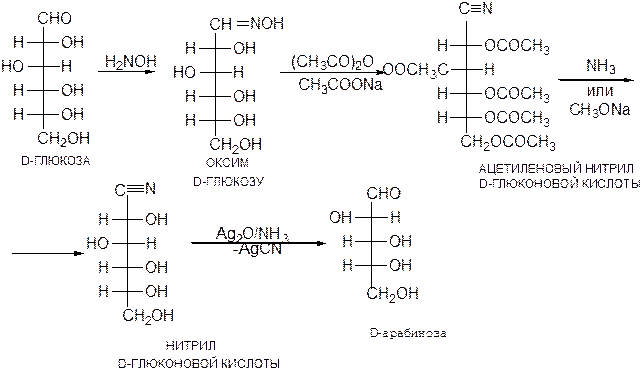
9. Удлинение цепи
Углеродная цепь наращивается циангидридным методом:
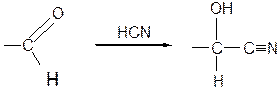
затем идет гидролиз нитрила с образованием лактона кислоты, при восстановлении которого получается моноза, содержащая на один атом углерода больше, чем исходная.
10. Алкилирование
а) При обработке моноз спиртами в присутствии газообразного HCl получаются ацетали, называемые гликозидами. В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не учавствуют. Образующийся алкилгликозид является смесью аномеров (в формулах Хеуорса и конформационных формулах неопределенная конфигурация гликозидного гидроксила изображается горизонтально расположенным волнистым валентным штрихом):
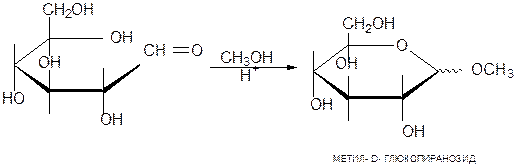
Гликозиды, в которых связь с алкильным остатком, образована через атом кислорода, называют О-алкилгликозидами. Они легко гидролизуются водными растворами кислот, но устойчивы к гидролизу в щелочных условиях.
б) Действие на монозы алкилгалогенидов в смеси с оксидом серебра или диалкилсульфатов в щелочной среде приводит к алкилированным моносахаридам. Обычно эту реакцию проводят с О-метилгликозидами для получения исчерпывающе метилированных моноз.
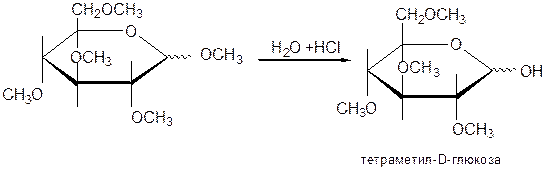
11. Ацилирование моноз
Происходит при действии на монозы, хлорангидридов или ангидридов кислот, в присутствии кислых (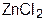 ) или основных (пиридин, ацетат натрия) катализаторов:
) или основных (пиридин, ацетат натрия) катализаторов:
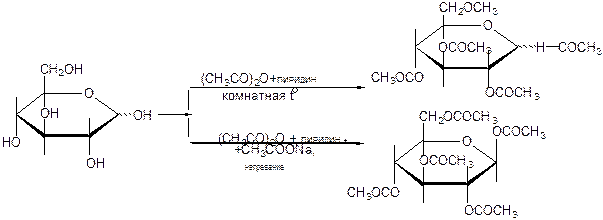
12. Брожение
Отличительным свойством моносахаридов является их способность вступать в анаэробное (без доступа кислорода) расщепление под влиянием микроорганизмов или выделенных из них ферментов. Такие процессы называются брожением.
Наиболее легко подвергаются брожению глицериновый альдегид, диоксиацетон и гексозы. Легче подвергаются брожению монозы D-ряда, то есть встречающиеся в природе, чем монозы L-ряда.
Спиртовое брожение – это расщепление глюкозы в анаэробных условиях смесью ферментов, зимазой, которую выделяют дрожжевые грибки.
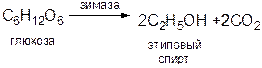
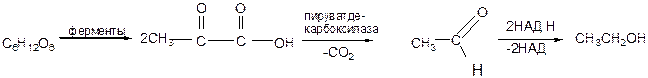
Уксуснокислое брожение. Если брожение осуществляется в присутствии кислорода, то в качестве основного продукта получают уксусную кислоту.
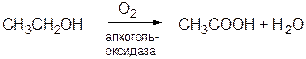
Таким образом получают “винный уксус” (пищевую уксусную кислоту) специально, но этот процесс ответственен также за “прокисание” вина при нарушении технологии спиртового брожения и при негерметичном хранении неокрепшего вина.
Молочнокислое брожение. Известны два вида молочнокислого брожения. При ферментативном брожении под действием Lactobacillus delbruckii
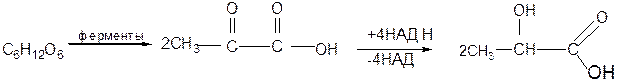
Этот процесс реализуется в производстве молочной кислоты, кисломолочных продуктов, хлеба, при силосовании кормов в сельском хозяйстве. В ином варианте ферментативного брожения (Bacterium lactis aerogene  s) образуются молочная кислота, уксусная кислота, этиловый спирт,
s) образуются молочная кислота, уксусная кислота, этиловый спирт, 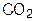 и некоторые другие соединения. Такое брожение идет при квашении плодов и овощей.
и некоторые другие соединения. Такое брожение идет при квашении плодов и овощей.
Лимоннокислое брожение:
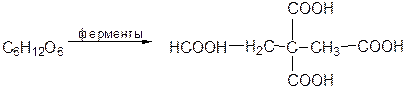
Маслянокислое брожение:
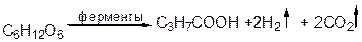
Известны и другие типы брожения, например, ацетон-бутиловое и др.
Важнейшие представители
1. Ксилоза ( древесный сахар).Входит в состав полисахаридов ксиланов, содержащихся в древесине, соломе, кукурузных кочерыжках, лузге подсолнечника. При гидролизе получают D-ксилозу.
Ксилоза – бесцветное кристаллическое вещество.
Ксилоза не усваивается организмом человека и не подвергается брожению.
При нагревании ксилозы в водных растворах серной кислоты происходит циклизация и отщепление воды. Образуется гетероциклическое соединение фурфурол 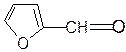 .
.
2. Рибоза. Входит в состав рибонуклеиновых кислот и может быть получена их гидролизом.
Бесцветное крисаллическое вещество, хорошо растворимое в воде
Рибоза используется в синтезе нуклеозидов.
3. 2- Дезоксирибоза
Образует бесцветные металлы, хорошо растворимые в воде. В кристаллическом виде существует в виде фуранозы.
Дезоксирибоза используется в синтезах нуклеозидов.
4. Глюкоза(виноградный сахар).
В свободном виде содержится во фруктовых соках.
В кристаллическом виде можно получить оба аномера D-глюкозы a – и 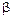 -формы. Оба являются бесцветными кристаллическими веществами с приятным сладким вкусом, оптически активны.В растворе наблюдыется мутаротация. Чистую глюкозу получают кислотным гидролизом крахмала.
-формы. Оба являются бесцветными кристаллическими веществами с приятным сладким вкусом, оптически активны.В растворе наблюдыется мутаротация. Чистую глюкозу получают кислотным гидролизом крахмала.
Используют глюкозу в пищевой промышленности, медицине, для синтеза глюконовой и аскорбиновой кислот, в качестве восстановителя в текстильной промышленности, для получения этилового спирта.
5. Галактоза.
Встречается в природе в свободном виде, в виде гликозидов, дисахаридов (лактозы), полисахаридов. Она входит в состав стероидных алкалоидов, выделенных из растении семейства пасленовых, например соланина, содержащегося в картофеле.
6. Фруктоза(плодовый сахар, левулоза.
Распространена в растительном мире. Содержится в помидорах, яблоках. Больше всего ее в пчелином меде (до 50%).
Получают фруктозу гидролизом сахарозы.
Фруктоза – наиболее сладкая из всех сахаров. Она в 1,5 раза слаще сахарозы и в 3 раза слаще глюкозы. Используют фруктозу в медицине как ценный продукт питания
7. Сорбоза и аскорбиновая кислота. Кетогексоса сорбоза содержится в природных продуктах, принадлежит к L-ряду.Получают микробиологическим окислением D-сорбита. В кристаллическом состоянии существует в форме пиранозы. Оптически активна.
L-Сорбоза служит исходным веществом для синтеза аскорбиновой кислоты (витамина С).
L-Аскорбиновая кислота – бесцветное кристалличекое вещество с кислым вкусом, хорошо растворяется в воде, оптически активна. Содержится во многих фруктах и овощах. Важный витамин. Является сильным восстановителем, так как имеет едиольную структуру. Суточная потребность в ней для человека – не менее 50мг.
8. Гликозиды. Связь между агликоном и остатком монозы (гликозидная связь) может осуществляться через атомы кислорода, азота и углерода. В зависимости от этого различают O-,N- и С-гликозиды:
В природе наиболее распространены O- и N-гликозиды. Большое количество О-гликозидов встречается в растениях, например ванилин- 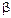 -D- глюкопиранозин в стручках ванили; кониферин в составе лигнина; амигдалин в косточках горького миндаля, абрикосов, слив, вишен, в листьях лавровишни и пр. Наиболее распространенными в природе N-гликозидами являются компоненты нуклеиновых кислот – нуклеозиды:
-D- глюкопиранозин в стручках ванили; кониферин в составе лигнина; амигдалин в косточках горького миндаля, абрикосов, слив, вишен, в листьях лавровишни и пр. Наиболее распространенными в природе N-гликозидами являются компоненты нуклеиновых кислот – нуклеозиды:
Значительно реже встречаются С- гликозиды. Такие гликозиды, в которых агликонами служат остатки аденина являются антибиотиками.
Все гликозиды устойчивы к щелочному гидролизу.
|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 3327; Нарушение авторских прав?; Мы поможем в написании вашей работы!