
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Критерии оценивания заданий с развёрнутым ответом
|
|
|
|
Работа 2
Работа 1

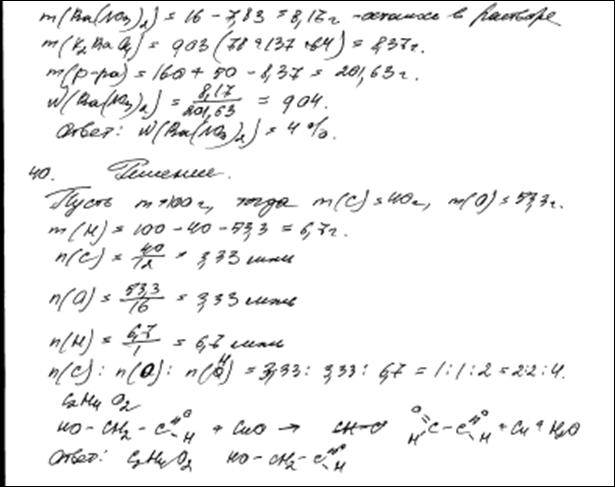


| 36 |
Используя метод электронного баланса, составьте уравнение реакции:
Cr2(SO4)3 + Cl2 + … ® K2CrO4 + KCl + … + H2O
Определите окислитель и восстановитель.
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы | ||
Элементы ответа:
1) Составлен электронный баланс:
| |||
| 2) Указано, что сульфат хрома(III) (за счёт хрома в степени окисления +3) является восстановителем, а хлор в степени окисления 0 – окислителем. | |||
| 3) Определены недостающие в схеме вещества, и расставлены коэффициенты в уравнении реакции: Cr2(SO4)3 + 3Cl 2 + 16KOH = 2K2CrO4 + 6KCl + 3K2SO4 + 8H2O | |||
| Ответ правильный и полный, содержит все названные выше элементы | |||
| Правильно записаны только два из названных выше элементов ответа | |||
| Правильно записан один из названных выше элементов ответа | |||
| Все элементы ответа записаны неверно | |||
| Максимальный балл | 3 |
| 37 |
Карбид алюминия полностью растворили в бромоводородной кислоте.
К полученному раствору добавили раствор сульфита калия, при этом наблюдали образование белого осадка и выделение бесцветного газа. Газ поглотили раствором дихромата калия в присутствии серной кислоты.
Образовавшуюся соль хрома выделили и добавили к раствору нитрата бария, наблюдали выделение осадка. Напишите уравнения четырёх описанных реакций.
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
| Ответ включает в себя четыре уравнения возможных реакций, соответствующих описанным превращениям: 1) Al4C3 + 12HBr = 4AlBr3 + 3CH4↑ 2) 2AlBr3 + 3K2SO3 + 3H2O = 2Al(OH)3¯ + 3SO2↑ + 6KBr 3) 3SO2 + K2Cr2O7 + H2SO4 = Cr2(SO4)3 + K2SO4 + H2O 4) Cr2(SO4)3 + 3Ba(NO3)2 = 3BaSO4¯ + 2Cr(NO3)3 | |
| Правильно записаны четыре уравнения реакций | |
| Правильно записаны три уравнения реакций | |
| Правильно записаны два уравнения реакций | |
| Правильно записано одно уравнение реакции | |
| Все элементы ответа записаны неверно | |
| Максимальный балл | 4 |
| 38 |
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:

При написании уравнений реакций используйте структурные формулы органических веществ.
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
Ответ включает в себя пять уравнений реакций, соответствующих схеме превращений:

| |
| Правильно записаны пять уравнений реакций | |
| Правильно записаны четыре уравнения реакций | |
| Правильно записаны три уравнения реакций | |
| Правильно записаны два уравнения реакций | |
| Правильно записано одно уравнение реакции | |
| Все уравнения реакций записаны неверно | |
| Максимальный балл | 5 |
Примечание. Допустимо использование структурных формул разного вида (развёрнутой, сокращённой, скелетной), однозначно отражающих порядок связи атомов и взаимное расположение заместителей и функциональных групп в молекуле органического вещества.
| 39 |
Газ, выделившийся при взаимодействии 7,4 г нитрида кальция с 9 г воды, полностью поглощён 200 мл 3,5%-ного раствора соляной кислоты ( = 1,05 г/мл). Определите массовую долю хлорида аммония в образовавшемся растворе.
= 1,05 г/мл). Определите массовую долю хлорида аммония в образовавшемся растворе.
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
Элементы ответа.
1) Составлены уравнения реакций:
Ca3N2 + 6H2O = 3Ca(OH)2 + 2NH3
NH3 + HCl = NH4Cl
2) Определено количество вещества NH3, и указано, что вода дана в избытке:
n(Ca3N2) = 7,4 /148 = 0,05 моль
n(H2O) = 9 / 18 = 0,5 моль, следовательно, H2O – в избытке.
n(NH3) = 2n(Ca3N2) = 0,1 моль
3) Определено количество вещества NH4Cl, и указано, что HCl – в избытке:
n(HCl) =  / 36,5 = 0,2 моль
HCl – в избытке
n(NH3) = n(NH4Cl) = 0,1 моль
4) Определена массовая доля NH4Cl:
m(NH4Cl) = 0,1 · 53,5 = 5,35 г
ω(NH4Cl) = 5,35 / / 36,5 = 0,2 моль
HCl – в избытке
n(NH3) = n(NH4Cl) = 0,1 моль
4) Определена массовая доля NH4Cl:
m(NH4Cl) = 0,1 · 53,5 = 5,35 г
ω(NH4Cl) = 5,35 /  = 0,025 или 2,5% = 0,025 или 2,5%
| 2. |
| Ответ правильный и полный, включает все названные выше элементы | |
| В ответе допущена ошибка в одном из названных выше элементов | |
| В ответе допущены ошибки в двух из названных выше элементов | |
| В ответе допущены ошибки в трёх из названных выше элементов | |
| Все элементы ответа записаны неверно | |
| Максимальный балл | 4 |
Примечание. В случае, когда в ответе содержится ошибка в вычислениях в одном из элементов (во втором, третьем или четвёртом), которая привела к неверному ответу, оценка за выполнение задания снижается только на 1 балл.
| 40 |
При сгорании 4,48 л (н.у.) газообразного органического вещества получили 35,2 г углекислого газа и 10,8 мл воды. Плотность этого вещества составляет 2,41 г/л (н.у.). Известно также, что это вещество не реагирует с аммиачным раствором оксида серебра, а при реакции его с избытком бромной воды происходит присоединение атомов брома только ко вторичным атомам углерода.
На основании данных условия задачи:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества;
3) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции этого вещества с избытком бромной воды.
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
Элементы ответа:
Общая формула вещества – CxHyOz
1) Найдены количество вещества углекислого газа, воды и органического вещества:
n(CO2) = 35,2 / 44 = 0,8 моль
n(H2O) = 10,8 / 18 = 0,6 моль
M(CxHyOz) = 2,41 · 22, 4 = 54 г/моль
n(CxHyOz) = 4,48 / 22,4 = 0,2 моль
2) Определена молекулярная формула вещества:
n(C) = n(CO2) = 0,8 моль
n(H) = 2n(H2O) = 1,2 моль
x = n(C) / n(CxHyOz) = 0,8 / 0,2 = 4
y = n(H) / n(CxHyOz) = 1,2 / 0,2 = 6
4 · 12 + 6 + z · 16 = 30
z = 0
Молекулярная формула – C4H6
3) Составлена структурная формула вещества:
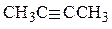 4) Составлено уравнение реакции этого вещества с избытком бромной воды:
4) Составлено уравнение реакции этого вещества с избытком бромной воды:
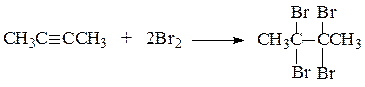
| |
| Ответ правильный и полный, содержит все названные выше элементы | |
| В ответе допущена ошибка в одном элементе ответа | |
| В ответе допущена ошибка в двух элементах ответа | |
| В ответе допущена ошибка в трёх элементах ответа | |
| Все элементы ответа записаны неверно | |
| Максимальный балл | 4 |
Работа 1



|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 1007; Нарушение авторских прав?; Мы поможем в написании вашей работы!
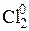 + 2 ē → 2 Cl –
+ 2 ē → 2 Cl –