
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
За будовою ця кислота є насиченою монокарбоновою, з відкритим ланцюгом. Виберіть цю кислоту.
|
|
|
|
A. 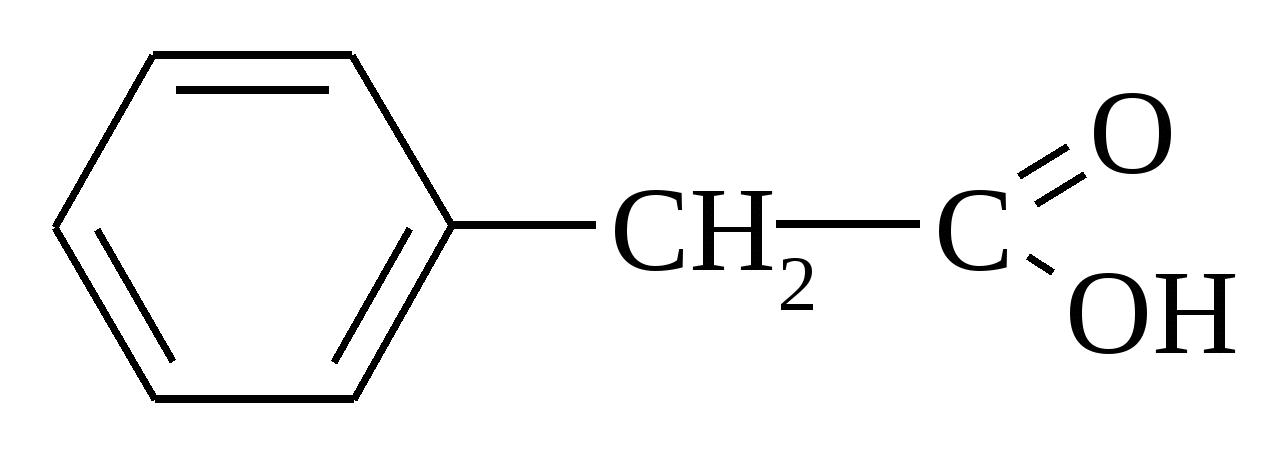 B.
B. 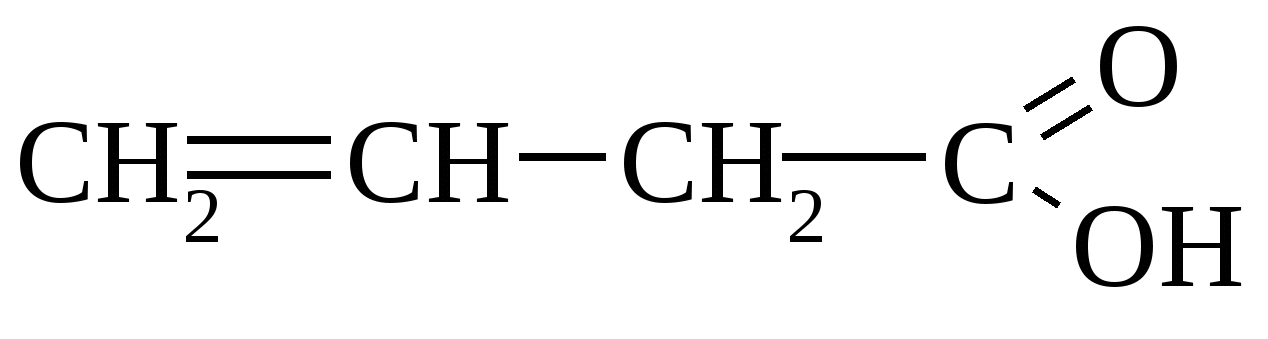 C.
C. 
 D.
D.
9. Вкажіть, похідною якої гетерофункціональної сполуки є зображена формула препарату анестезин:
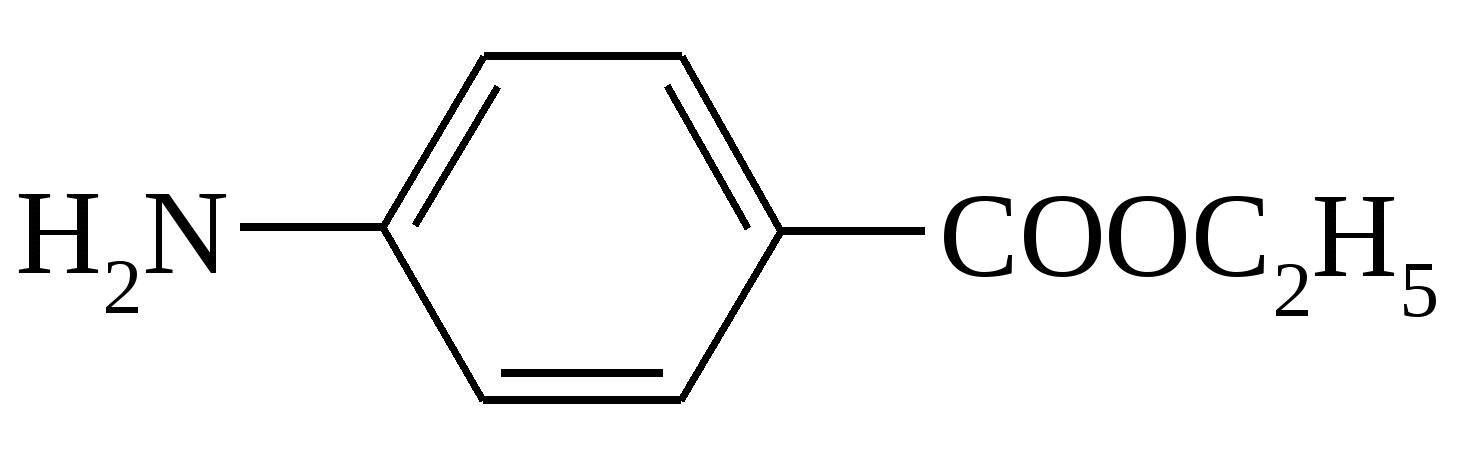
А. n -Амінобензойної кислоти. B. Саліцилової C. Молочної кислоти D. Коламіну
Практична робота № 2
«Амінокислоти»
Актуальність теми: Біоорганічні сполуки належать переважно до гетеро- функціональних, що містять дві або більше функціональних груп. α - Амінокислоти L- ряду є структурною ланкою пептидів та білків, що є основою всіх живих організмів. Самостійна позааудиторна робота студентів: Засвоїти матеріал навчальної програми: Будову, властивості та медико – біологічне значення амінокислот та їх похідних.
Блок інформації: До складу білків входять близько 20 α - Амінокислот L- ряду. 
Хімічні властивостіамінокислот. 1. Амфотерні властивості. Оскільки до складу амінокислот входять дві функціональні групи, то амінокислоти проявляють властивості двох класів сполук: карбонових кислот (кислотні властивості) та органічних амінів (основні властивості). Водні розчини амінокислот мають нейтральне, лужне або кисле середовище залежно від співвідношення функціональних груп. Більшість амінокислот мають нейтральне середовище. Глутамінова, аспарагінова кислоти утворюють кислий розчин (дві групи -СООН, одна NH2), лізин, аргінін — лужний (одна група — СООН, дві — NН2). 2. Утворення пептидного зв'язку. Αмінокислоти внаслідок взаємодії карбоксильної та аміногрупи вступають в реакцію поліконденсації й утворюють пептиди:
 Групу – СО – NН – називають пептидною групою.
Групу – СО – NН – називають пептидною групою.
Сполука, яка утворюється в результаті конденсації двох амінокислот, називається дипептид. На одному кінці його молекули перебуває вільна аміногрупа, а на іншому — карбоксильна група. Завдяки цьому дипептид може також приєднувати до себе наступні молекули амінокислот. В організмі амінокислоти сполучаються між собою багато разів до утворення білкової молекули.
3.Біологічно важливі хімічні реакції амінокислот. Низка важливих перетворень α-амінокислот в організмі відбувається під впливом вітаміну В6.
- Декарбоксилування (руйнування карбоксильної групи) - утворення біогенних амінів.
 Серин Коламін При декарбоксилуванні серину утворюється коламін
Серин Коламін При декарбоксилуванні серину утворюється коламін
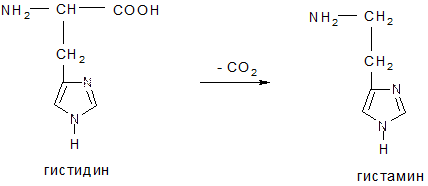 При деяких патологічних станах в організмі з амінокислоти гістидин утворюється значна кількість біогенного аміну гістаміну. Унаслідок накопичення гістаміну виникають різні захворювання алергійного характеру. Окиснення і декарбоксилування триптофану приводять до утворення біогенного аміну серотоніну.
При деяких патологічних станах в організмі з амінокислоти гістидин утворюється значна кількість біогенного аміну гістаміну. Унаслідок накопичення гістаміну виникають різні захворювання алергійного характеру. Окиснення і декарбоксилування триптофану приводять до утворення біогенного аміну серотоніну.  Серотонін вважається нейромедіатором кори головного мозку. Порушення його обміну спричиняє захворювання на шизофренію. Важливу роль відіграють і інші біогенні аміни, такі як холін, норадреналін, адреналін. - - --- Дезамінування – відщеплення аміногрупи. Наприклад, при окисному дезамінуванні аланіну утворюється піровіноградна кислота (ПВК).
Серотонін вважається нейромедіатором кори головного мозку. Порушення його обміну спричиняє захворювання на шизофренію. Важливу роль відіграють і інші біогенні аміни, такі як холін, норадреналін, адреналін. - - --- Дезамінування – відщеплення аміногрупи. Наприклад, при окисному дезамінуванні аланіну утворюється піровіноградна кислота (ПВК).
 У результаті реакції дезамінування утворюється токсичний амоніак. Для його знешкодження в організмі постійно відбувається утворення нетоксичних продуктів – сечовини або сечової кислоти, які виводяться із сечею. Медико – біологічне значення амінокислот. Амінокислоти є основним будівельним матеріалом для синтезу специфічних тканинних білків, ферментів, пептидних гормонів і інших фізіологічно активних сполук. Крім того, що амінокислоти утворюють білки, амінокислоти широко використовують в сучасній фармакології: Амінооцтову кисоту (гліцин) використовують для поліпшення пам΄яті, при розумової відсталості у дітей, алкоголізмі. γ- Аміномасляну кислоту (ГАМК, аміналон) використовують для лікування нервово-психічних захворювань, при ослабленні пам΄яті, порушенні мозкового кровообігу. Глутамінову кислоту використовують для лікування психічних захворювань. Амінокислоти застосовують також у якості парентерального харчування хворих, тобто минаючи шлунково-кишковий тракт, із захворюваннями травних і інших органів; а також для лікування захворювань печінки, недокрів'я, опіків (метіонін), виразок шлунка (гістидин).
У результаті реакції дезамінування утворюється токсичний амоніак. Для його знешкодження в організмі постійно відбувається утворення нетоксичних продуктів – сечовини або сечової кислоти, які виводяться із сечею. Медико – біологічне значення амінокислот. Амінокислоти є основним будівельним матеріалом для синтезу специфічних тканинних білків, ферментів, пептидних гормонів і інших фізіологічно активних сполук. Крім того, що амінокислоти утворюють білки, амінокислоти широко використовують в сучасній фармакології: Амінооцтову кисоту (гліцин) використовують для поліпшення пам΄яті, при розумової відсталості у дітей, алкоголізмі. γ- Аміномасляну кислоту (ГАМК, аміналон) використовують для лікування нервово-психічних захворювань, при ослабленні пам΄яті, порушенні мозкового кровообігу. Глутамінову кислоту використовують для лікування психічних захворювань. Амінокислоти застосовують також у якості парентерального харчування хворих, тобто минаючи шлунково-кишковий тракт, із захворюваннями травних і інших органів; а також для лікування захворювань печінки, недокрів'я, опіків (метіонін), виразок шлунка (гістидин).
Завдання для позаудиторної самостійної роботи:
1. Дайте визначення амінокислотам, наведіть загальну формулу
α- Амінокислоти L- ряду, формули та назви окремих представників (не менше трьох).
2. Напишіть назви незамінних амінокислот та вкажіть продукти харчування, в яких вони містяться.
3. Вкажіть медико – біологічне значення амінокислот.
Зміст і методика проведення аудиторного заняття
План проведення заняття 1. Дати відповіді на питання вихідного рівня знань: 1) α - Амінокислоти L- ряду: визначення, загальна формула, окремі представники. 2) Класифікація амінокислот: за природою радикала; за співвідношенням функціональних груп; за здатністю до синтезу в організмі. 3) Вкажіть незамінні амінокислоти та вміст їх в продуктах харчування. 4) Назвіть біологічно важливі реакції амінокислот. Складіть рівняння реакції утворення дипептиду (Глі – Ала), трипептиду Глі- Ала – Глі). 2. Лабораторна робота.
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 405; Нарушение авторских прав?; Мы поможем в написании вашей работы!