
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химия кислорода и его соединений
|
|
|
|
Химия элементов VIA группы
VIA группу образуют четыре неметалла: кислород, сера селен, теллур, называемые халькогенами, и радиоактивный металл полоний. Атомы элементов VIA группы имеют электронную формулу ns2np4. Для них характерны степени окисления -2, 0, +4, +6. У атома кислорода отсутствуют 2d-орбитали, поэтому его валентность равна двум. Наличие d-орбиталей у атомов других элементов позволяет им иметь валентности два, четыре или шесть.
Кислород - самый распространенный элемент, на его долю приходится 47,2% по массе литосферы и атмосферы вместе взятых. Кислород взаимодействует с большинством химических элементов. Белки, жиры и углеводы являются органическими кислородосодержащими веществами. Как животные, так и растения при дыхании поглощают атмосферный кислород. Теплокровные животные погибают без кислорода в течении нескольких минут. С участием кислорода идет минерализация растительных или животных остатков в почве до NH3, CO2 и H2O. Без аэрации почва не может быть плодородной.
Кислород представляет собой газ без цвета, без вкуса, без запаха. Кислород может быть получен при сжижении и разделении воздуха. В лаборатории кислород получают разложением перманганата калия или разложением хлората калия - бертолетовой соли:
2KMnO4  K2MnO4 + MnO2 + O2
K2MnO4 + MnO2 + O2
2KClO3  2KCl + 3O2
2KCl + 3O2
Известны две аллотропические модификации кислорода: кислород О2 и озон О3. Озон может быть получен из кислорода под действием электрического разряда или ультрафиолетового излучения:
3О2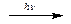 2О3
2О3
Озон - сильный окислитель. его активность обусловлена распадом его молекул с образованием атомарного кислорода, который более активен, чем молекулярный кислород:
О3 ® О2 + О
|
|
|
Молекулярный кислород (степень окисления равна нулю) является активным окислителем. Кислород в низшей степени окисления -2 (в оксидах, в воде) окислителем быть не может. В промежуточной степени окисления -1, например, в пероксиде водорода, кислород может иметь как окислительные, так и восстановительные свойства. С сильными окислителями пероксид водорода проявляет восстановительные свойства, окисляясь до кислорода О2.
2KMnO4 + 3H2SO4 + 5H2O2 ® 5O2 + 2MnSO4 + K2SO4 + 8H2O
С сильными восстановителями пероксид водорода проявляет окислительные свойства. Кислород при этом восстанавливается до степени окисления -2.
2KI + H2SO4 + H2O2 ® I2 + K2SO4 + 2H2O
Пероксид водорода может быть получен действием кислот на пероксиды металлов:
BaO2 + H2SO4 ® BaSO4 + H2O2
Окислительная активность пероксида водорода, обуславливающая его обеззараживающие свойства, связана с образованием в момент выделения атомарного кислорода:
Н2О2 ® Н2О + О
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 295; Нарушение авторских прав?; Мы поможем в написании вашей работы!