
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Частные политропные процессы
|
|
|
|
Связь между параметрами процесса.
Если индикаторная диаграмма обработана, то
pvn = const или p1v1n = p2v2n и p1/p2 = (v2/v1)n (3.7)
для любых двух состояний процесса. Для рабочих тел, у которых уравнения состояния или сложны или, чаще, просто отсутствуют, найти связь температуры Т с другими параметрами состояния р или v аналитическим путем невозможно.
Для идеального газа, т.е. кроме связи pvn = const еще справедлива связь pv = RуT, сочетание этих зависимостей позволяет получить взаимосвязь:
T1 / T2 = (v2 / v1)n-1 = (p1 / p2)(n-1)/n. (3.8)
Замечание. Вывод связей (3.8) предлагаем провести самостоятельно.
Если какой-то параметр состояния при взаимодействии с внешней средой фиксировать, то процесс, входящий в гамму политропных, называют частным:
pvn = const и p = const → n = 0 – изобарный,
а для идеального газа из (3.8) T1/T2 = v1/v2.
pvn = const и v = const → n = ± ∞ - изохорный,
а для идеального газа из (3.8) T1/T2 = p1/p2.
pvn = const и T = const – изотермический,
а для идеального газа n = 1 и из (3.8) v2/v1 = p1/p2.
При s = const → n = k ≡ cp / cv – изоэнтропийный (адиабатный) с уравнением
pvk = const.
Замечание. Условие Q (q) = 0 (нет источников теплоты) означает, что Tds ≡ 0 и s = const и по первому признаку процесс назван адиабатным (adiabatos – непереходимая – в смысле тепловой изоляции)
На рис.3.2 представлены графики политроп с различными показателями n для частных процессов, только еще раз напомним, что величина показателя адиабаты для двухатомных газов k ≈ 1,4.
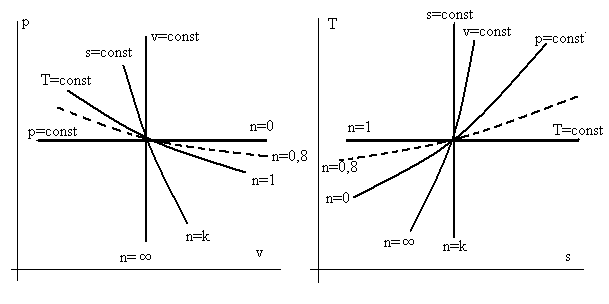
Рис. 3.2. Взаимное расположение частных политропных
процессов в осях p – v и T – s при различных значениях
показателей политропы n.
Замечание. Если необходимо построить график оригинального политропного процесса, т.е. не совпадающего с указанными частными, то, зная величину n, не сложно построить этот график на фоне частных процессов.
Пример. Построить график политропного процесса с показателем политропы n = 0,8 в осях p – v и T – s.
Решение этой задачи основано на том обстоятельстве, что линии частных процессов делят всю плоскость с координатными осями на сектора. Следовательно, график (в осях p – v или T – s) политропного процесса с каким-то n должен проходить в соответствующем секторе. На рис. 3.2 линия с n = 0,8 расположена в секторе между политропами n = 0 и n = 1 и обозначена пунктиром.
1.3. Расчет изменения функций состояния Δu, Δh
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2651; Нарушение авторских прав?; Мы поможем в написании вашей работы!