
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Степень электролитической диссоциации
|
|
|
|
Основные положения теории растворов электролитов. Общая (аналитическая) концентрация и активность ионов в растворе, их взаимосвязь.
При установившемся равновесии отношение произведения концентраций продуктов реакции к произведению концентраций исходных веществ представляет собой для данной реакции при данной температуре величину постоянную, называемую константой равновесия. При этом концентрации каждого вещества должны быть возведены в степень, соответствующую их стехиометрическому коэффициенту.
ЗДМ строго применим к неэлектролитам и слабым электролитам в разбавленных водных растворах. Концентрированные водные растворы слабых электролитов и все сильные электролиты (кислоты, щелочи, соли) дают существенные отклонения от ЗДМ.
Значение константы равновесия позволяет оценить направление и глубину протекания химической реакции. При К = 1 скорости прямой и обратной реакции равны. Если К > 1, это благоприятствует протеканию реакции в прямом направлении, если К < 1 – в обратном.
Следовательно, изменение концентраций реагирующих веществ или их продуктов вызывает смещение равновесия химической реакции. При увеличении концентраций А и В и уменьшении С и D равновесие сдвигается вправо, при увеличении концентраций С и D равновесие сдвигается влево.
Большинство реакций, используемых в аналитической химии, проводится в растворах. В соответствии с теорией электролитической диссоциации электролиты в растворах распадаются (диссоциируют) на положительно и отрицательно заряженные ионы вследствие взаимодействия с молекулами растворителя. Положительно заряженные ионы называют катионами (ионы водорода, металлов). Отрицательно заряженные ионы называются анионами (ионы кислотных остатков, гидроксид-ионы).
Процесс электролитической диссоциации изображают химическими уравнениями, например:
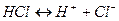
Количественно диссоциация (ионизация) характеризуется степенью диссоциации (ионизации), которая равна отношению числа молей, продиссоциировавших молекул (Сдисс) к общему числу молей (Сисх) растворенного электролита и численно выражается в долях единицы или процентах(%):
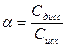 или
или 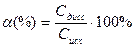
По способности к диссоциации электролиты разделяют на 3 группы:
1. сильные электролиты (α= 1, диссоциируют полностью). К сильным электролитам относят большинство солей (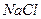 ,
, 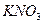 ,
, 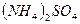 и др.), неорганические кислоты (
и др.), неорганические кислоты (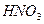 ,
, 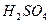 ,
, 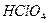 ,
, 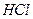 ,
, 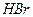 ,
, 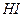 ) и щелочи (
) и щелочи (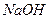 ,
, 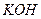 ,
, 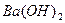 ,
, 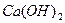 . Степень диссоциации составляет 30% и более процентов.
. Степень диссоциации составляет 30% и более процентов.
2. слабые (α<1, диссоциируют частично). Степень диссоциации слабых электролитов составляет менее 3%. К этой группе относят сероводородную, борную кислоты, карбонат натрия, гидроксид аммония и др.
3. электролиты средней силы. Характеризуются степенью диссоциации от3 до 30%. К этой группе относят фосфорную кислоту, сернистую, щавелевую, 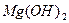 и некоторые соли тяжелых металлов.
и некоторые соли тяжелых металлов.
Для слабых электролитов степень диссоциации увеличивается с уменьшением концентрации (разбавлением) и увеличением температуры.
Степень диссоциации характеризует химическую активность электролитов. Например, хлороводородная кислота легко взаимодействует с металлическим цинком и быстро разлагает мрамор. Более слабая уксусная кислота медленнее взаимодействует и с цинком, и с мрамором. Многие, нерастворимые в уксусной кислоте соединения (сульфид цинка, оксалат кальция, хромат бария), легко растворяются в хлороводородной кислоте. Следовательно, чем выше степень диссоциации кислоты и ее концентрация, тем больше в растворе присутствует ионов водорода (протонов) и тем сильнее она в химическом отношении. Сила оснований также определяется степенью их диссоциации, т.е. концентрацией гидроксид-ионов.
Общая концентрация ионов в растворе сi определяется молярной концентрацией растворенного электролита (C, моль/л) с учетом его степени диссоциации (α) и числа ионов (m), на которые диссоциирует молекула электролита в растворе:
ci = m∙ α ∙C
Например, для 0,1 М раствора Al2(SO4)3 имеем:
Al2(SO4)3 → 2Al3+ + 3SO42- (α = 1)
c (Al3+) = 2∙1∙0,1 = 0,2 моль/л
c (SO42-) = 3∙1∙0,1 = 0,3 моль/л
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 919; Нарушение авторских прав?; Мы поможем в написании вашей работы!