
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные характеристики химической связи
|
|
|
|
МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ
Ковалентная химическая связь является двухэлектронной. Электроны, участвующие в образовании химической связи, имеют противоположные спины и образуют общую электронную пару.
Различают обменный и донорно-акцепторный механизмы образования химической связи:
1) Обменный – два атома предоставляют по одному электрону на образование общей электронной пары.
Например, образование молекул водорода и хлороводорода:
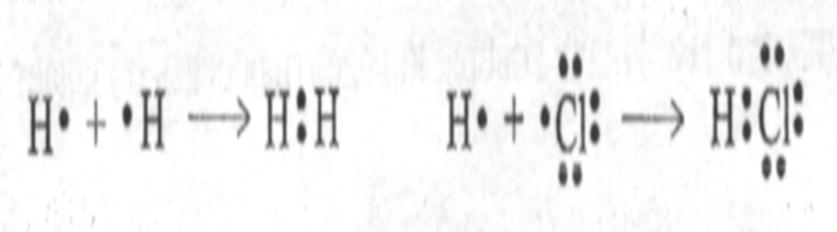
2) Донорно-акцепторный – один атом (донор) предоставляет электронную пару, а второй (акцептор) – свободную орбиталь.
Например, взаимодействие аммиака с ионом водорода с образованием катиона аммония
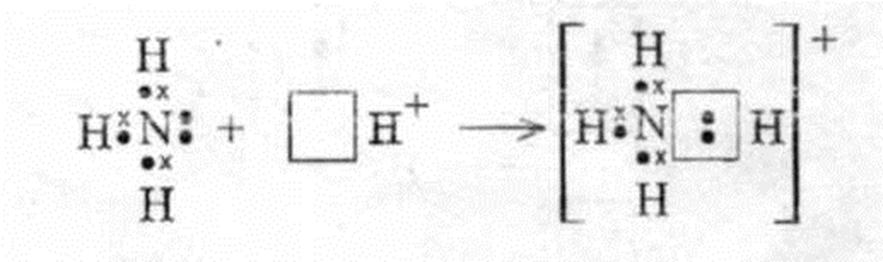
По способу перекрывания электронных облаков связи делят на σ-связь и π- связь:
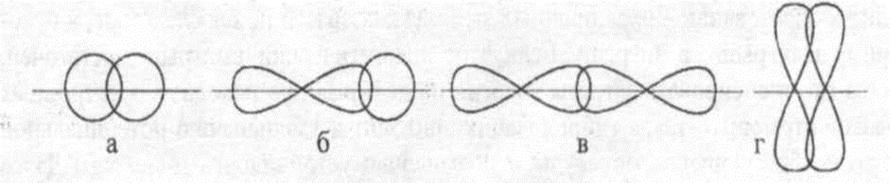
1) σ-связь образуется за счёт перекрывания электронных облаков по прямой линии, соединяющей центры взаимодействующих атомов. Она может осуществляться между двумя s-облаками, двумя p-облаками, s- и p-облаками или между s- и d-облаками.
2) π -связь образуется за счёт перекрывания электронных облаков выше и ниже линии, соединяющей центры взаимодействующих атомов. Она образуется в основном при перекрывании р-орбиталей.
σ-связь является более прочной чем π-связь.
Энергия связи – это энергия, необходимая для разрыва химической. Энергии разрыва и образовании связи равны по величине но противоположны по знаку. Чем больше энергия химической связи, тем устойчивее молекула. Обычно энергию связи измеряют в кДж/моль.
Для многоатомных соединений с однотипными связями за энергию связи принимается среднее ее значение, рассчитанное делением энергии образования соединения из атомов на число связей. Так, на разрыв связи H–H затрачивается 432,1 кДж/∙моль, а на разрыв четырех связей в молекуле метана CH4 – 1648 кДж/∙моль и в этом случае EC–H = 1648: 4 = 412 кДж/моль.
Длина связи – это расстоянию между ядрами взаимодействующих атомов в молекуле. Измеряется в нм или А (ангстрем=10-8 см). Она зависит от размеров электронных оболочек и степени их перекрывания.
Полярность связи – это распределение электрического заряда между атомами образовавшими химическую связь. Для определения полярности связи надо сравнить электоотрицательности атомов, участвовавших в образовании связи. Если электроотрицательности одинаковы, то связь будет неполярная, а в случае разных электроотрицательностей – полярной. Крайний случай полярной связи, когда общая электронная пара практически полностью смещена к более электроотрицательному элементу, приводит к ионной связи.
Например: Н–Н – неполярная, Н–Сl – полярная и Nа+–Сl- – ионная.
Смещением электронной пары к более электроотрицательному атому приводит к образованию диполя. Диполь – система из двух равных, но противоположных по знаку зарядов, находящихся по разным сторонам связи.
Полярность молекулы – это векторная сумма дипольных моментов всех связей молекулы. Следует различать полярности отдельных связей и полярность молекулы в целом.
Например, линейная молекула CO2 (О=С=О) неполярна, так как дипольные моменты полярных связей С=О компенсируют друг друга. Полярность молекулы воды означает, что она нелинейна, то есть дипольные моменты двух связей О—Н не компенсируют друг друга, так как расположены под углом, не равным 180°.
Пространственное строение молекул – форма и расположение в пространстве электронных облаков.
В соединениях, содержащих более двух атомов, важной характеристикой является валентный угол, образуемый химическими связями в молекуле и отражающий ее геометрию.
Порядок связи – это число химических связей между двумя атомами. Чем выше порядок связи, тем прочнее связаны между собой атомы и тем короче сама связь. Порядок связи выше трех не встречается. Например, порядок связи в молекулах H2, O2 и N2 равен соответственно 1, 2 и 3, поскольку связь в этих случаях образуется за счёт перекрывания одной, двух и трех пар электронных облаков.
4. ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ
4.1.Ковалентная связь – это связь между двумя атомами за счет образования общей электронной пары.
Количество химических связей определяется валентностями элементов. Валентность элемента равна числу орбиталей, принимающих участие в образовании химических связей. Ковалентная неполярная связь - эта связь, осуществляемая за счет образования электронных пар между атомами с практически равной электроотрицательностью. Например, Н2, О2, N2, Cl2 и т. д. Ковалентная полярная связь – эта связь, осуществляемая за счет образования электронных пар между атомами с различной электроотрицательностью. Например, НCl, H2S, PH3 и т.д. Ковалентная связь обладает свойствами: 1) Насыщаемости – способностью атома образовывать столько ковалентных связей, сколько у него имеется валентных орбиталей. 2) Направленности – перекрытие электронных облаков происходит в направлении обеспечивающем максимальную плотность перекрытия. 4.2.Ионная связь – это связь между противоположно заряженными ионами. Её можно рассматривать как крайний случай ковалентной связи. Как правило, она Такая связь возникает при большой разнице в электроотрицательностях взаимодействующих атомов. Иoннaя связь не обладает направленностью и насыщаемостью. Степень окисления – это условный заряд атома в соединении исходя из предположения, что происходит полная ионизация связей. образуется между металлом и неметаллом.
образуется между металлом и неметаллом.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 2018; Нарушение авторских прав?; Мы поможем в написании вашей работы!