
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Давление пара растворителя
|
|
|
|
Уравнение Гиббса-Дюгема позволяет найти давление пара растворителя 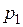 в зависимости от его концентрации, если известна зависимость давления пара растворенного вещества как функция температуры.
в зависимости от его концентрации, если известна зависимость давления пара растворенного вещества как функция температуры.
Выражая концентрацию в молярных долях и логарифмируя выражение (6.12), получим уравнение
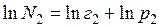 ,
,
дифференцирование которого дает по 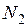 дает
дает
 или
или 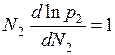 .
.
Отсюда, согласно уравнению 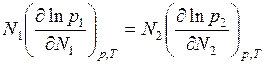 :
:
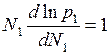 и
и 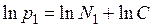 ,
,
где С – константа интегрирования и 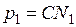 . Для определения С примем
. Для определения С примем 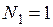 , тогда, очевидно,
, тогда, очевидно, 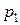 равно давлению пара чистого растворителя
равно давлению пара чистого растворителя
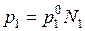 . (6.15)
. (6.15)
Это уравнение выражает закон Рауля, согласно которому давление пара растворителя над раствором меньше, чем давление пара чистого растворителя, и пропорционально молярной доле растворителя.
Исторически это закон был открыт эмпирическим путем на основании измерений давления пара различных органических растворителей над растворами. Рауль предложил для него следующую формулировку, равносильную уравнению (6.15): относительное понижение давления пара растворителя равно молярной доле растворенного вещества:
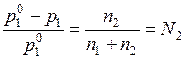 . (6.16)
. (6.16)
В отличие от закона Генри, который справедлив при любом способе выражения концентрации, закон Рауля требует, чтобы она выражалась в молярных долях. Оба закона справедливы для разбавленных растворов.
Из закона Рауля вытекают важные следствия, касающиеся температур кипения и замерзания разбавленных растворов нелетучих веществ.
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 449; Нарушение авторских прав?; Мы поможем в написании вашей работы!