
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Виды окислительно-восстановительного титрования
|
|
|
|
В ОВ титровании, как и в кислотно-основном титровании, применяют прямое, обратное и заместительное титрирование. Наиболее точные результаты получают, при прочих равных условиях, при прямом титровании.
В расчетах результатов ОВ титрования молярную массу эквивалента реагирующего вещества А (окислителя или восстановителя) М(1/zА) и молярную концентрацию эквивалента с(1/z А) вычисляют, исходя из того, что в ОВ реакции величина z равна числу электронов n, принимающих участие в реакции т.е. разности степеней окисления окисленной и восстановленной форм данного вещества А:
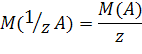
с(1/z А) = zc(A)
где М(А) и с(А) - соответственно молярная масса и молярная концентрация вещества А.
Прямое ОВ титрование проводят тогда, когда ОВ реакция удовлетворяет требованиям, перечисленным выше. Например, определение железа(II) прямым перманганатометрическим титрованием по схеме
5Fe2+ + MnO4- + 8H+ = Mn2+ + 5Fe3+ + 4H2O
Обратное ОВ титрование проводят тогда, когда применение прямого титрования нецелесообразно по тем или иным причинам.
К аликвоте анализируемого раствора, содержащего определяемый компонент X, прибавляют точно известное количество вещества А, взятого в избытке по сравнению с его стехиометрическим количеством, и выдерживают раствор некоторое время для обеспечения полноты протекания реакции между X и А. Непрореагировавший избыток вещества А оттитровывают стандартным раствором титранта Т.
Так, например, при иодиметрическом определении сульфид-иона к аликвоте анализируемого раствора, содержащего сульфид-ионы, прибавляют в избытке точно известное количество раствора иода. Протекает реакция
S2- + I2 = S + 2I-
Непрореагировавший избыток иода оттитровывают стандартным раствором тиосульфата натрия:
2Na2S2O3 + I2 = Na2S4O6 + 2NaI
Заместительное ОВ титрование применяют для определения веществ как вступающих, так и не вступающих в ОВ реакции.
Так, при иодометрическом определении пероксида водорода к аликвоте анализируемого раствора, содержащего определяемый пероксид водорода в серно-кислой среде, прибавляют избыточное по сравнении со стехиометрическим количество иодида калия. При этом протекает реакция с образованием иода:
Н2О2 + 2I- + 2H+ = I2 + 2H2O
Выделившийся иод (заместитель) в количестве, эквивалентном количеству пероксида водорода в аликвоте, оттитровывают стандартным раствором тиосульфата натрия:
2 Na2S2O3 + I2 = Na2S4O6 + 2NaI
Расчеты проводят так же как и при прямом титровании, исходя из закона эквивалентов.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2314; Нарушение авторских прав?; Мы поможем в написании вашей работы!