
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Иодатометрия
|
|
|
|
Иодатометрия, или йодатометрическое титрование - это определение различных восстановителей титрованием раствором иодата калия KIO3. Метод –фармакопейный.
Сущность метода. В основе метода лежит полуреакция (1):
IO3- +6e + 6H+ = I- + 3H2O (1)
Стандартный OB потенциал редокс-пары IO3-,Н+|I- при комнатной температуре равен 1,08 В. т.е. имеет довольно высокое значение.
В соответствии с полуреакцией (1) число электронов, принимающих участие в этой полуреакции, равно n = 6; фактор эквивалентности для иодат-иона в подобных ОВ процессах равен 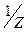 =
= 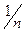 = 1/6. Молярная масса эквивалента иодата калия равна
= 1/6. Молярная масса эквивалента иодата калия равна
М(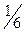 KIO3) = М(KIO3)/6 = 35,6668 г/моль.
KIO3) = М(KIO3)/6 = 35,6668 г/моль.
Молярная концентрация с(KIO3) и молярная концентрация эквивалента с(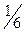 KIO3) связаны соотношением
KIO3) связаны соотношением
с(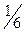 KIO3) = 6с(KIO3)
KIO3) = 6с(KIO3)
Иодат-ион способен в кислой среде, в зависимости от условий, восстанавливаться также до иода в соответствии с полуреакцией
IO3- +5e + 6H+ = 0,5I2 + 3H2O
Стандартный ОВ потенциал редокс-пары IO3-,Н+|I2 при комнатной температуре равен 1,195 В.
Титрант метода. В качестве титранта метода применяют водный раствор иодата калия KIO3 обычно с молярной концентрацией эквивалента 0,1 моль/л.
Титрант можно готовить по точной навеске иодата калия высокой степени чистоты (обычно химически чистого, «х.ч.»).
Стандартные растворы иодата калия хранят в сосудах из темного
стекла с притертыми пробками, в темном месте.
Индикаторы метода. В иодатометрии при визуальном определении
КТТ используют либо свежеприготовленный 1%-ный раствор крахмала либо не смешивающиеся с водой органические экстрагенты - хлороформ, тетрахлорид углерода, способные экстрагировать иод из водной фазы, окрашиваясь при этом в фиолетовый цвет. При 1 избыточной капле KIO3 выделяется I2, крахмал синеет.
6H+ + I- + IO3- = I2 + 3H2O
2I- - 2e = I2
2I+5 + 10e = I2
В качестве индикаторов используют и некоторые красители.
Применение иодатометрии. Методом иодатометрического титрования определяют различные вещества, обладающие восстановительными свойствами, например олово(II), сурьму(III), мышьяк(III), Hg22+, железо(II), иодиды, сульфиты, тиосульфаты, тиоцианаты, аскорбиновую кислоту, гидразин, гидразид изоникотиновой кислоты и др.
Способом обратного титрования, с иодатометрическим окончанием.
можно определять и окислители, такие; как PbO2, MnO2, пероксиды водорода и бария и т.п.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 6459; Нарушение авторских прав?; Мы поможем в написании вашей работы!