
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кристаллические и аморфные твердые тела. Кристаллическая решетка
|
|
|
|
Зонная теория твердых тел
ЛЕКЦИЯ 27
Твердыми телами называются тела, характеризующиеся постоянством формы и объема, причем тепловые движения частиц в них представляю собой хаотические колебания частиц относительно положений равновесия.
Выделяют кристаллические и аморфные твердые тела.
Кристаллические тела – это твердые тела, имеющие упорядоченное расположение частиц (атомов, молекул), которое периодически повторяется.
Характерным признаком кристаллических тел является кристаллическая решетка.
Кристаллическая решетка – это структура, для которой характерным является регулярное расположение частиц с периодической повторяемостью в трех измерениях.
Кристаллы ограничены упорядоченно расположенными друг относительно друга плоскими гранями, которые сходятся в ребрах и вершинах. У злами кристаллических решеток называются точки, в которых расположены частицы, а точнее – точки, относительно которых частицы в твердых телах совершают колебания.
Крупные одиночные кристаллы, имеющие форму правильных многогранников, называются монокристаллами. Их форма оперделяется химическим составом кристалла. Поликристаллы имеют мелкокристаллическую структуру – состоят из большого числа срощенных мелких, хаотично расположенных кристаллов (кристаллические зерна, кристаллити).
Аморфные тела – это твердые тела, физические свойства которых одинаковы по всем направлениям (наблюдается изотропия свойств). Для них, как и для жидкостей, характерен ближний порядок в расположении частиц; у них в отличие от жидкостей подвижность частиц достаточно мала. Аморфные твердые тела (смола, стекло и др..) являются переохолажденными жидкостями и не имеют четко выраженных свойств кристаллов.
Особенностью аморфных тел является отсутствие у них определенной точки плавления, то есть невозможно указать определенную температуру, выше которой можно было бы констатовать жидкое состояние, а ниже – твердое. Их опыта известно, что в аморфных телах со временем может наблюдаться процесс кристаллизации, например в стекле появляются кристаллы; оно, теряя пластичность, начинает мутнеть и превращается в поликристаллическое тело.
В дальнейшем будем рассматривать только кристаллические твердые тела.
2. Виды кристаллических связей
Кристаллы классифицируют по кристаллографическим и по физическим признакам.
1. Кристаллографический признак осуществляется только по пространственной периодичности в расположении частиц (частицы поэтому рассматривают как геометрические точки).
Кристаллические решетки когут кметь разные виды симметрии.
Симметрия кристаллических решеток проявляется в их свойстве объединяться друг с другом при некоторых перемещениях, например, при параллельном переносе, поворотах, отображении или их комбинациях. Кристаллическим решеткам свойственны 230 комбинаций элементов симметрии, или 230 разных пространственных групп. С переносной симметрией в трехмерном просторанстве связано понятие трехмерной периодической структуры – пространственной решетки (решетки Браве). Любые пространственные решетки могут быть составлены повторением в трех разных направлениях одного и того же структурного элемента. Всего существует 14 типов решеток Браве, отличающихся по виду переносной симметрии. Они распределяются по семи кристаллографическим системам или сингониям, таким как трехклинная, моноклинная, ромбическая, тетрагональная, ромбоэдрическая (тригональная), гексагональная, кубическая.
2. Физический признак осуществляется по природе частиц, расположенных в узлах решетки, и по характеру сил взаимодействия между ними.
Типы кристаллов по физическому признаку такие:
1) Ионные кристаллы. В узлах кристаллических решеток по порядку располагаются ионы противоположного знака (типичные представители – NaCl (структура изображена на рис. 27.1), углекислый кальций и другие соли). Связь, обусловленная кулоновскими силами притяжения между разноименно заряженными ионами, называется ионной. Здесь нельзя выделить отдельные молекулы: кристалл является как бы одной гигантской молекулой.
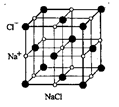
Рис. 27.1
2) Атомные кристаллы. В узлах кристаллических решеток располагаются нейтральные атомы, удерживающиеся в узлах ковалентными связями квантово-механического происхождения (у соседних атомов коллективизированы валентные электроны, слабо связанные с атомом). Типичные представители: алмаз, графит, германий и т.д. Структура решетки алмаза приведена на рис. 27.2.
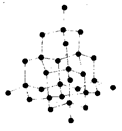
Рис. 27.2
3) Металлические кристаллы (Na, А1 и др.). В узлах кристаллических решеток располагаются положительные ионы металла. При образовании кристаллической решетки валентные электроны, слабо связанные с атомами, отрываются от атомов и коллективизируются: они уже принадлежат не одному атому, как в случае ионной связи, и не паре соседних атомов, как при ковалентной, а всему кристаллу в целом.
4) Молекулярные кристаллы. В вузлах кристаллических решеток располагаются нейтральные молекулы вещества, силы взаимодействия между которыми обусловлены незнаительным взаимным сдвигом электронов в электронных оболочках атомов. Эти силы называют ван-дер-ваальсовскими, поскольку они имеют ту же природу, что и силы притяжения между молекулами, приводящие к отклонению газов от идеальности.
Характерной особенностью монокристаллов является их анизотропия – зависимость физических свойств твердых тел (тепловых, упругих, электрических, оптических) от направлений в кристалле.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 5082; Нарушение авторских прав?; Мы поможем в написании вашей работы!