
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Метод валентных связей
|
|
|
|
Метод валентных связей:
1.Связь образуется электронами с антипараллельными спинами.
2.Хим. связь всегда направлена в сторону максимального перекрывания электронных плотностей.
МВС (локализованных электронных пар) исходит из положения, что каждая пара атомов в молекуле удерживается вместе при помощи 1 или нескольких общих электронных пар. Т.е. в представлении МВС хим. связь локализована между двумя атомами, т.е. она двуцентровая и двухэлектронная.
Сила взаимодействия между электроном и ядром атома Н2 составляет 1030 эр/с. Встает вопрос, почему электрон не падает на ядро и атомная система стабильная. Объяснением служит 2 тезиса:
1) атом Н2 вращается по электронной обитали с определенной скоростью, усиливает эффекты отталкивания от ядра и этим можно объяснить устойчивость системы. 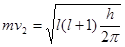 Однако в стационарном состоянии скорость движения электрона=0.
Однако в стационарном состоянии скорость движения электрона=0.
2)электрон падает на ядро и благодаря волновым свойствам удерживает систему в устойчивом состоянии. Однако этот процесс возможен в нейтронах звезд
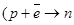
Единственным тезисом, который может объяснить причину устойчивости атома водорода является следующий: электрон стремится как можно занять больший объем. ΨH=ΨE
Сокращенное уравнение Шредингера для атома Н2.Для рациональных способов решения уравнение Шредингера. От декартовых координат перешли к полярным координат r,Ө,μ разделили переменные величины и уравнение будет представлено в виде произведения 3х отдельных функций, каждая зависит от одного аргумента.
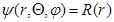 - рациональная волновая функция зависит от безразмерных величин n,e.
- рациональная волновая функция зависит от безразмерных величин n,e.
Ө(ө) Φ(φ) – сферические волновые функции зависят L, me,0.
Ур-е Шредингера в полярных координатах для атома Н2 решается в том случае, если безразмерная величина n принимает значение 1.2.3… ~, l, 0,1.2 до n-1 me +l, 0-l. Безразмерные величины были названы квантовыми числами.
Литература:
1. Ахметов, Н.С. Общая и неорганическая химия / Н.С.Ахметов. – 3-е изд. – М.: Высшая школа, 2000. – 743с.
- Т.Браун. Химия – в центре наук / Браун.Т, Лемей Г.Ю. – М.: Мир, 1983. – тт. 1–2.
- Карапетьянц М.Х. Общая и неорганическая химия / М.Х. Карапетьянц, С.И.Дракин. – М.: Высшая школа, 2002.
- Коровин Н.В. Общая химия / Н.В.Коровин. – М.: Высшая школа, 2006. – 557 с.
- Кузьменко Н.Е. Краткий курс химии / Н.Е. Кузьменко, В.В Еремин, В.А. Попков. – М.: Высшая школа, 2002. – 415 с.
- Зайцев, О.С. Общая химия. Строение веществ и химические реакции / О.С.Зайцев. – М.: Химия, 1990.
- Карапетьянц, М.Х. Строение вещества / М.Х. Карапетьянц, С.И.Дракин. – М.: Высшая школа, 1981.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 334; Нарушение авторских прав?; Мы поможем в написании вашей работы!