
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение конфтгурации полипептидов и белков
|
|
|
|
Здесь много методов их вариантов, но наиболее надежны данные, получаемые методом КД.
Возможности применения метода КД для исследования вторичной и третичной структуры белков основывается на следующих фактах и постулатах:
1. Рентгено-структурный анализ показал, что основными структурными элементами пептидной цепи являются три модельных структуры: α-спираль, β-структура с параллельными цепями и неупорядоченные участки в виде клубка (ρ-структура);
2.
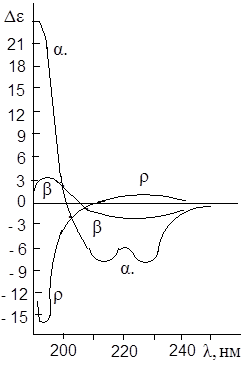 |

 Исследование спектров КД полипептидов с модельными структурами в области p p* и n p* переходов (195 – 240 нм) показало, что различные структуры имеют различные характеристические спектры:
Исследование спектров КД полипептидов с модельными структурами в области p p* и n p* переходов (195 – 240 нм) показало, что различные структуры имеют различные характеристические спектры:
3. Установлена корреляция между содержанием в одной молекуле белка трех модельных структур и его спектром КД. Вклады трех модельных структур в спектр считают аддитивными, поскольку они подчиняются уравнению:
Del = DeaРa + DebРb + DerРr,
где Dea, Deb и Der - соответственно круговой дихроизм чистых a, b и r
форм, Р – доля этих форм в структуре белка.
4. Считая, что наблюдаемый спектр КД белка определяется пропорциональными вкладами спектров КД трех модельных структур, определяют вклад этих структур и их %-ное содержание в белке.
Существует несколько методов расчетов содержания модельных структур в белке. Остановимся на наиболее удобном изодихроическом методе, основанном на определении кругового дихроизма при трех длинах волн для трех так называемых изодихроических точек, в которых пересекаются характеристические кривые спектров двух структурных форм (см. спектр, представленный в пункте 2).
Ниже в таблице представлены значения кругового дихроизма для изодихроических точек, по которым и проводят расчеты:
| Опреде- ляемая конфор- мация | l изодихроичес- кой точки, при которой проводят определение, нм | Del для измеряе- мой конформации | Del для изодихроических точек |
| a b r | 200,5 | Dea209= -9,39 ± 0,45 Deb202=2,02 ± 0,15 Der200,5= -2,02 ± 0,15 | Deb209=Der209= -0,85 ± 0,06 Dea202=Der202= -1,81 ± 0,15 Dea200,5=Deb200,5=2,57 ± 0,15 |
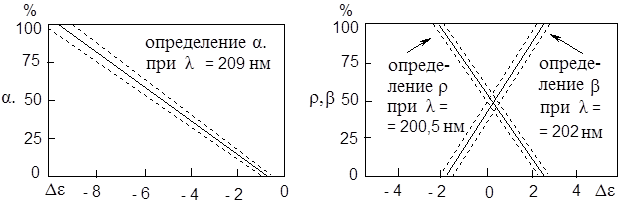 |
Для l изодихроических точек строится три калибровочных прямых, при помощи которых по значениям De для реальных структур рои этих длинах волн определяют % содержания каждой конформационной структуры:
. Можно также проводить расчеты по уравнениям:
%a = (De209 + 0,85)/(- 9,39 + 0,85);
%b = (De202 + 1,81)/(2,02 + 1,81);
%r = (De200,5 - 2,57)/(-2,02 -2,57).
Этот метод является самым доступным, быстрым и удобным, но в интервале l (200 – 210 нм) кривые КД сильно чувствительны к влиянию среды, к строению аминокислотных остатков (особенно ароматических). Разница в l очень небольшая, поэтому требуется очень высокая точность экспериментальных измерений спектров КД.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 413; Нарушение авторских прав?; Мы поможем в написании вашей работы!