
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнение Аррениуса
|
|
|
|
Вывести более точную зависимость V от Т можно с помощью уравнения изохоры или изобары химической реакции:
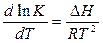
где 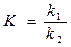 - константа химического равновесия,
- константа химического равновесия,
k1 и k2 – константы скорости в прямой и обратной реакции;
ΔН – теплота химической реакции;
Т - абсолютная температура;
R – универсальная газовая постоянная.
Подставим k1/k2 вместо К:
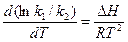
 ,
,
где ΔН = Е1 – Е2, тогда
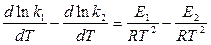
Можно считать, что правая и левая части равны попарно с точностью до величины В:

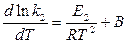
Экспериментально доказано, что В = 0. В общем виде уравнения можно записать:
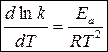 (дифференциальная форма)
(дифференциальная форма)
| (1) |
Это уравнение Аррениуса (характеризует зависимость скорости химической реакции от Т).
Величина Еа имеет размерность энергии (кДж/моль, ккал/моль) и называется энергией активации – это тот избыток энергии по сравнению со средней энергией молекул при данной Т, которой должны обладать частичка, чтобы вступить в элементарный химический акт.
Интегрируем уравнение (1):
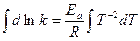
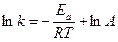 (интегральная форма)
(интегральная форма)
| (2) |
 где А – предэкспоненциальный множитель (характеризует число активных столкновений, приводящих к элементарному химическому акту).
где А – предэкспоненциальный множитель (характеризует число активных столкновений, приводящих к элементарному химическому акту).
Определение Еа при трех и более температурах (графический метод). Построим зависимость ln k от 1/T. Отрезок, отсекаемый на оси Оу, равен ln A при 1/Т = 0; тангенс угла наклона равен:
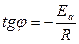
Отсюда найдем величину Еа. Потенцируем уравнение (2):
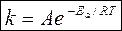
(экспоненциальная форма)
Зная величину Eа, определенную из зависимости ln k от 1/Т, из этой зависимости можно определить предэкспоненциальный множитель А:
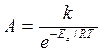
Видно, что чем больше Еа, при данном А, тем меньше скорость химической реакции.
Определение Еа при двух температурах (аналитический метод).
Проинтегрируем уравнение Аррениуса в пределах от Т1 до Т2:
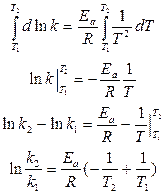
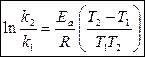
где k1 – константа скорости при температуре Т1, k2 – при Т2.
Зная величину k1 при температуре Т1, можно определить k2 при Т2.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 1345; Нарушение авторских прав?; Мы поможем в написании вашей работы!