КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнение для процесса катодного перенапряжения
|
Формула Тафеля
Разряд ионов гидроксония, приводящий к выделению молекул Н2, является одним из важнейших электрохимических процессов, который во-первых, сопровождает многие электрохимические реакции, во-вторых, является источником получения молекул Н2 и, в-третьих, этот процесс наиболее простой и наиболее изученный.
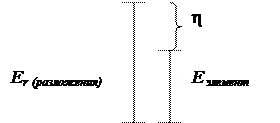
Выделение молекул Н2 на катоде сопровождается некоторым перенапряжением. Водородное перенапряжение представляет собой тот избыток напряжения, который необходимо приложить к элементу сверх его э.д.с., чтобы начался процесс выделения Н2.
Водородное перенапряжение замедляет процесс выделения Н2 и приводит к непродуктивному расходованию электрического тока.
Поэтому водородное перенапряжение стремятся устранить или хотя бы уменьшить.
Причиной водородного перенапряжения является замедленность одной из стадий сложного электрохимического процесса восстановления ионов Н3О+ до молекулы Н2
Известно, что сам процесс состоит из следующих стадий:
(-) Pt | HCl, aq | Pt (+)
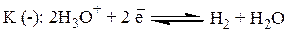
суммарный процесс
Стадии процесса разряда ионов Н3О+ до Н2:
1) Диффузионная стадия – представляет собой быструю доставку Н3О+ к поверхности электрода за счет диффузии
2) Стадия дегидратации – в ионе Н3О+ протон связан с молекулой Н2О и разряд иона Н3О+ невозможен без предварительной дегидратации.

3) Стадия разряда и адсорбции протона Н – представляет собой собственно электрохимическую реакцию. Образовавшиеся атомы Н одновременно адсорбируются металлом электрода.
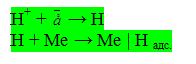
Иногда стадия 2 и 3 совмещаются в одном акте – разрядка ионов Н3О+.
 4) Стадия ионизации или рекомбинации – после насыщения поверхности электрода Н адс. ионизуется и переходит в раствор.
4) Стадия ионизации или рекомбинации – после насыщения поверхности электрода Н адс. ионизуется и переходит в раствор.
5) Стадия выделения газа: образовавшиеся молекулы Н2 перемещают раствор и выделяется в виде пузырьков газа.
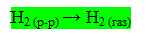
Замедление любой из вышеперечисленных стадий приводит к появлению перенапряжения. Величина перенапряжения направлена на ускорение самой медленной стадии электрохимического процесса.
Было выдвинуто много теорий относительно того как происходит процесс восстановления Н2 и какая из стадий является самой медленной и определяет скорость процесса в целом. Справедливость той или ионной теории ВП определяется возможностью с помощью данной теории объяснить и как можно точнее вывести формулу Тафеля.
Наиболее известны и признаны следующие две теории.
| Рекомбинационная теория (Тафель) | Теория медленного разряда иона (Смитс) |
| 1. Какова лимитирующая стадия? | |
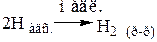 стадия рекомбинации
стадия рекомбинации
| 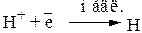 стадия разряда иона
стадия разряда иона
|
| 2. Какой вид имеет формула Тафеля выведенная с помощью теории? | |
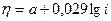 (величина
(величина 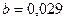 , а не 0,016, т.е. в 4 раза меньше. Тафель не учел неоднородность поверхности Ме и наличия сил отталкивания между адсорбированными атомами. Т. е. основной недостаток малое значение b. , а не 0,016, т.е. в 4 раза меньше. Тафель не учел неоднородность поверхности Ме и наличия сил отталкивания между адсорбированными атомами. Т. е. основной недостаток малое значение b.
|
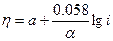 если
если 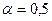 , то , то
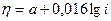 Величина b правильная, что является основным достоинством данной теории.
Величина b правильная, что является основным достоинством данной теории.
|
| 3. Для каких электродов применима данная теория? | |
| Металлы с малым перенапряжением – Pt, Ni | Металлы с большим перенапряжением – Hg, Pb |
|
|
Дата добавления: 2014-01-07; Просмотров: 774; Нарушение авторских прав?; Мы поможем в написании вашей работы!