
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пластидні пігменти – хлорофіли, каротиноїди, фікобіліни
|
|
|
|
Фотосинтез.
Загальне рівняння фотосинтезу.
Процес фотосинтезу виражають сумарним рівнянням:
світло
СО2 + Н2О → {СН2 О} + О2,
хлорофіл
у якому виражена суть явища, що складається в тому, що на світлі в зеленій рослині із гранично окислених речовин – діоксиду вуглецю й води утворюються органічні речовини й вивільняється молекулярний кисень. Фотосинтез - це процес трансформації поглиненої енергії світла в хімічну енергію органічних сполук. Причому в процесі фотосинтезу відновлюються не тільки СО2, але й нітрати або сульфати, а енергія може бути спрямована на різні ендергонічні процеси, у тому числі на транспорт речовин.
У процесі еволюції рослин сформувався спеціалізований орган фотосинтезу – листок. У середньому листи поглинають 80-85% енергії фотосинтетично активної радіації (ФАР), що є видимою частиною спектру електромагнітного випромінювання з довжиною хвилі 400-700 нм, і 25% енергії інфрачервоних променів, що складає близько 55% енергії загальної радіації, або 16,5105 Дж/(м2-ч).
Листок відбиває 10% ФАР і 45% інфрачервоних променів і пропускає відповідно 5 і 30%. На фотосинтез використається 1,5-2% поглиненої синтетично активної радіації, інша поглинена енергія витрачається в основному на випаровування води – транспірацію (95-98%), можливий також і теплообмін з атмосферою.
Листкова поверхня досягає значних розмірів і перевершує площа ґрунту, що займає рослина. Для характеристики розмірів фотосинтетичного апарата використають індекс листової поверхні (L), що розраховують як площа листів (м2), що доводиться на 1 м2 ґрунту. Для сільськогосподарських рослин помірної зони середні значення листового індексу 3-5, у південних широтах з вологим кліматом до 8-10. Наприклад, поверхня листів 1 га посівів зернових культур у фазі цвітіння досягає 20-40 тис. м2, у низькорослих яблунь під час вегетації площа листків становить 25- 30 тис. м2/га.
Фотосинтез пов'язаний з вибірковим поглинанням пігментами світла у видимій частині сонячного спектра. Фотосинтетичні пігменти становлять 10-15% сухої маси хлоропластів. По хімічній природі діляться на дві групи – хлорофіли та каротиноїди.
Хлорофіли. Хлоропласти вищих рослин містять хлорофіл а й хлорофіл б. Вони були ідентифіковані російським вченим М.С. Цвєтом (1906 р.) за допомогою розробленого їм методу хроматографії. Структурна формула хлорофілу, запропонована Г. Фішером (1939 р.), одержала остаточне підтвердження в I960 р. у результаті двох незалежно проведених робіт у США й ФРН по штучному синтезу хлорофілу а.
Хлорофіл – складний ефір дикарбонової кислоти хлорофіліна, у якої одна карбоксильна група етерифікована залишком метилового спирту (СН3ОН), а інша - залишком одноатомного неорганічного спирту фітолу (С20Н39ОН):
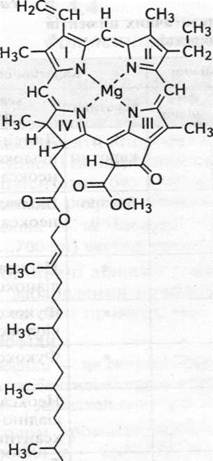 На малюнку наведена структурна формула хлорофілу а. Чотири пірольних кільця (I—IV) з'єднані між собою метиновими містками, які утворюють порфіринове ядро. Атоми азоту пірольних кілець чотирма координаційними зв'язками взаємодіють із атомом Mg. У структурі порфіринового ядра є також циклопентанове кільце, що містить хімічно активну карбонільну групу. Структура, що складається з тетрапірольного й циклопентанового кілець, одержала назву форбіна.
На малюнку наведена структурна формула хлорофілу а. Чотири пірольних кільця (I—IV) з'єднані між собою метиновими містками, які утворюють порфіринове ядро. Атоми азоту пірольних кілець чотирма координаційними зв'язками взаємодіють із атомом Mg. У структурі порфіринового ядра є також циклопентанове кільце, що містить хімічно активну карбонільну групу. Структура, що складається з тетрапірольного й циклопентанового кілець, одержала назву форбіна.
Порфиринове кільце – це система з дев'яти пар подвійних й одинарних, тобто кон‘югованих зв'язків, які чергуються з 18 делокалізованими π-електронами. Хлорофіл b відрізняється від хлорофілу а тим, що у третього вуглецю другого пірольного кільця замість метильної знаходиться альдегідна група. Структура хлорофілу, позбавлена фітолу, називається хлорофілідом. При заміщенні атома магнію протонами водню утворюється феофітин.
Оптичні властивості. Відмінною рисою всіх пігментів є наявність в їхньому складі системи слабко утримуваних делокалізованих електронів, що порушуються квантами видимої частини сонячного спектра. Це лежить в основі їхньої властивості – вибіркового поглинання світла. Різко виражені максимуми поглинання хлорофілів перебувають у синьо-фіолетовій і червоній частинах спектра. Максимуми поглинання розчину хлорофілу а в етиловому спирті – 428-430 й 660-663 нм відповідно, хлорофілу b – 452-455 й 642-644 нм. Хлорофіли дуже слабко поглинають жовтогарячі й жовті промені й зовсім не поглинають зелені й інфрачервоні. Тому розчин хлорофілу а має зелений або синьо-зелений колір, хлорофілу b – жовто-зелений.
Поглинання в синьо-фіолетовій частині спектра обумовлено системою кон‘югованих 9 пар одинарних і подвійних зв'язків порфиринового ядра молекули хлорофілу з 18 делокалізованими π-електронами, які збуджуються квантами з енергією 4,5x10-19 Дж, що відповідає цим променям. Поглинання в червоній області спектра (енергія кванта 3x10-19 Дж) пов'язане з гідруванням подвійного зв'язку у С7-С8 в IV пірольному кільці, присутністю магнію в порфириновому ядрі й наявністю циклопентанового кільця (V). Саме ці особливості структури сприяють зниженню поглинання в жовтій і зеленій частинах спектра.
В хлорофілу b, що відрізняється від хлорофілу а заміною метильної групи на альдегідну, максимуми поглинання світла виявляються більше зближеними за рахунок зсуву синьо-фіолетового в довгохвильову, а червоного – у короткохвильову області. Крім того, хлорофіл b більш повно використовує синьо-фіолетове світло, ніж хлорофіл а; у червоних променях переваги має хлорофіл а.
Розчин хлорофілу має яскраву червону-вишнево-червону флуоресценцію – випромінюванням поглинених квантів світла. Відповідно до правила Стокса флуоресценція зрушена в більше довгохвильову частину в порівнянні з поглинанням світла, максимум флуоресценції 650-668 нм. Хлорофіл у живому листі флуоресціює слабко. Це пов'язане з тим, що енергія поглинених квантів в основному перетворюється в хімічну, причому за інтенсивністю флуоресценції листка можна судити про ефективність фотосинтезу. Чим інтенсивніше флуоресценція, тим нижче ККД використання поглиненої енергії.
Як відомо, світло має водночас хвильові й корпускулярні властивості, тобто поширюється як хвиля та поглинається квантами, або фотонами. Поглинання кванта світла супроводжується переходом у багатший енергією короткоживучий збуджений стан, пов'язаний з переходом електрона на більш віддалену від ядра орбіталь. Електронні орбіталі атомів характеризуються певними енергетичними рівнями, що зростають по мірі видалення від ядра. Ті кванти світла, енергія яких відповідає різниці енергій між двома орбіталями, поглинаються з переходом електрона на більше далеку орбіталь. Тому можуть поглинатися тільки кванти світла із зовсім певною довжиною хвилі.
В органічних молекулах майже всі електрони спарені, тобто перебувають у тому самому енергетичному стані, маючи протилежні спини (основний синглетний енергетичний стан – Sо). Поглинання молекулою хлорофілу кванта червоного світла з енергією 170 кДж/моль призводить до першого синглетного електроно-збудженого стану – S1 час існування якого приблизно 10-9 с. Збуджена молекула хлорофілу переходить у стабільний стан шляхом повернення електрона на вихідну орбіталь. Поглинена енергія при цьому може витрачатися різними способами: розсіюванням теплоти; втратою у вигляді випромінювання; збудженням сусідніх молекул пігментів (перенесення енергії до фотохімічних центрів); здійсненням фотохімічної роботи. Можливі також втрата частини енергії у вигляді теплоти й перехід молекули із синглетного в метастабільний триплетний збуджений стан (з оберненням спіна електрона). Триплетний стан триває набагато довше (> 10-4 с). Із триплетного стану молекула може повернутися в основний за рахунок більш тривалого, ніж флуоресценція, слабкого довгохвильового світіння – фосфоресценції або направивши енергію на фотохімічні реакції.
Поглинання кванта в синьо-фіолетовій області спектра (вміст енергії 300 кДж/моль квантів) приводить до виникнення винятково короткого (< 10-12) другого збудженого синглетного стану (S2). За рахунок виділення частини енергії у вигляді теплоти молекула переходить в S1 і подальші події відповідають збудженню червоним світлом. Тому поглинання світла в синій і червоній областях дає однаковий спектр флуоресценції (червоний), а також рівні кількості фотохімічної роботи, незважаючи на неоднаковий зміст енергії поглинених квантів.
Таким чином, молекула хлорофілу завдяки структурним змінам і фізико-хімічним особливостям здатна виконувати три найважливіші функції: вибірково поглинати енергію світла; трансформувати її в енергію електронного збудження (або запасати її у вигляді енергії електронного збудження); фотохімічно перетворити енергію збудженого стану в хімічну енергію. Для функціонування молекули хлорофілу істотне значення має її просторова організація. Магній-порфиринове кільце молекули являє собою майже плоску пластинку товщиною 0,42 нм і площею 1 нм2. Це гідрофільна фотоактивна частина молекули хлорофілу. Довгий (2 нм) аліфатичний залишок фітолу, що утворює кут з порфіриновим кільцем, – її гідрофобний полюс, необхідний для взаємодії молекули хлорофілу з гідрофобними ділянками мембранних білків і ліпідів.
Каротиноїди. Це жиророзчинні пігменти жовтого, яскраво жовтого й червоного кольорів. Вони входять до складу хлоропластів і хромопластів зелених частин рослин (квіток, плодів, коренеплодів). У не зелених листках їхній колір маскується хлорофілом.
Структура й властивості. Каротиноїди є тетратерпеноїдами (8 залишків ізопрену, С40). Каротиноїди можуть бути ациклічними (аліфатичними), моно- і біциклічними. Цикли на кінцях молекул каротиноїдів - похідні іонона. Каротини являють собою вуглеводні з формулою С40Н56. У хлоропластах вищих рослин містяться α- і ß-каротини. ß-каротин має два ß-іононових кільця (подвійний зв'язок між С5 і С6). При гідролізі ß-каротину по центральному подвійному зв'язку утворюються дві молекули вітаміну А (ретинолу). α-каротин відрізняється від ß -каротину тим, що в нього одне кільце (ß -іононове, а друге ε-іононове - подвійний зв'язок між С4 й C5).
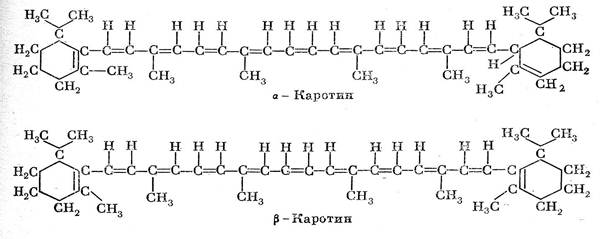
Ксантофіли є кисневмісними похідними каротину. Ксантофіл лютеїн — похідне α-каротину, а зеаксантин – ß-каротину. Вони мають по одній гідроксильній групі в кожному іононовому кільці – С40Н56О2. Додаткове включення в молекулу зеаксантина двох атомів кисню по подвійних зв'язках С5-С6 (епоксидні групи) призводить до утворення віолаксантина (С40Н56О4), при включенні епоксидних груп у лютеїн утворюється неоксантин. Синтез каротиноїдів починається з ацетил~SKoА через мевалонову кислоту до лікопіна – ациклічного каротину, що є попередником всіх інших каротиноїдів. Спектри поглинання каротиноїдів характеризується двома смугами у фіолетово-синій і синій частинах спектра від 400 до 500 нм і визначаються системою кон‘югованих зв'язків. При збільшенні числа таких зв'язків максимуми поглинання зміщаються в довгохвильову частину спектра. Подібно хлорофілам, каротиноїди нековалентно пов'язані з білками й липоїдами мембран і тилакоїдів.
Фізіологічна роль каротиноїдів. Каротиноїди є обов'язковими компонентами пігментних систем. Вони виконують роль додаткових пігментів, які передають енергію поглинених квантів хлорофілу а для здійснення фотохімічної роботи. Особливо зростає їхнє значення як світловловлюючих систем у синьо-фіолетовій і синій частинах спектра у затінках, тобто коли переважає розсіяна радіація.
Є докази, що каротиноїди виконують захисну функцію, запобігаючи фотоокисленню хлорофілу.
Висловлюється також припущення про пряму участь каротиноїдів у розщепленні води й кисневому обміні при фотосинтезі.
У верхівках пагонів рослин каротиноїди забезпечують визначення напрямку світла і їхню орієнтацію до світлового потоку за рахунок фототропізму.
Фікобіліни. Характерні пігменти синьо-зелених, червоних та деяких інших водоростей, які вони містять окрім хлорофілів. Цю назву вони одержали завдяки своїй подібності до тваринних пігментів – білірубінів.
За хімічною будовою біліни – тетрапіроли з відкритим ланцюгом, без металу. Як і хлорофіли, фікобіліни - тетрапіроли, але чотири залишки піролу в них створюють незамкнутий витягнутий або згорнутий ланцюг.
Хромофорною групою фікоціанів (С34Н42О9) є фікоціанобілін, фікоеретринів (С34Н47О8) – фікоеритробілін. Фікоеритробілін у сполученні з білком називають фікоеритрином. Він добре поглинає кванти зеленої частини спектра. Вони трапляються переважно у червоних водоростей і визначають їхнє забарвлення, мають максимуми поглинання 500-568 нм.
Фікоціаніни характерні для синьо-зелених водоростей і максимуми поглинання дещо в довгохвильову область — від 585 до 630 нм.
До фікобілінів належать також алофікоціаніни – пігменти з максимумами поглинання від 585 до 650 нм, хромофорну групу їх не визначено. Цю назву алофікоціаніни одержали тому, що спочатку їх приймали за одну з форм фікоціаніну.
Алофікоціанін характерний для синьозелених, хоча трапляється також у червоних і криптомонадових водоростей. Фікобіліни концентруються або в стромі, або формують особливі впорядковані ансамблі на поверхні мембран – фікобілісоми. Пігменти даної групи виконують функцію світлозбиральної антени та забезпечують передачу поглинутої ними енергії сонячного світла до хлорофілів а.
Наявність фікобілінів дає змогу водоростям у процесі фотосинтезу використовувати промені, які проникають на певну глибину та займати відповідні екологічні ніші.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 12126; Нарушение авторских прав?; Мы поможем в написании вашей работы!