
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Локальная формулировка второго начала термодинамики
|
|
|
|
Рассмотрим неравновесную систему, для каждого физически бесконечно малого элемента которой, определено значение плотности энтропии (6.1.3). В пределах каждого такого элемента выполняется условие детального равновесия, т.е. в каждой такой области энтропию можно определить термодинамически, через приведенное количество теплоты:
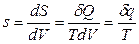 , (6.2.1)
, (6.2.1)
где Т – температура, характеризующая объем 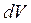 , а
, а 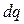 - плотность количества теплоты.
- плотность количества теплоты.
Приращение плотности энтропии, аналогично приращению любой величины (например, плотности энергии (6.1.10)) можно разбить на две составляющие: 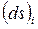 - приращение плотности энтропии, обусловленное процессами внутри системы и
- приращение плотности энтропии, обусловленное процессами внутри системы и 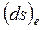 - приращение, обусловленное процессами в окружающей систему среде:
- приращение, обусловленное процессами в окружающей систему среде:
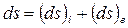 (6.2.2).
(6.2.2).
По аналогии с рассмотрением плотности потока энергии, можно заключить, что скорость изменения плотности энтропии, обусловленная внешними процессами, равна дивергенции потока энтропии, взятой с обратным знаком:
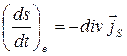 . (6.2.3)
. (6.2.3)
Об отличии или равенстве нулю производства энтропии в каждой точке системы (т.е. обусловленное процессами внутри системы) ничего определенного в общем случае сказать пока нельзя. Однако рассмотрев изменение энтропии в частных неравновесных процесса (например стационарном процессе теплопроводности) можно прийти к выводу что энтропия в каждой точке будет увеличиваться.:
Таким образом, в выражении (6.2.2) оба слагаемых отличны от нуля. И второе начало линейной термодинамики в локальной форме для рассматриваемого случая приобретает вид:
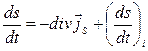 (6.2.10)
(6.2.10)
Второе начало в виде (6.2.10) справедливо для неравновесной системы (не обменивающейся частицами), в которой коэффициенты переноса остаются постоянными. В таких условиях второе начало формулируется в виде: скорость изменения плотности энтропии равна сумме дивергенции потока энтропии, взятой с обратным знаком и скорости производства энтропии в данной точке системы.
На основе второго начала равновесной термодинамики получен критерий эволюции изолированных систем. Аналогично существует критерий эволюции систем в неравновесной термодинамике. Сейчас нам уже известно, что системы, не слишком удаленные от равновесия, при неизменных внешних условиях, переходят в стационарное состояние. Как при этом изменяется скорость производства плотности энтропии? Ответ на этот вопрос дает критерий эволюции Пригожина: процессы в системах, не слишком далеких от равновесия идут таким образом, что скорость производства плотности энтропии, в каждой точке системы, стремится к минимальной из всех возможных.
Этот вывод получен в научной школе И. Пригожина на основе анализа соотношений Онзагера, который занимался разработкой неравновесной термодинамики. За свои работы по неравновесной термодинамике в 1968 году Л. Онзагеру присуждена Нобелевская премия.
.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 325; Нарушение авторских прав?; Мы поможем в написании вашей работы!