
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Первое начало (закон) термодинамики
|
|
|
|
Первый закон термодинамики сформулирован на основе огромного числа наблюдений и опытных фактов и является частным случаем закона сохранения и превращения энергии преминительно к термодинамическим процессам. Большая заслуга в установлении этого закона пренадлежит Майеру (нем. врач), Геймгольцу (нем. физик) и Джоулю (англ. физик) они независимо друг от друга пришли к установлению этого закона в 40-х годах 19 века.
Ими был установлен механический эквивалент теплоты, т.е. определено кол-во тепла, выделяемое в системе при совершении работы.
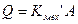 или
или 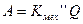
Раньше работу и теплоту измеряли разными единицами, в частности теплоту измеряли в калориях. 1 кал – это кол-во тепла необходимое для нагревания 1 г чистой дистиллированной воды при температуре 4 оС на 1 оС.
1 кал= 1,185 Дж.
Если количества теплоты и работу измерять в одних еденицах, например в Дж, как это сделано в системе СИ, то механический эквивалент теплоты будет равен единице
.
1-й закон термодинамики можно сформулировать по разному, но суть при этом останется одна и та же.
Различные формулировки первого закона термодинамики:
1. dQ=dU+dA или Q= U2-U1 +A
Кол-во тепла подведенное к системе идет на увеличение ее внутренней энергии и на совершение работы системы над внешними телами
2. dU=dQ+dA’ или U2-U1 =Q+A’
Изменение внутренней энергии системы равно количеству тепла подведенного к системе и работе совершенной внешними телами над системой
3. dA=dQ-dU или A= Q + (U1-U2)
Работа совершаемая системой, происходит за счет подводимого тепла и убыли внутренней энергии системы.
4. Если система участвует в круговом процессе, то за цикл U2-U1 = 0 т.к. внутренняя энергия является функцией состояния.
Раз изменение внутренней энергии за цикл равно нулю, то работа совершаемая системой за цикл равна количеству подведенного тепла A=Q за цикл.
Четвертая формулировка следующая: Не возможен «Перпетум мобеле» первого рода, т.е. периодически действующий тепловой двигатель, который бы совершал работу больше чем количество тепла полученное из вне.
Первый закон термодинамики подтверждается многочисленными наблюдениями, и применим не только к физическим процессам, но и к другим химическим, биологическим. Фактически он является критерием достоверности той или иной гипотезы.
Мы уже отмечали что внутренняя энергия системы однозначно определяет состояние системы, т.е внутренняя энергия является функцией состояния. Ее изменение не зависит каким образом система перешла из одного состояние в другое.
 А вот работа, совершаемое системой при переходе из одного состояние в другое, зависит от того каким образом система осуществляет этот переход
А вот работа, совершаемое системой при переходе из одного состояние в другое, зависит от того каким образом система осуществляет этот переход
= A1a2 > A1b2
Т.е работа является функцией процесса. А т.к
Q= ∆U +A то и теплота полученная системой является функцией процесса.
Когда эту разницу хотят подчеркнуть то для б.м приращений этих величин(функций) используют различные значки Для функций состояния dU, а для функций процесса dA и dQ (читается дельта)
С учетом сказанного 1-й закон термодинамики запишится в виде:
1. dQ=dU+ddA
2. dU=dQ+dA’
3. dA=dQ-dU
Формулировки останутся прежними.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 472; Нарушение авторских прав?; Мы поможем в написании вашей работы!