
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электроды второго рода
|
|
|
|
Электроды второго рода представляют собой полуэлементы, состоящие из металла, покрытого слоем его труднорастворимого соединения (соли, оксида, гидроксида) и погруженного в раствор, содержащий тот же анион, что и труднорастворимое соединение электродного металла. Схематически электрод второго рода можно представить как A n – êMA êM, а протекающую в нем реакцию
MA + ne = M + A n –;
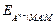 =
= 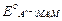 + 2,303
+ 2,303 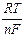 lg
lg 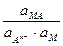 =
=
= 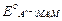 - 2,303
- 2,303 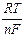 lg
lg 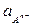
(учитывая, что активности металла и твердого соединения МА постоянны).
Таким образом, потенциал электрода второго рода определяется активностью анионов труднорастворимого соединения электродного металла. Однако электроды второго рода обратимы и по отношению к катионам электродного металла:
ПРМА = 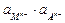 ;
;
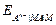 =
= 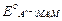 - 2,303
- 2,303 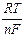 lg ПРМА + 2,303
lg ПРМА + 2,303 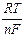 lg
lg  =
=
=  + 2,303
+ 2,303 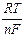 lg
lg 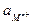 =
= 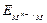 .
.
Из сопоставления потенциалов соответствующих электродов первого и второго рода можно найти ПР труднорастворимых солей.
Потенциалы электродов второго рода легко воспроизводимы и устойчивы, поэтому эти электроды часто применяют в качестве электродов сравнения, по отношению к которым измеряют потенциалы других электродов. Наиболее важны в практическом отношении каломельные, ртутно-сульфатные, хлоридсеребряные, ртутнооксидные и сурьмяные электроды.
Каломельный электрод. Это ртуть, покрытая пастой из смеси каломели со ртутью, находящаяся в контакте с раствором KCl:
Cl– êHg2Cl2 êHg
Электродная реакция:
Hg2Cl2 + 2 e = Hg + 2 Cl–
Eкал = Eокал - 2,303 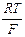 lg
lg 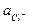
При 25оС Eкал = + 0,2678 - 0,059 lg 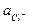 .
.
Eкал определяется активностью ионов Cl–. Наиболее часто употребляются каломельные полуэлементы, в которых концентрация KCl - насыщенный раствор, 1.0 М или 0.1 М. Каломельные электроды, особенно насыщенный, удобны тем, что диффузионный потенциал, возникающий на границе данного раствора с насыщенным KCl, незначителен и во многих случаях его можно не принимать во внимание.
Ртутно-сульфатный электрод SO42– êHg2SO4 êHg аналогичен каломельному, ртуть покрыта слоем пасты из ртути и сульфата ртути (I), а в качестве раствора используется H2SO4. При 25оС
Eрт.с. = + 0,6156 - 0,0296 lg 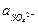 .
.
Хлоридсеребряный электрод представляет собой систему
Cl– êAgCl êAg;
Eхс = Eохс - 2,303 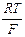 lg
lg 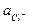 = + 0,2224 - 0,059 lg
= + 0,2224 - 0,059 lg 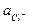 .
.
Ртутно-сульфатный и хлоридсеребряный электроды целесообразно применять в тех случаях, когда исследуемый полуэлемент содержит в качестве электролита либо серную кислоту или сульфаты, либо соляную кислоту или хлориды. Чтобы уменьшить величину диффузионного потенциала, концентрацию этих электролитов в электродах сравнения следует брать такую же, как и в исследуемых полуэлементах.
Металлоксидные электроды интересны тем, что здесь в роли анионов труднорастворимого соединения электродного металла выступают ионы гидроксида. К ним относятся, например, ртутнооксидный и сурьмяный электроды:
OH– êHgO êHg и OH– êSb2O3 êSb
Уравнения электродных реакций и потенциалов этих электродов:
HgO + H2O + 2 e = Hg + 2OH–
Sb2O3 + 3H2O + 6 e = 2Sb + 6OH–
Eрт.окс. = Eорт.окс. - 2,303 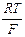 lg
lg 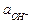 ;
;
Eсурьм. = Eосурьм. - 2,303 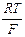 lg
lg 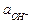 .
.
Уравнения для электродного потенциала получены при допущении, что постоянны активности не только соответствующих металлов и их оксидов, но и воды, также принимающей участие в электродной реакции.
Металлоксидные электроды второго рода, как и металлсолевые электроды второго рода, обратимы по отношению не только к ионам гидроксила, но и к ионам электродного металла. Кроме того, они обратимы и по отношению к ионам водорода, потому что ионное произведение воды при заданной Т постоянно для любого водного раствора электролита.
Металлоксидные электроды можно применять как электроды сравнения в любых растворах кислот и щелочей, однако ртутнооксидный электрод вследствие заметной растворимости оксидов ртути в кислотах можно рекомендовать лишь для растворов с рН > 7. Сурьмяный электрод из-за неустойчивости состава его поверхностного оксида применять как электрод сравнения нельзя; он используется в качестве индикаторного электрода для приближенных определений рН в умеренно кислых и нейтральных растворах.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1085; Нарушение авторских прав?; Мы поможем в написании вашей работы!