
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Потенциометрия. Потенциометрия основана на измерении разности электродных потенциалов, возникающей на границе электрод–электролит
|
|
|
|
Потенциометрия основана на измерении разности электродных потенциалов, возникающей на границе электрод–электролит. При этом потенциал одного из них (электрода сравнения) не зависит от измеряемого фактора, а потенциал второго (рабочего электрода) изменяется при воздействии на него аналита. “Passive” potential difference between two electrodes.
Электрохимический потенциал Е имеет электрохимическую и термодинамическую природу.
В результате окисления и восстановления исходных веществ образуется свободная энергия, которая расходуется на изменение потенциала рабочего электрода. Ионы движутся (диффундируют) к электроду и восстанавливаются на нем или окисляются, соответственно забирая или отдавая электроны. Стабильное значение потенциала возникает при равновесной реакции, т. е. когда в ней поддерживается равновесие между процессами выделения вещества на электроде и диффузии ионов. Ток через ячейку для сведения к минимуму эффекта поляризации должен быть близок к нулю.
Измерительный электрод в БСС всегда предназначен для выделения из раствора только необходимого иона из смеси, т. е. выполняется ион-селективным. Эти свойства достигаются благодаря применению мембран, пропускающих одни элементы и связывающие или задерживающие другие.
Наиболее часто в БСС используют в качестве ИП следующие типы ионоселективных потенциометрических преобразователей: электроды и полевые транзисторы для анализа ионов в жидкостях и газах. Потенциометрические электроды генерируют разность потенциалов, зависящую от активности специфических ионов. Регистрируемой величиной является разность потенциалов между измерительным электродом и инертным электродом сравнения. Потенциал электрода сравнения должен быть постоянным. Показания потенциометрического электрода описываются уравнением Нернста и поэтому электроды и измерительные приборы для них в большинстве случаев взаимозаменяемы. Важной характеристикой потенциометрических измерений является измерение потенциала электрода при фактическом отсутствии тока в цепи измерения. При измерениях не проходит каких-либо химических реакций и раствор находится в равновесном состоянии.
(a) Ион-селективные электроды. Логарифмическая зависимость между величиной потенциала и активностью ионов (46) позволяет создавать аналитические приборы с большим диапазоном измерения.
Наиболее распространен рН – электрод, селективный к ионам водорода (pH = –lg[H+], где [H+] – активность ионов водорода). Если определяется только один вид иона и существует электрохимическое равновесие между электродом и раствором, то при стандартных условиях потенциал электрода (46)
E = E 0 + 0,05915 lg[ H+ ]
(47)
б) Ион-селективные полевые транзисторы (ИСПТ). Полевой транзистор управляется напряжением, подаваемым на затвор. В ИСПТ затвор является ион-чувствительным [30] в результате того, что на него нанесен дополнительный слой, селективный к ионам с помощью таких соединений как Al2O3, Ta2O5, Si3N4 (рис. 9). Тогда выражение для тока стока приобретает вид
i с = k (U з – U п – a U э–д + const)2,
(48)
где U з – потенциал затвора; k – коэффициент, определяемый параметрами ион-селективного слоя, a – коэффициент, характеризующий химическую чувствительность мембраны, U п – пороговое напряжение затвора, U э–д – потенциал на границе электролит–диэлектрик, который, подобно pH-электроду, линейно зависит от логарифма концентрации ионов водорода:
U э–д = (RT / F) lg[H+].
(49)
в) Газочувствительные электроды. В этих электродах над газовой мембраной размещен тонкий слой промежуточного раствора, изменяющего свои свойства в зависимости от концентрации газа, что воспринимается ион-селективным электродом [3, 28].
г) Газочувствительные полевые транзисторы (ГЧПТ). Свойство металла палладия поглощать водород и катализировать его расщепление было использовано [3] для разработки газочувствительного полевого транзистора.
На границе затвора образуется слой ионов водорода, которые приводят к изменению тока стока транзистора. В присутствии кислорода атомы водорода вступают в реакцию, что уменьшает толщину их слоя, поэтому с помощью транзистора можно измерять концентрацию как водорода, так и кислорода.
Показано [3], что ГЧПТ могут катализировать расщепление сероводорода, аммиака, метана и бутана.
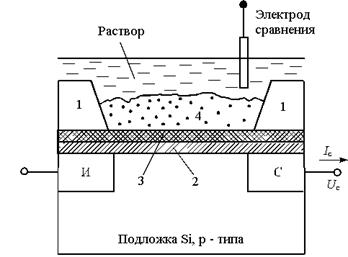
Рис. 9. Схематическое изображение pH - чувствительного полевого транзистора и БСС на его основе:
Si - кремниевая подложка p - типа, И, С - зоны истока и стока;
1- изолирующее покрытие, 2 - диэлектрик из двуокиси кремния;
3 - химически чувствительная мембрана, 4 - иммобилизованный БО;
I c, U 3, U c - ток стока, подаваемые потенциалы затвора и стока
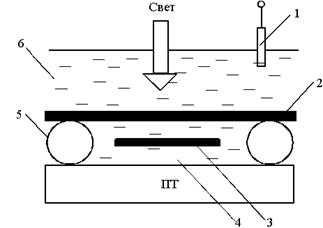
Рис. 10. Схематическое изображение БСС на основе светочувствительного транзистора: 1 - электрод сравнения, 2 - фоточувствительная мембрана, содержащая фотохромный краситель и ионофор, 3 - светозащитный экран.4 - внутренний электролит, 5 - герметизирующее кольцо.6 - раствор, содержащий измеряемые соединения
д) Светоуправляемые полевые транзисторы (СУПТ). Мембрану затвора полевого транзистора модифицируют фоточувствительными красителями, претерпевающими обратимые фотопревращения, сопровождающиеся изменением их зарядов (рис. 10). Существенной особенностью новых типов ИП является возможность изменять их состояние внешними источниками излучения. Например, УФ-излучение вызывает генерацию потенциала. Фотоиндуцированный потенциал может быть функцией состава электролита, наличия субстратов ферментативных реакций.При освещении мембраны импульсами УФ-излучения измеряют импульсный ток стока транзистора, который зависит от концентрации ионов. Это позволяет простыми методами создавать высокочувствительные миниатюрные БСС, а за счет быстрой замены мембраны с биослоем и красителями настраивать ИП на анализ широкого спектра биологически активных соединений.
Потенциометрические ИП используются в различных видах БСС.
а) Ион-селективные электроды с ферментными и клеточными БХП [45, 48–50, 65]. При ферментативных реакциях дыхания в результате переработки субстратов выделяются газы (пп. 2.3.1, 2.5.1). Пропускание некоторых газов через водный раствор приводит к появлению кислот и понижению значения pH.
Ферментные pH – электроды обычно включают:
· трубку с полупроницаемой мембраной;
· ферменты или организмы, иммобилизованные на мембране;
· полупроницаемую мембрану для измеряемого газа;
· слой водной среды с буферным раствором (для минимизации колебаний pH);
· ИП на основе pH-электрода.
Электрод погружают в аналит (п. 3.2) и через 30–60 мин фиксируют изменение pH. С помощью таких электродов можно оценивать активность соответствующих ферментов и воздействие на нее загрязнений среды. Недостатком их является малый срок службы – около 100 ч.
Помимо электродов, селективных к ионам водорода, разработаны [28] электроды, селективные к ионам Na+, K+, Cu+, Pb2+, Cd2+, F–, Cl–, Br–, J–.
б) Ион-селективные транзисторы с БХП на основе ферментов, организмов и комплекса антиген-антитело [30, 67]. На ион-селективном слое, нанесенном на затвор, иммобилизируют фермент или микроорганизмы и измеряют ток транзистора. На основе pH-чувствительных ИСПТ созданы опытные модели БСС на ацетилхолинэстреразу (п. 1.3.1), хлороароматические уксусные кислоты, ионы Na+. ИСПТ позволяют создавать БСС для определения пестицидов, иммуноглобулина, микробных клеток (в этом случае на мембране ИСПТ иммобилизуют антитела или клетки бактерий, меченые антителами). В перспективе такиие БСС могут составить конкуренцию иммуно-ферментному анализу (п. 2.5.6).
ИСПТ выпускаются АО «Авангард» (РФ), фирмой IMT (Швейцария).
в) Газочувствительные электроды с ферментными БХП [3]. Эти ИП позволяют упростить конструкцию рассмотренных выше ферментных электродов, и измерять концентрацию таких газов, как CO2, NH3, Cl2.
Наиболее распространены при проектировании БСС электроды фирмы ORION RES. CORP.
Таблица 7
БСС с газочувствительными и ион-селективными электродами [3]
| Вид ИП | Определяемый субстрат/фермент |
| NH3 | Мочевина, аминокислоты, глутамин, нитраты, нитриты, креатинин/ ли азы, деамин азы |
| CO2 | Мочевина, аминокислоты/ декарбоксил азы |
| pH | Пенициллин, РНК, ДНК, глюкоза /ферменты, катализирующие реакции с изменением pH |
| J– | Глюкоза, аминокислоты, холестерин, спирты |
г) Газочувствительные транзисторы (ГЧПТ) с ферментными БХП [3]. Этот тип БСС применяют для измерения активности дегидроген аз цикла Кребса (п. 1.2.2), отщепляющих водород, для определения кислорода и метана и для оценки активности ферментов анаэробного брожения.
д) Светоуправляемые транзисторы (СУПТ) с ферментными БХП. Данный тип ИП используют для проектирования БСС, чувствительных к иону аммония. Подобные БСС разработаны для оценки активности уре азы, фермента, катализирующего гидролиз мочевины до аммиака и углекислоты [30].
Перспективность полевых транзисторов обусловлена в первую очередь их сравнительно малыми размерами, возможностью смены биопленок, хорошей воспроизводимостью результатов, исключительно высокой чувствительностью, низкой ценой при массовом производстве.
В биосенсорной детекции широко используется принцип оценки либо концентрации продукта биохимической реакции, либо концентрации субстрата реакции. Если ферментативная реакция приводит к образованию электрохимически активного продукта, его можно определять/детектировать электрохимическими методами. Аналогично с помощью электрохимических методов можно определять субстраты реакции.
Ионометрия. В предыдущем разделе рассматривалось применение электрохимических (амперометрических) методов для детекции кислорода (субстрат реакции) и пероксида водорода (продукт реакции). В ряде случаев биохимическая реакция приводит к изменению ионного состава среды, что позволяет применять электрохимические методы детекции ионов – т.е. ионометрию. Наиболее распространенными случаями изменения ионного состава является изменение концентрации ионов водорода [Н+], т.е. изменение рН среды. Для оценки изменений ионного состава разработаны потенциометрические электрохимические методы, выполняемые с помощью ионочувствительных или ион-селективных электродов (ИСЭ). Ион-селективным является электрод, выходной потенциал которого пропорционален логарифму активности какого-либо специфического иона в измеряемом растворе. На основе ион-селективных электродов созданы разнообразные модели биосенсоров. В этом случае ИСЭ является преобразователем биосенсора, а сами биосенсоры, в соответствии с их классификацией, относятся к электрохимическим потенциометрического типа.
В биосенсорах потенциометрического типа преобразователь является генератором ЭДС. Возникающая разность потенциалов задается концентрацией/активностью определяемого иона. Измерения выполняются относительно электрода сравнения. Потенциометрические измерения характеризуются следующими особенностями: регистрируется потенциал Е как функция времени и концентрации С измеряемого иона, Е = f (t, С), при условии, что ток, протекающий через электрод, равен нулю, I = 0. Потенциометрические электроды должны иметь высокое сопротивление. Чем выше сопротивление, тем точнее регистрируется генерируемая разность потенциалов, поскольку снижается шунтирующее влияние электрода. Для измерений, как правило, используются электроды, сопротивление которых не менее, чем 1012 – 1015 Ом, что вполне приемлемо, с практической точки зрения, обеспечивает условие I ~ 0. Характеризуя параметры существующих ИСЭ отметим, что большинство из них имеют рабочий диапазон измеряемых концентраций от 10-1 до 10-5 М вещества. Исключение составляют рН-электроды, имеющие расширенный диапазон, заключенный в пределах от 1 до 10-12 М концентрации протонов, [Н+].
В электродах потенциометрического типа отсутствует расход вещества. Зависимость потенциала электрода Е от концентрации анализируемого вещества С является логарифмической функцией: Е = (RT/nF) ln C + const, где n – заряд иона; F- число Фарадея; R- газовая постоянная и T абсолютная температура. Незначительная ошибка при измерении Е может привести к довольно значительной погрешности определения С. Например, при n = 1 погрешность измерения Е в 10 мВ приводит к 19%-й погрешности для величины С. Из-за этих недостатков биосенсоры на основе амперометрических индикаторных электродов, для которых характерной является линейная зависимость тока I от концентрации C искомого вещества, считаются более практичными, несмотря на то, что для них в большинстве случаев необходимо строго контролировать гидродинамические условия вблизи поверхности электрода.
Рассмотрим основные принципы формирования биосенсоров потенциометрического типа.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2512; Нарушение авторских прав?; Мы поможем в написании вашей работы!