
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Выбор индикаторных электродов для химических реакций разного типа
|
|
|
|
1. Кислотно-основное титрование, определение рН раствора.
В этом случае индикаторный электрод должен реагировать на активность ионов Н+ (или величину рН раствора). К таким электродам относится, например, стеклянный электрод.
2. Окислительно-восстановительное титрование, определение потенциала раствора.
В этом случае в качестве индикаторных используют металлические инертные электроды. Они выполняют роль переносчиков электронов. Например, при титровании раствора Со2+ раствором K3[Fe(CN)6] протекает реакция:

Индикаторным электродом является инертный платиновый электрод. Его потенциал до т. э. определяется наличием пары Co3+/Co2+, т. к. в растворе имеется ещё неоттитрованный Co2+ и образовавшийся продукт реакции – Co3+. Следовательно, уравнение Нернста для платинового электрода до т. э. запишется в виде

После т. э. в растворе образуется новая окислительно-восстановительная пара – 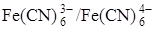 – за счёт наличия продукта реакции и появления избытка титранта. Теперь она определяет потенциал платинового электрода:
– за счёт наличия продукта реакции и появления избытка титранта. Теперь она определяет потенциал платинового электрода:
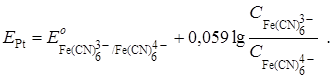
3. Осадительное титрование.
В этом случае в качестве индикаторных используют электроды, обратимые к определяемому иону или к титранту:
§ электроды I рода;
§ электроды II рода;
§ ИСЭ.
Например, для титрования ионов Cl– раствором AgNO3 можно взять серебряный электрод Ag/Ag+ (электрод I рода, реагирует на активность ионов титранта Ag+) или хлоридсеребряный электрод Ag, AgCl / KCl (электрод II рода, реагирует на активность определяемых ионов Cl–).
Кроме того, при проведении осадительного титрования можно воспользоваться инертным платиновым электродом, если искусственно создать в растворе окислительно-восстановительную пару. Например, при титровании раствора Zn2+ раствором K4[Fe(CN)6] протекает реакция осаждения:
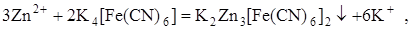
в ходе которой ни один элемент не меняет степени окисления, т. е. ни одной окислительно-восстановительной пары в растворе нет и платиновый электрод использовать невозможно. Но если добавить в раствор до начала титрования немного K3[Fe(CN)6], то в нём появляется пара  . При титровании концентрация одного из компонентов (K3[Fe(CN)6]) остаётся постоянной, а концентрация другого компонента (K4[Fe(CN)6]) меняется. Следовательно, меняется отношение их концентраций и потенциал платинового электрода тоже будет меняться.
. При титровании концентрация одного из компонентов (K3[Fe(CN)6]) остаётся постоянной, а концентрация другого компонента (K4[Fe(CN)6]) меняется. Следовательно, меняется отношение их концентраций и потенциал платинового электрода тоже будет меняться.
4. Комплексометрическое титрование.
В этом случае в качестве индикаторных используют электроды, обратимые к определяемому иону:
§ электроды I рода;
§ ИСЭ.
Кроме того, так же, как и при проведении осадительного титрования, можно воспользоваться инертным платиновым электродом, если искусственно создать в растворе окислительно-восстановительную пару. Например, при титровании ионов Fe3+ раствором комплексона III в раствор вводят немного Fe2+ и берут платиновый электрод.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 1100; Нарушение авторских прав?; Мы поможем в написании вашей работы!