
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Паперова хроматографія
|
|
|
|
Тонкошарова хроматографія (ТШХ) відноситься до площинної, розподільної (її різновидом є паперова хроматографія) хроматографії.ТШХ виконується на шарі сорбенту, який тонким шаром наноситься на металеві чи скляні пластини, є також і готові пластини із закріпленим шаром сорбента.
Йонно-обмінна хроматографія (ЙОХ) грунтується на обміні йонів, які знаходяться у фазі йоніту з йонами, які у вигляді розчину проходять через шар йоніту. У якості йоніту можуть бути: як природні так і синтетичні, органічні і неорганічні речовини (цеоліти, глини, бентоніт, Al2O3, йонно-обмінні смоли).
Йонно-обмінні смоли−це синтетичні полімери на основі феноформальдегідних смол, сополімерів стиролу і дивінілбензолу тощо, які містять функціональні групи, до складу яких входять рухливі іони. Йонно-обмінні смоли, одержані в 1935 році Адамсом і Холмсом, мають ряд переваг порівняно з природними алюмосилікатами (цеолітами):
- постійні характеристики;
- висока механічна і хімічна стійкість;
- можливість створення йонітів із необхідними параметрами, а також селективними щодо певної речовини;
- висока йонообмінна здатність.
Йонний обмін на катіоніті можна уявити з рис. 7.1.
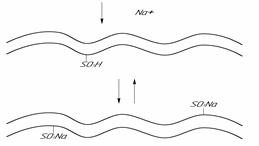
Рис. 7.1- Схема йонного обміну на сильнокислотному катіоніті КУ-2 в кислотній формі
Схематично процес обміну на катіоніті записується в такій формі:
RH + Na+↔ RNa + H+,
де RH і RNa- катіоніти H+ і Na+ у формі катіоніту, H+ і Na+ - у вільному вигляді.
За типом обміну іоніти поділяються на катіоніти і аніоніти. Залежно від типу функціональної групи катіоніти поділяються на сильнокислотні, містять йоногенну сульфогрупу SO3H (КУ-1, КУ-2), слабокислотні містять карбоксильну СООН (КФУ) чи фосфінову групу – PO3H2 (РФ, ІСФ-1). Сильноосновний аніоніт містить трифеніламонієву групу (АВ-17), слабоосновні (первинні і вторинні аміногрупи АН-2Ф, АН-1 тощо).
Для регенерації відпрацьованих катіонітів використовують розчин хлоридної кислоти(для переведення в кислотну форму), або розчин NaCl (для переведення в сольову форму).
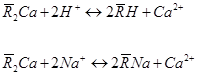 або
або 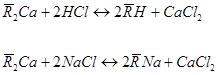
Для регенерації аніоніту використовують розчин лугу(для переведення в лужну форму) і розчин хлориду натрію(для переведення в сольовому).
 або
або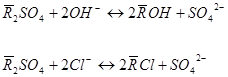
Якість йонно-обмінної смоли залежить від її сорбційної здатності і хімічної стійкості. Кількісними характеристиками ЙОХ є константа рівноваги йонного обміну К та коефіцієнт селективності Кс та обмінна ємність.
Константа рівноваги йонного обміну К для процесу (у нерухомій системі) має вигляд:
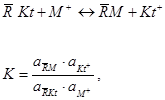 (7.1)
(7.1)
де 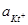 і
і 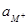 - активність йонів у розчині;
- активність йонів у розчині; 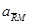 і
і 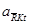 - активність йонів у фазі йонітів.
- активність йонів у фазі йонітів.
За величиною константи рівноваги можна визначити ступінь сорбованості йонів, якщо:
- К =1 − сорбованість витиснювального йона Кt+ і йона-витиснювача М+ однакова;
- К >1− сорбованість йона-витискувача більша;
- К <1− сорбованість йона-витискувача більша, процес відбувається у зворотному напрямі.
Замінивши активності концентраціями, одержимо концентраційну константу Кс (для розбавлених розчинів, коли f ≈1):
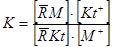 (7.2)
(7.2)
Якщо концентрація одного з йонів у фазі йоніту і в розчині велика, порівняно з іншими, наприклад, 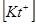 >>
>> 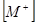 і
і 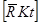 >>
>> 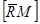 , то використовують коефіцієнт розподілу D:
, то використовують коефіцієнт розподілу D:
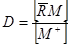 (7.3)
(7.3)
Коефіцієнт розподілу визначають експериментально. Він тим більший, чим сильніше йоніт утримує йон.
Якщо рухома фаза рухається відносно йоннообмінної смоли, рівноважні стани між йоннообмінником і розчином набуває характеру складних залежностей:
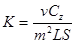 , (7.4)
, (7.4)
де V- об`єм витискуючого розчину,мл; С-концентрація в розчині витискуючих йонів, моль/л; m- питома ємність йоніту,моль/г; L- висота шару смоли в колонці, см; S- поперечний переріз колонки, см2; z-заряд витискуваного йона.
Чим більша відмінність між константами обмінної рівноваги, тим ефективніше розділення катіонів.
Можливість і ефективність розділення двох катіонів А+ і В+ за допомогою йоніту, що має протіон А+, визначають за допомогою коефіцієнту фактору розділення α (його ще називають коефіцієнтом селективності)−відношення констант обмінної рівноваги двох розділюваних йонів.
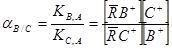 (7.5)
(7.5)
Залежно від природи йону, його концентрації та поляризованості, спорідненість його до сорбента змінюються у широких межах. Спорідненість тим більша, чим більша величина заряду йона; чим менший розмір гідратованого йона; чим більша поляризованість йона.
Ряд сорбованості для однозарядних катіонів має вигляд:
Li+< H+< Na+< K+< NH4+< Rb+< Cs+< Ag+< Tl+.
Ефективність обмінної ємності катіоніту, який знаходиться у сухому вигляді, визначається кількістю мілі моль-еквівалентів, поглинутих йонів на 1 г сухого іоніту; в набухлому вигляді – на 1 мл йоніту. Для більшості йонно-обміних смол ця величина складає 2-10 ммольекв/г.
ЙОХ широко використовується як в аналітичній хімії, так і у технологічних процесах, зокрема для знесолення вод.
Використанняя ЙОХ:
- для визначення концентрації розчинів солей;
- для визначення вмісту кристалізаційної води у кристалогідратах;
- для концентрування йонів;
- для розділення катіонів металів.
На відміну від паперової хроматографії, тонкошарова хроматографія на пластинах має ряд переваг, завдяки механічній міцності та хімічній стійкості, на пластинах можна розділяти агресивні суміші і використовувати агресивні проявники, крім того пластини можна використовувати повторно, змінюючи сорбент та товщину його шару.
Ефктивність сорбенту залежить від: природи активних центрів і їх концентрації на поверхні сорбенту, ступеня дисперсності частинок, площі активної поверхні сорбента, вмісту води, природи рухомої фази.
Вибір розчинника(рухомої фази) залежить від хімічної природи як сорбента, так і аналізованої суміші. При цьому враховують елюючу (вимиваючу) здатність (здатність витісняти речовини, сорбовані на поверхні сорбента).
Для сорбентів існують такі елюотропні ряди (в порядку зростання полярності):
Циклогексан→ССl4→трихлоретилен→толуол→бензол→дихлоретан→хлороформ→діетиловий ефір→етилацетат→піридин→ацитон→етанол→ метанол→вода.
Систему розчиник для ТШХ підбирають, змішуючи розчинники з початку та кінця елюотропного ряду.
Виконується на спеціальному хроматографічному папері, який схожий на фільтрувальний, проте більш однорідний і має високу міцність. Існують різні марки хроматографічного паперу. У паперовій хроматографії розподіл компонентів суміші відбувається між нерухомою фазою (водою, що міститься у папері) і рухомою фазою (розчинником), який рухається захоплюючи компонети, завдяки капілярним силам (висхідна хроматоргафія) чи капілярним і гравітаційним силам (нисхідна хроматографія).
За технікою виканання існує кілька видів площинної хроматографії: (рис. 7.2)
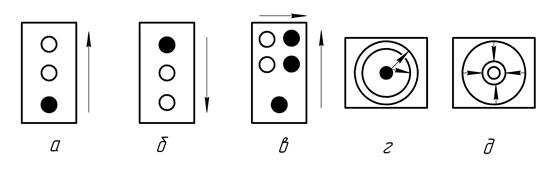
Рис. 7.2 −Види площинної хроматографії: одномірна висхідна(а), одномірна нисхідна (б), двомірна (в), концентрична колова (г), антиколова (д)
Коли рухома фаза пройде відстань приблизно 10 см від стартової лінії, на яку нанесений капіляром досліджуваний розчин, смужку паперу чи пластину виймають із хроматографічної камери, відмічаючи фінішну лінію олівцем, висушують і проявляють одержану хроматограму.
Способи проявлення хроматограм (способи детектування плям):
1. Фізичні способи:
- термічна обробка (за температури 200 °С органічні речовини обвугліюються, проявляючись у вигляді коричневих плям);
- радіохімічний- вимірюють радіоактивність, якщо компоненти суміші радіоактивні, або в них спеціально введені радіоізотопи;
- флуоресцентний- опромінюють ультрафіолетовим світлом; при цьому світяться флуоресцентні речовини суміші, або фон, якщо він оброблений флуоресціюючим реагентом, а плями не світяться.
2. Хімічні (обробка реагентами, які утворюють з компонентами суміші забарвлені сполуки), при цьому використовують:
- універсальні реагенти, зокрема, КMnO4 чи концентрована сірчана кислота на фіолетовому фоні:
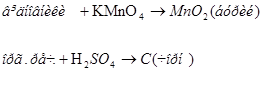
- селективні реагенти (за допомогою розчину 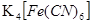 виявляють катіони
виявляють катіони 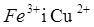 :
:
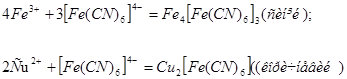
Якісний аналіз проводять за специфічним кольором плями; за величиною коефіціента рухливості- відношення відстані, яку пройшов кожен з компонентів до відстані, яку за цей час пройшов розчинник.(рис.7.3)
|
|
|
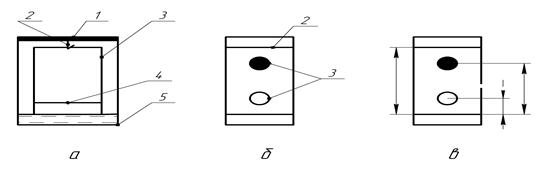
Рис. 7.3- Схема паперової хроматографії: а)камера для хроматографування (1-кришка, 2-гачок, 3-смужка хроматографічного паперу, 4-аналізована суміш, 5- рухома фаза); б) вигляд хроматограми після проявлення (1,2- стартова і фінішна лінії, 3- зони окремих компонентів); в)вимірювання відстаней для розрахунку коефіцієнтів рухливості(на прикладі суміші катіонів Сu2+ s Fe3+)
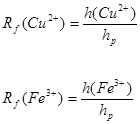
Два компоненти можна якісно розділити, якщо ∆ Rf≥0,04, якщо ці умови не виконюються плями компонентів знаходяться близько одна від одної, або накладаються.
Якщо хроматографію проводити на одному сорбенті, з тією ж рухомою фазою, за однакових температур, то величина Rf=const.
Кількісний аналіз у площинній хроматографії проводять:
1. безпосередньо на хроматограмі(на папері чи шарі сорбента):
- за розміром плями (напівкількісне визначення);
- спектрофотометричним методом за спектрами поглинання і спектрами відбивання;
2. вміст плями компонента розчиняють у розчиннику і кількісно визначають одним із методів:
- спектрофотометричним;
- флуоресцентним;
- атомно-абсорбційним, використовуючи метод порівняння, добавки, градуювального графіка.
Для розділення двох компонентів А і В, критерій розділення можна розрахувати як:
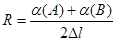 ,
,
де 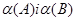 - діаметри плям компонентів А і В відповідно; ∆l- відстань між плямами.
- діаметри плям компонентів А і В відповідно; ∆l- відстань між плямами.
Ситова хроматографія (СХ)− різновид рідинної розподільної хроматографії, в якому нерухомою фазою є пористі речовини- молекулярні сита. Часточки розділюваної суміші, що мають менший розмір часток, утримуються в порах нерухомої фази, часточки з більшим, ніж пори, розміром виносяться з рухомою фазою.
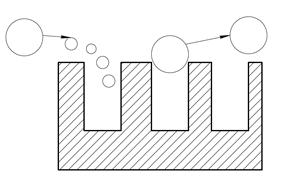
Рис. 7.4- Схема розділення компонентів суміші методом ситової хроматографії
Методом СХ розділяють високомолекулярні і низькомолекулярні речовини, проводять знесолення розчинів, видаляють домішки з газів та рідин.
Нерухомою фазою може бути: пористе скло, силікати, продукти піролізу пластмас, гелі.
СХ, в якій нерухомою фазою є гелі називається гель-проникаючою хроматографією.
Гелі−речовини здатні набухати, утворюючи структури з різними розмірами часток. Їх поділяють на гідрофобні (полістирольні гелі – стирогель, полівінілацетатні, пористе скло, порасил) та гідрофільні (декстранові- сефадекси, молселекти, поліакриламідні-біогелі).
Гелі бувають: м`які (декстранові), напівжорсткі (стирогелі), жорсткі (пористі гелі, пористе скло).
Хеміохроматографія. Це різновид хроматографії, який грунтується на різній здатності компонентів суміші, що розділяється, вступати і ті чи інші хімічні реакції з реагентами, які містить нерухома фаза. При цьому сорбент змішіють із реагентом або сорбент сам є реагентом.
За типом хімічної реакції хеміохроматографія поділяється на такі види:
- осадова;
- лігандна;
- окисно-відновна;
- біоспецифічна (афінна) хроматографія.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 2629; Нарушение авторских прав?; Мы поможем в написании вашей работы!