
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
При оксидиметрических титрованиях
|
|
|
|
Вывод.
(№ 465).
Краткая характеристика конкретных методов
Индикаторы, применяемые в окислительно – восстановительном титровании
Титрования.
Расчет, построение и анализ кривых окислительно – восстановительного
Лекция № 7
окислительно ‑ восстановительного титрования.
Для подготовки к контрольной работе и к сдаче коллоквиума по окислительно – восстановительному титрованию необходима также тщательная проработка методических указаний и учебного пособия:
- Калинкин И.П. Титриметрические методы анализа [Текст]: методические указания/ Калинкин И.П., Маметнабиев Т.Э. – СПб: СПбГТИ (ТУ), 2008 – 48с.
- Калинкин И.П. Титриметрические методы анализа. Примеры решения задач. Учебное пособие:[Текст] / И.П. Калинкин, Т.Э. Маметнабиев - СПб.: СПбГТИ (ТУ), 2009. – 43 c .(№1578).
7.1 В отличие от кривых других видов титрования, в которых кривые титрования обычно строят в координатах 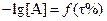 кривые редоксметрического титрования, как правило, строят в координатах
кривые редоксметрического титрования, как правило, строят в координатах  или
или 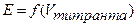 .
.
Если в редокс ─ реакции участвуют компоненты следующих обратимых
редокспар:
 (7.1)
(7.1)
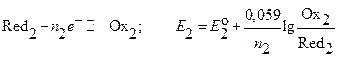 (7.2)
(7.2)
и 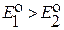 , то Ox1 выступает в качестве окислителя, который взаимодействует с восстановителем Red2. Как Ox1, так и Red2 могут быть либо определяемым веществом, либо титрантом (реагентом):
, то Ox1 выступает в качестве окислителя, который взаимодействует с восстановителем Red2. Как Ox1, так и Red2 могут быть либо определяемым веществом, либо титрантом (реагентом):
определяемое
титрант вещество (аналит)
оксидиметрическое титрование  (7.3)
(7.3)
редуциметрическое титрование  (7.4)
(7.4)
После добавления каждой порции титранта в растворе устанавливается равновесие: 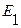 =
=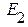 и в случае обратимых редокспереходов:
и в случае обратимых редокспереходов:
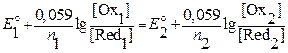 , (7.5))
, (7.5))
Следовательно, для вычисления потенциала в любой точке кривой титрования, кроме начального момента, для которого отношение [Oxi] / [Redi] неизвестно, расчет можно вести по концентрациям компонентов либо первой, либо второй пары.
Расчет целесообразно вести по той редокс ─ паре, которая доминирует в процессе титрования при соответствующем значении потенциала, т.е. до точки эквивалентности в интервале 0 < t < 100 %, расчет редокс ─ потенциала удобнее вести по концентрациям компонентов той пары, которая содержит определяемое вещество; концентрация этого вещества 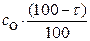 , концентрация второго компонента этой редокс ─ пары
, концентрация второго компонента этой редокс ─ пары 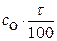 .
.
После точки эквивалентности (при t > 100 %) расчет лучше вести по второй паре, содержащей титрант. После точки эквивалентности титрант больше не расходуется на химическое взаимодействие с определяемым веществом. Происходит лишь накапливание титранта и, следовательно, его концентрацию можно вычислить по формуле 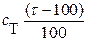 , где
, где 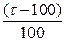 – доля избытка титранта. Концентрация второго компонента этой редокспары
– доля избытка титранта. Концентрация второго компонента этой редокспары 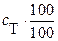 .Потенциал в точке эквивалентности рассчитывают по формуле:
.Потенциал в точке эквивалентности рассчитывают по формуле:  .
.
Потенциал в точке эквивалентности, согласно (7.5), можно выражать как потенциал первой пары и в то же время как потенциал второй пары:
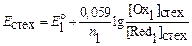 (7.6)
(7.6)
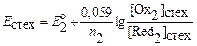 (7.7)
(7.7)
После умножения левой и правой части уравнения (7.6) на n 1, а уравнения (7.7) – на n 2 и сложения получают:
 (7.8)
(7.8)
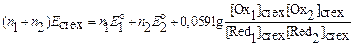 (7.9)
(7.9)
Из условий стехиометрии вышеприведенных уравнений (7.3) и (7.4) в точке эквивалентности имеют место соотношения:
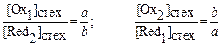 (7.10)
(7.10)
Следовательно, под логарифмом в уравнении (7.9) стоит единица, сам логарифм равен нулю, и редокс ─ потенциал в точке эквивалентности можно вычислить по формуле:
 (7.11))
(7.11))
На основании изложенных положений расчет значений окислительно ─ ‑восстановительного потенциала при построении кривых редоксметрических титрований производится по следующим формулам:
| Значения τ,% | Расчетные уравнения |
| 0 <τ <100 |
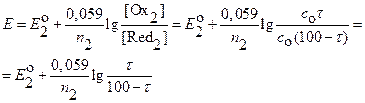 (7.12) (7.12)
|
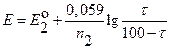
| |
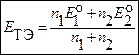
| |
| > 100 | 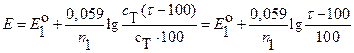 (7.13) (7.13)
|
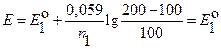
|
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 834; Нарушение авторских прав?; Мы поможем в написании вашей работы!