
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Константа химического равновесия
|
|
|
|
Рассмотрим реакцию в общем виде:
mA + nB  pC + qD.
pC + qD.
Состояние равновесия характеризуют величиной К – константы равновесия. Согласно закону действия масс константа равновесия равна отношению произведений равновесных концентраций продуктов ([C], [D], моль/л) и исходных веществ ([A], [B], моль/л) с учетом стехиометрических коэффициентов (m, n, p, q):
 .
.
Уравнение константы равновесия показывает, что в условиях равновесия концентрации всех веществ, участвующих в реакции, связаны между собой. Изменение концентрации любого из этих веществ влечет за собою изменения концентраций всех остальных веществ; в итоге устанавливаются новые концентрации, но соотношение между ними вновь отвечает константе равновесия. Константа равновесия зависит от природы веществ, температуры, но не зависит от концентраций.
Для гомогенной реакции
2 SO2(г) + O2(г)  2 SO3(г).
2 SO3(г).
константу равновесия химической реакции выражают уравнением:
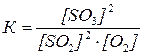 .
.
В случае гетерогенных реакций в выражение константы равновесия не входят концентрации конденсированных фаз (жидких или кристаллических, для реакций, протекающих в растворах, – твердых). Например,
СО2(г) + С(графит)  2СО(г)
2СО(г) 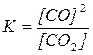
BaSO4(к)  Ba2+ + SO42–
Ba2+ + SO42– 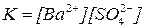 .
.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 750; Нарушение авторских прав?; Мы поможем в написании вашей работы!