
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Растворы
|
|
|
|
Задания для самостоятельной подготовки
Для предложенной обратимой реакции (табл. 1) напишите математическое выражение константы химического равновесия и укажите направление смещения равновесия при изменении условий:
а) уменьшении концентрации одного из газообразных продуктов;
б) понижении давления в системе;
в) повышении температуры в системе.
Таблица 1
| Номер | Уравнение реакции | 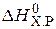 , кДж , кДж
| |
| 1 | 2 | 3 | |
SO3(г) + H2(г)  SO2(г) + H2O(г) SO2(г) + H2O(г)
| -144 | ||
2H2(г) + O2(г)  2 H2O(г) 2 H2O(г)
| -484 | ||
FeO(к) + CO(г)  Fe(к) + CO2(г) Fe(к) + CO2(г)
| +400 | ||
2N2O(г) + O2(г)  4NO(г) 4NO(г)
| +196 | ||
2NO(г)  N2(г) + O2(г) N2(г) + O2(г)
| -180 | ||
| Окончание табл. 1 | |||
| 1 | 2 | 3 | |
NH4Cl(к)  NH3(г) + HCl(г) NH3(г) + HCl(г)
| +63 | ||
2CH4(г) + 3O2(г)  2CO(г) + 4H2O(г) 2CO(г) + 4H2O(г)
| -597 | ||
H2O(г) + CO(г)  CO2(г) + H2(г) CO2(г) + H2(г)
| -41 | ||
2Al2(SO4)3 (к)  2Al2O3(к) + 6SO2(г) + 3O2(г) 2Al2O3(к) + 6SO2(г) + 3O2(г)
| +1740 | ||
ZnSO4(к)  ZnO(к) + SO3(г) ZnO(к) + SO3(г)
| +565 | ||
2N2O3(г)  2NO(г) + N2O4(г) 2NO(г) + N2O4(г)
| +149 | ||
2H2S(г) + 3O2(г)  2H2O(г) + 2SO2(г) 2H2O(г) + 2SO2(г)
| -1038 | ||
S(к) + H2(г)  H2S(г) H2S(г)
| -21 | ||
CO2(г) + C(т)  2CO(г) 2CO(г)
| +172 | ||
CH4(г) + H2O(г)  3H2(г) + CO(г) 3H2(г) + CO(г)
| +206 | ||
PCl5(г)  PCI3(г) + Cl2(г) PCI3(г) + Cl2(г)
| +21 | ||
Fe3O4(к) + CO(г)  3FeO(к) + CO2(г) 3FeO(к) + CO2(г)
| +21 | ||
N2O3(г)  NO(г) + NO2(г) NO(г) + NO2(г)
| +104 | ||
C(к) + O2(г)  CO2(г) CO2(г)
| -394 | ||
2AlCl3(к)  2Al(к) + 3Cl2(г) 2Al(к) + 3Cl2(г)
| +338 | ||
2CO(г) + O2(г)  2CO2(г) 2CO2(г)
| -566 | ||
2NH3(г)  N2(г) + 3H2(г) N2(г) + 3H2(г)
| +92 | ||
H2(г) + I2(г)  2HI(г) 2HI(г)
| +12 | ||
BaCO3(к)  BaO(к) + CO2 (г) BaO(к) + CO2 (г)
| +251 | ||
4NO(г) + 6H2O(г)  4NH3(г) + 5O2(г) 4NH3(г) + 5O2(г)
| +908 | ||
2МgCl2(к) + O2(г)  2MgO(к) + 2Cl2(г) 2MgO(к) + 2Cl2(г)
| +82 | ||
Ca(OH)2(к)  CaO(к) + H2O(г) CaO(к) + H2O(г)
| +109 | ||
N2(г) + O2(г)  2NO(г) 2NO(г)
| +180 | ||
NO(г) + NO2(г)  N2O3(г) N2O3(г)
| -149 | ||
3FeO(к) + CO2(г)  Fe3O4(к) + CO(г) Fe3O4(к) + CO(г)
| -21 | ||
Раствор – однородная многокомпонентная система переменного состава, состоящая из растворителя, растворенных веществ и продуктов их взаимодействия.
Существует несколько способов выражения состава раствора.
Массовая доля растворенного вещества (С). Это отношение массы растворенного вещества (mВ) к массе раствора (m). Это отношение может быть выражено в долях единицы или в процентах:
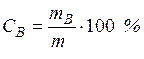 (1)
(1)
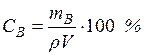 (2)
(2)
Молярная концентрация раствора (СM, моль/л, М) это отношение количества растворенного вещества (νВ) к объему раствора (V)
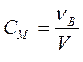 (3)
(3)
 (4)
(4)
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 693; Нарушение авторских прав?; Мы поможем в написании вашей работы!