
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Комплексные соединения. Комплексные соединения - это соединения, характеризующиеся наличием хотя бы одной ковалентной связи
|
|
|
|
Комплексные соединения - это соединения, характеризующиеся наличием хотя бы одной ковалентной связи, возникшей по донорно-акцепторному механизму.
Они образуются в результате взаимодействия более простых неорганических соединений: солей, кислот, оснований, без выделения побочных веществ. Например,
Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2;
FeCl3 + 6KCN = K3[Fe(CN)6] + 3KCl;
HgI2 + 2KI = K2[HgI4].
Теорию комплексных соединений предложил в 1893 году Вернер. В сос-таве каждого комплексного соединения он выделяяет внутреннюю и внеш-нюю сферы. Во внутреннюю сферу, которую отделяют квадратными скобка-ми, входит центральный атом - комплексообразователь и окружающие его ионы, атомы или молекулы, называемые лигандами, например:
[Co(NH3)6] Cl3
внутренняя внешняя
сфера сфера
Со3+ - комплексообразователь, NH3 - лиганд, 6 – координационное чис-ло.
Комплексообразователями наиболее часто служат ионы металлов (как правило, d- элементов). Лигандами могут быть ионы F-, Cl-, Br-, I-, CN-, NO2- и др., а также нейтральные полярные молекулы, например, H2O, NH3, CO. Число лигандов, располагающихся вокруг комплексообразователя, опреде-ляет координационное число, оно обычно равно удвоенной валентности иона-комплексообразователя.
Внутренняя сфера может быть нейтральной, положительно или отрица-тельно заряженной. Заряд комплексного иона (внутренняя сфера) равен алгебраической сумме зарядов комплексообразователя и лигандов.
Например, заряд иона [Au(CN)2] равен (+1) + (-2) = -1. Формула комплексного иона [Au(CN)2]-. В соответствии с номенклатурой, рекомендованной IUPAC, в комплексном соединении сначала всегда называют анион (в именительном падеже), а затем катион (в родительном падеже). Если в соединение входит комплексный катион, то сначала называют лиганды - отрицательные ионы, добавляя к ним окончание "о" (например, хлоро -, циано-, родано- и т.д.), а затем - лиганды - нейтральные молекулы. При этом аммиак называют аммин, воду - аква. Если лигандов несколько, то сначала греческим числительным указывают их число: 2 - ди, 3 - три, 4 - тетра, 5 - пента, 6 - гекса. В скобках указывается валентность металла.
Например,
[Ag(NH3)2]Cl - хлорид диамминсеребра (I);
[Cu(NH3)4]SO4 - сульфат тетраамминмеди (II);
[Pt(NH3)4(NO2)2]Cl2 - хлорид динитротетраамминплатины (IV).
Если в соединение входит комплексный анион, то, называя комплексо-образователь, используют латинское название элемента с добавлением окончания - ат с указанием степени его окисления. Наконец, называют кати-он внешней сферы в родительном падеже. Например,
K2[HgI4] - тетраиодомеркурат (II) калия;
K3[ Fe(CN)6 ] - гексацианоферрат (III) калия.
Название нейтральных комплексов составляют из названия лигандов (в указанной выше последовательности) и обычных русских названий цент-ральных атомов в именительном падеже, степень окисления не указывается. Например:
[ PtCl4(NH3)2 ] - тетрахлородиамминплатина;
[ Co(NO2)3(H2O)3 ] - тринитритотриаквакобальт.
В водных растворах комплексные соединения практически полностью диссоциируют на ионы внешней сферы и комплексный ион, т.е. являются сильными электролитами:
K[ Ag(CN)2 ] ® K+ + [ Ag(CN)2 ]- - первичная диссоциация.
Комплексные ионы диссоциируют по типу слабых электролитов:
 [ Ag(CN)2 ]- Ag+ + 2CN-.
[ Ag(CN)2 ]- Ag+ + 2CN-.
Как равновесный процесс диссоциацию комплексного иона можно охарактеризовать константой равновесия, называемой константой нестойкости комплекса Кн = 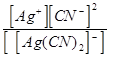
Чем больше константа нестойкости, тем менее прочен комплекс, и наоборот. Комплексный ион можно разрушить, заменяя лиганды на более сильные или связывая ион-комплексообразователь в нерастворимое соединение с более низким произведением растворимости:
[ CoCl6 ]3- + 6CN - = [ Co(CN)6 ]3- + 6Cl-
KH KH
KH > KH - условие разрушения
[ Cu(NH3)4 ]2+ + S2- = CuS¯ + 4NH3
KH ПР
KH > ПР - условие разрушения
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 364; Нарушение авторских прав?; Мы поможем в написании вашей работы!