
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вязкость газов и углеводородных конденсатов
|
|
|
|
Вязкость газа в зависимости от изменения параметров, характеризующих его состояние, изменяется сложным образом. При низких давлениях и температурах свойства реальных газов приближаются к идеальным. Закономерности изменения вязкости газов при различных давлениях и температурах можно объяснить, исходя из некоторых положений кинетической теории газов. Динамическая вязкость газа связана с его плотностью r, средней длиной свободного пробега молекул l и средней скоростью молекул v соотношением 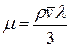 . (Ш.64)
. (Ш.64)
По формуле (Ш.54) определяется зависимость динамической вязкости газа от давления и температуры. С повышением давления плотность газа возрастает, но при этом уменьшается средняя длина свободного пробега молекул, а скорость их не изменяется. Поэтому с увеличением давления динамическая вязкость газа вначале практически остается постоянной. Из формулы (III.54) также следует, что с увеличением температуры вязкость_газа должна возрастать, так как средняя скорость молекул v увеличивается, а r и l, остаются постоянными при постоянном объеме газа. Отмеченный характер изменения вязкости газов объясняется спецификой проявления внутреннего трения. Количество движения из слоя в слой передается вследствие перелета молекул газа в движущиеся друг относительно друга слои. При этом возникают силы, тормозящие движение одного слоя и увеличивающие скорость движения другого. С повышением температуры увеличиваются скорость и количество движения, передаваемое в единицу времени, и, следовательно, больше будет вязкость. Вязкость газов мало зависит от давлений, если они близки к атмосферному. Однако с повышением давления эти закономерности нарушаются — с увеличением температуры понижается вязкость газа, т. е. при высоких давлениях вязкость газов изменяется с повышением температуры аналогично изменению вязкости жидкости. Газы с более высокой молекулярной массой, как правило, имеют и большую вязкость. В сжатом газе перелет молекул в движущиеся друг относительно друга слои затруднен и передача количества движения из слоя в слой происходит в основном, как у жидкостей, за счет временного объединения молекул на границе слоев. При повышении температуры ухудшаются условия для объединения молекул вследствие увеличения скоростей их движения и поэтому вязкость сильно сжатых газов уменьшается с повышением температуры. На рис. III.4 приведена зависимость динамической вязкости метана от давления и температуры, а на рис. III.5 — вязкости различных газов при атмосферном давлении в зависимости от температуры. В широком диапазоне давлений и температур вязкости смесей углеводородных (неполярных) газов можно определить по графикам на рис. III.6, составленным в приведенных координатах на основе закона соответственных состояний (по вертикальной оси отложено отношение вязкости m при различных давлениях к вязкости (m0 при атмосферном давлении).
 Рис. II1.4. Зависимость коэффициента динамической вязкости метана от давления и температуры.
Рис. II1.4. Зависимость коэффициента динамической вязкости метана от давления и температуры.

 Рис. II1.5. Динамическая вязкость газов при атмосферном давлении в зависимости от температуры: 1 — гелий; 2 — воздух; 3 — азот; 4 — углекислый газ; 5 — сероводород; 6 — метан; 7 — этилен; 8 — этан; 9 — пропан; 10 — n-бутан; 11 — i-бутан; 12 — пентан; 13 — гексан; 14 — гептан; 15 — октан; 16 — нонан; 17 — декан
Рис. II1.5. Динамическая вязкость газов при атмосферном давлении в зависимости от температуры: 1 — гелий; 2 — воздух; 3 — азот; 4 — углекислый газ; 5 — сероводород; 6 — метан; 7 — этилен; 8 — этан; 9 — пропан; 10 — n-бутан; 11 — i-бутан; 12 — пентан; 13 — гексан; 14 — гептан; 15 — октан; 16 — нонан; 17 — декан
Рис. II1.6, Зависимость отношения вязкости m/m0 от приведенных давлений и температур.
При содержании в газе более 5 % азота следует учитывать его влияние на вязкость газа и определять средневзвешенную вязкость смеси по формуле
m = yama + (1—ya)mу, (II1.55)
 где m — динамическая вязкость смесей углеводородных газов и азота; ma и mу — динамические вязкости азота (рис. Ш.7) и углеводородной части смеси газов; уа — молярная доля азота в составе газа.
где m — динамическая вязкость смесей углеводородных газов и азота; ma и mу — динамические вязкости азота (рис. Ш.7) и углеводородной части смеси газов; уа — молярная доля азота в составе газа.
Рис. III.7. Зависимость динамической вязкости азота от давления и температуры
Для экспериментального определения вязкости газов при различных условиях разработано много методов. Основные из них — метод, основанный на измерении скорости падения шарика в исследуемом газе, методы, основанные на регистрации скорости вращения цилиндров и затухания вращательных колебаний диска, подвешенного в исследуемом газе.
Коэффициент динамической вязкости природных газов можно рассчитать по приведенным параметрам [25].
Например, при высоких давлениях (р>5 МПа) коэффициент динамической вязкости газа можно подсчитать по формуле
(m — m0) ε = 10,8×10-5 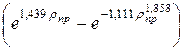 (II1.56)
(II1.56)
Здесь m0 - коэффициент динамической вязкости газов при давлении р=0,1 МПа, мПа×с
 (III.57)
(III.57)
 Коэффициент динамической вязкости стабильного конденсата многих газоконденсатных месторождений при различных давлениях и температурах (при 30£t£200 °С; 1£р£50,0 МПа) можно приближенно рассчитать по формуле
Коэффициент динамической вязкости стабильного конденсата многих газоконденсатных месторождений при различных давлениях и температурах (при 30£t£200 °С; 1£р£50,0 МПа) можно приближенно рассчитать по формуле
 мПа-с. (III.58)
мПа-с. (III.58)
Зависимость вязкости жидких углеводородов при атмосферном давлении от температуры и молекулярной массы показана на рис. III.8.
Рис. III.8. Зависимость коэффициента динамической вязкости жидких углеводородов при атмосферном давлении от молекулярной массы при различных температурах
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 3608; Нарушение авторских прав?; Мы поможем в написании вашей работы!