
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Коэффициент сверхсжимаемости природных газов
|
|
|
|
Для определения многих физических свойств природных газов (коэффициента сверхсжимаемости, плотности, энтальпии, энтропии, коэффициента летучести др.) используются уравнения состояния.
Уравнением состояния называется аналитическая зависимость между параметрами, описывающими поведение простого или сложного вещества. В качестве таких параметров используются давление, объем и температура.
Менделеев—Клапейрон предложили следующее уравнение состояния идеальных газов: pV=GRT, (III.16)
где р — абсолютное давление, Па; V — объем, м3; G — масса вещества, кг; Т—абсолютная температура, К; R— удельная газовая постоянная, кДж/(кг-К).
Идеальным называется газ, силами взаимодействия между молекулами которого пренебрегают.
С термодинамической точки зрения идеальным называется газ, для которого справедливы равенства (III.17), (III.18) 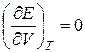 . (III.17)
. (III.17)
где Е — внутренняя энергия парообразования, Дж/моль.
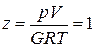 (III.18)
(III.18)
Здесь z — коэффициент, характеризующий степень отклонения реального газа от закона идеальных газов (коэффициент сверхсжимаемости).
Экспериментальная проверка уравнения (III.16), проведенная многими исследователями, показала, что все реальные газы не подчиняются законам идеальных газов.
Голландский физик Ван-дер-Ваальс в 1879 г. предложил учитывать собственный объем молекул газа и силы их взаимного притяжения посредством введения дополнительных членов в уравнение Менделеева—Клапейрона
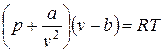 , (III.19)
, (III.19)
где v — удельный объем газа, а/v2 — константа сцепления молекул; b — поправка на объем молекул.
В уравнении (III.1.9) слагаемое а/v2 выражает внутреннее давление, которое является как бы равнодействующей сил притяжения всех молекул в объеме v. Оно прибавляется к внешнему давлению.
Ван-дер-Ваальс нашел, что поправка на объем молекул b, имеющих шарообразную форму, равна собственному объему молекул, увеличенному в 4 раза.
Уравнение (III.19) приближенное. Оказалось, что коэффициенты а и b в действительности — сложные функции объема температуры, формы молекул газа.
Это уравнение состояния удовлетворительно описывает поведение реальных газов лишь при давлениях до 10 МПа и температурах 283—293 К, но оно не может численно описывать поведение природных углеводородных газов гомологического ряда метана.
Дальнейший прогресс науки и техники требовал разработки более точного уравнения состояния природных газов, способного правильно описывать поведение их при давлениях до 100 МПа и температурах до 573 К в процессах добычи газа и при давлениях до 20 МПа и низких температурах до 123—93 К в процессах переработки природных газов.
В решении этой проблемы выявились два направления:
1) введение коэффициента z в уравнение состояния идеального газа, учитывающего отклонение реального газа от идеального;
2) добавление в уравнение состояния идеального газа большего числа констант. Так появились уравнения состояния Битти-Бриджмена с пятью константами, Бенедикта—Вебба—Рубина с восемью константами и др.
Рассмотрим подробнее два этих направления. Д. Браун и Д. Катц на основании изучения результатов своих экспериментальных измерений коэффициента отклонения реальных газов от законов идеального газового состояния z установили, что если приведенные параметры различных природных газов одинаковы (Рпр, Tпр), то они находятся в соответственных состояниях, при которых их физические и термодинамические свойства (z, плотность и др.) одинаковы, т. е. z=z (рпр, Тпр).
Приведенными параметрами индивидуальных компонентов называются безразмерные величины, показывающие, во сколько раз действительные параметры состояния газа (давление, абсолютная температура, объем, плотность, коэффициент отклонения) больше или меньше критических.
рпр = р/ркр; Tпр = T/Tкр; Vnp=V/Vкр; rпр=r/rкр; znp=z/zкр. (III.20)
Реальные природные газы -физические смеси большого числа углеводородных и неуглеводородных компонентов, простых и сложных газов. Молекулы простых газов (метан, гелий, аргон, криптон, ксенон и др.) имеют сферическую форму, а молекулы сложных газов и жидкостей — несферическую. Для простых газов силы притяжения, действующие вдоль линии, соединяющей центры сферических молекул, пропорциональны расстоянию в шестой степени. Для cложных газов и жидкостей силы притяжения (или отталкивания) между различными группами молекулярных пар не могут быть представлены лишь одной силой притяжения между центрами молекул. Для учета других, нецентричных сил вводится ацентрический фактор со. Он является третьим после приведенного давления и температуры параметром, оценивающим меру отклонения коэффициента сверхсжимаемости природных газов от его значения, определяемого классической двухпараметрической теоремой соответственных состояний z=z(pnp, Тпр, w) (III.21)
или zCM=z0(pnp, Тпр) + z1(pnp, Тпр)wсм (III.22)
где z0(pnp, Тпр) — коэффициент сверхсжимаемости простого газа, определяемый величинами pnp и Тпр, при w =0; z1(pnp, Тпр)—поправка к обобщенному коэффициенту сверхсжимаемости сложных газов и жидкостей, являющаяся функцией только приведенного давления и температуры; wсм — ацентрический фактор смеси газов,
wсм= 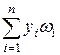 , (III.23)
, (III.23)
где wi — ацентрический фактор i-го компонента в смеси. Часто он определяется по формуле Эдмистера 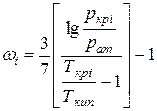 (П1-24)
(П1-24)
Здесь рат — атмосферное давление; Ткип — температура кипения компонента при атмосферном давлении. Ацентрический фактор многих веществ изменяется в пределах 0—0,4 (см. табл. III.5).
Отношение абсолютной критической температуры компонента к абсолютной температуре кипения при нормальных физических условиях зависит от типа углеводородов: парафиновых, нафтеновых или ароматических. Для углеводородов парафинового ряда отношение температур можно определить, например, по корреляционной зависимости Г. Р. Гуревича
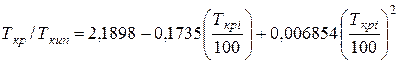 (111.25)
(111.25)
где 540£Ткр£775 К; 372£Ткип£625 К.
Приведенными параметрами для смесей газов называются безразмерные величины отношения действительных давлений, температуры, объема, плотности и коэффициента отклонения к псевдокритическим (среднекритическим) параметрам
рпр.см = р/ркр.см; Tпр.см = T/Tкр.см; Vnp.см =V/Vкр.см; rпр.см =r/rкр.см; znp.см =z/zкр.см.
где псевдокритические (среднекритические) параметры смеси (ркр.см; Tкр.см; Vкр.см; rкр.см; zкр.см) вычисляются по какому-либо правилу, чаще всего по правилу аддитивности КЭЯ. Аддитивным называется суммарное физическое свойство смеси, определяемое как сумма произведений молярных концентраций компонентов в смеси на свойства этих компонентов,
ркр.см= 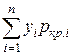 ; Ткр.см=
; Ткр.см= 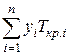 ; Vкр.см=
; Vкр.см= 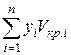 ;
;
rкр.см= 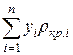 ; zкр.см=
; zкр.см=  ; (IП.26)
; (IП.26)
где yi — молярная доля компонента i в смеси газов; ркр.i; Tкр. i; Vкр.i; rкр.i; zкр.i — критические давление, абсолютная температура, молярный объем, плотность и коэффициент отклонения i-ro компонента смеси соответственно; n— число компонентов в смеси.
Критические давление, температура, молярный объем, плотность, коэффициент сверхсжимаемости z и другие величины приведены в табл. III.5.
Во многих случаях состав природных углеводородных газов определяется не полностью, а до бутана (С4Н10) или гексана (С6Н14) включительно, а все остальные компоненты объединяются в остаток (или псевдокомпонент) C5+ (или С7+).
Псевдокритические параметры такого остатка (C7+) при неизвестном групповом составе можно рассчитать по измеряемым величинам: его молекулярной массе — MC7+ и относительной (по воде) плотности rC7+ по зависимостям (III.28) и (III.29) или по графикам, приведенным в [6].
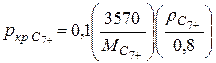 [МПа], (111.27)
[МПа], (111.27)
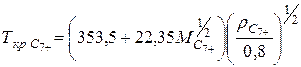 [К] (П1.28)
[К] (П1.28)
при 100£МC7+£ 240, 0,70£рC7+£0,95.
Если состав газоконденсатной смеси неизвестен, а измерена ее относительная плотность по воздуху Dсм, псевдокритические параметры смеси можно рассчитать по уравнениям
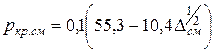 [МПа], (III.29)
[МПа], (III.29)
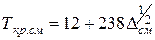 (II1.30)
(II1.30)
при 0,5£ 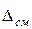 £1.
£1.
Если в составе природного газа содержится сероводород (менее 5 % по объему), критические параметры смеси можно определить по формулам
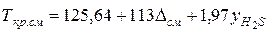 [К], (Ш.31)
[К], (Ш.31)
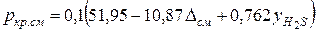 [МПа]. (111.32)
[МПа]. (111.32)
Пусть yH2S =0 и 1,4 % по объему, Dсм = 0,7. Определим влияние H2S на Ркр.см и Tкр.см. По формуле (111.30) без учета влияния H2S: Ткр.см = 12 + 238×0,71/2 = 211 К.
С учетом влияния H2S: Ткр.см=125,64+113×0,7+1,97×1,4 = 207,5 К.
Аналогично имеем 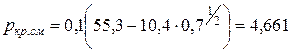 МПа,
МПа,
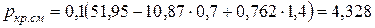 МПа.
МПа.
 Таким образом, коэффициент отклонения природной углеводородной смеси z можно определить графически, зная приведенные параметры рпр.см и Tпр.см (рис. III.1), или рассчитать по алгоритму и программе, составленным в 1961 г. Сейримом.
Таким образом, коэффициент отклонения природной углеводородной смеси z можно определить графически, зная приведенные параметры рпр.см и Tпр.см (рис. III.1), или рассчитать по алгоритму и программе, составленным в 1961 г. Сейримом.
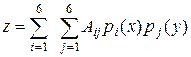 (III.33)
(III.33)
где Аij — 36 числовых коэффициентов; pj (у) —полиномы от аргументов 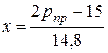 ;
; 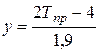 (Ш 34)
(Ш 34)
Рис. III.1. Зависимость коэффициента сверхсжимаемости природного газа z от приведенных абсолютных давления рпр и температуры Тпр
Коэффициент z по программе Сейрима можно определять с погрешностью, не превышающей 5 % от истинного значения, в довольно широком диапазоне приведенных давлений и температур: 0,01£рпр£20; 1,05£Тпр£3.
Сравнение вычисленных значений коэффициентов сжимаемости газоконденсатных смесей, содержащих углеводороды, различного строения (парафиновые, нафтеновые и ароматические), с данными экспериментальных измерений показало, что присутствие нафтеновых и ароматических углеводородов до 10 % по объему практически не влияет на характер изменения коэффициента отклонения z.
При содержании неуглеводородных компонентов в составе природного газа (N2, CO2, H2S) следует вводить поправку в рассчитанное значение z по правилу аддитивности: z = yaza + (l-ya)zy, (1II.35)
 где уа — молярная доля азота в смеси газов; za, zу — коэффициенты сверхсжимаемости азота и углеводородной части смеси газов.
где уа — молярная доля азота в смеси газов; za, zу — коэффициенты сверхсжимаемости азота и углеводородной части смеси газов.
На рис. III.2 показаны графические зависимости коэффициента сверхсжимаемости азота от давления и температуры.
Pис III.2. Зависимость коэффициента сверхсжимаемости азота от давления и температуры
При решении задач, связанных с добычей, транспортом, хранением и переработкой природных газов, наиболее употребительны уравнения состояния Редлиха — Квонга [7] и Бенедикта— Вебба — Рубина [7, 25]. Уравнение состояния Редлиха— Квонга записывается следующим образом:
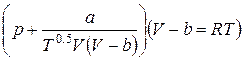 . (1II.36)
. (1II.36)
Для определения коэффициента z уравнение Редлиха — Квонга преобразуется к виду
z3—z2+ z(a2—b2р—b)р—a2bp2 = 0, (II1.37)
где а2 = 0,4278Т2.5кр/ркрТ2,5, (III.38)
b = 0,0867Tкр/ркрТ. (III 1.39)
Сравнение результатов расчета коэффициента z по уравнению (111.37) с данными экспериментальных измерений показало, что погрешность вычислений не превышает 2 % при 0,01£рпр<12; 1,05<Тпр£1,6.
Приведены пример и справочные и расчётные величины в книге
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 7462; Нарушение авторских прав?; Мы поможем в написании вашей работы!