
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Второй закон термодинамики
|
|
|
|
Первый закон термодинамики не позволяет определить направление протекания процесса. То есть возможен процесс самопроизвольной передачи тепла от холодного тела к горячему.
Второй закон термодинамики утверждает, что невозможен процесс, единственным результатом которого является передача энергии в форме теплоты от холодного тела к горячему. Из этого следует, что переход от неупорядоченного движения частиц к упорядоченному возможен лишь при условии, что он сопровождается каким-либо компенсирующим процессом.
Отношение теплоты Q, полученной телом в изотермическом процессе, к температуре T процесса, называется приведенным количеством теплоты Q*.
На малом участке процесса 1-2:
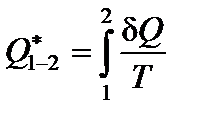 ;
;
Найдем приведенное количество теплоты, сообщаемое телу в обратимом цикле Карно.
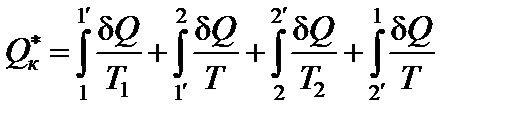 ;
;
Второй и четвертый интегралы равны нулю, так как 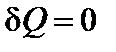 (адиабатные процессы)
(адиабатные процессы)
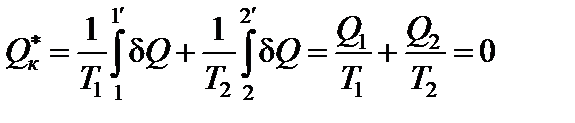 (с учетом формулы (*)).
(с учетом формулы (*)).
Это справедливо для любого обратимого цикла.
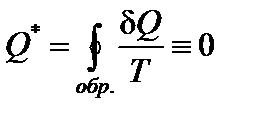 ;
;
В этом случае стоящее под интегралом выражение является полным дифференциалом некоторой функции S, т.е.
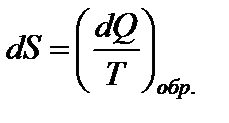
Функция S называется энтропией. dS и dQ имеют один и тот же знак. Значит, по характеру изменения энтропии можно судить о направлении процесса теплообмена.
Энтропия тела, подобно внутренней энергии, является однозначной функцией его состояния.
Энтропия изолированной системы при любых происходящих в ней процессах не может убывать
 .
.
Из определения энтропии следует, что

Запишем первый закон термодинамики

Здесь знак равенства относится к обратимым процессам, а знак неравенства – к необратимым.
Сделаем преобразования


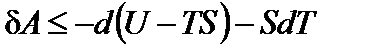 ;
;
Введем обозначение: 

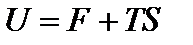 .
.
Таким образом, внутренняя энергия тела состоит из двух частей: F – называется свободной энергией. Это та энергия, которая может быть обращена в работу; TS – связанная энергия, которая не может быть передана в изотермическом процессе в форме работы. Энтропия является мерой связанности энергии.
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 334; Нарушение авторских прав?; Мы поможем в написании вашей работы!