
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Окислительный обжиг сульфидов
|
|
|
|
Нерастворимые сульфиды
Необратимый гидролиз сульфидов
Обратимый гидролиз растворимых сульфидов
Сульфиды
Реакции протекают в тех случаях, если образующийся сульфид Ме нерастворим не только в воде, но и в сильных кислотах.
Качественная реакция на сульфид-анион S2- и на H2S
Одна из таких реакций используется для обнаружения анионов S2- и сероводорода:
H2S+Pb(NO3)2=2HNO3+PbS↓ – черный осадок.
Газообразный H2S обнаруживают с помощью влажной бумаги, смоченной раствором Pb(NO3)2, которая чернеет в присутствии H2S
Сульфидами называют бинарные соединения серы с менее ЭО элементами, в том числе с некоторыми неметаллами
Наибольшее значение имеют сульфиды металлов, поскольку многие из них представляют собой природные соединения и используются как сырье для получения свободных металлов, серы, диоксида серы.
Сульфиды щелочных металлов и аммония хорошо растворимы в воде, но в водном растворе они подвергаются гидролизу в очень значительной степени: S2-+H2O ⇆ HS- +OH-. Поэтому растворы сульфидов имеют сильнощелочную реакцию.
Труднорастворимые сульфиды щелочно-земельных металлов и Mg благодаря гидролизу переходят в растворимые кислые соли – гидросульфиды:
2CaS+2HOH=Ca(HS)2+Ca(OH)2
При нагревании растворов сульфидов гидролиз протекает по второй ступени:
HS-+H2O ⇆ H2S↑+OH-
Сульфиды некоторых металлов подвергаются необратимому гидролизу и полностью разлагаются в водных растворах, например:
Al2S3+6H2O=3H2S↑+2Al(OH)3↓
Аналогичным образом разлагаются Cr2S3, Fe2S3.
Большинство сульфидов тяжелых металлов в воде практически не растворяются и поэтому гидролизу не подвергаются. Некоторые из них растворяются под действием сильных кислот, например:
FeS+2HCl=FeCl2+H2S↑;
ZnS+2HCl=ZnCl2+H2S↑.
Окисление сульфидов кислородом воздуха при высокой температуре является важной стадией переработки сульфидного сырья. Примеры:
2ZnS+3O2=2ZnO+2SO2↑;
4FeS2+11O2=2Fe2O3+8SO2↑
Соединения серы (IV). SO2 - оксид серы
Физические свойства.
SO2 - диоксид серы, сернистый газ, сернистый ангидрид. Бесцветный газ с резким запахом, хорошо растворяется в воде.
Химические свойства. SO2 - кислотный оксид.
При растворении SO2 в воде происходит его частичное соединение с молекулами воды – образуется слабая сернистая кислота. В водном растворе устанавливаются равновесия:
SO2+H2O ⇆ H2SO3 ⇆ H++HSO3- ⇆ 2H++SO32-
При обычных условиях равновесие сильно смещено влево.
Взаимодействие с основными оксидами и щелочами.
SO2+CaO=CaSO3 – сульфид кальция
SO2+NaOH=NaHSO3 – гидросульфит натрия
SO2+2NaOH=H2O+Na2SO3 – сульфит натрия
SO2 - активный восстановитель.
Диоксид серы окисляется в газовой фазе до SO3:
2SO2+O2=2SO3
SO2+O3=SO3+O2
SO2+NO2=SO3+NO
На свету легко окисляется хлором:
SO2+Cl2=SO2Cl2 – хлористый сульфурил
В водных растворах при окислении SO2 образуется серная кислота:
SO2+2HNO3=H2SO4+2NO2 ↑;
SO2+H2O2=H2SO4
Обесцвечивание окрашенных окислителей (KMnO4 и Br2) – качественная реакция для распознавания SO2:
SO2+Br2+2H2O=H2SO4+2HBr
3SO2+2KMnO4+4H2O=3H2SO4+2MnO2↓+2KOH
SO2 - окислитель (при взаимодействии с сильными восстановителями):
Продуктом восстановления чаще всего является свободная сера:
SO2+2H2S 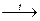 3S↓+2H2O
3S↓+2H2O
SO2+2CO 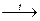 S+2CO2
S+2CO2
H2SO3 - сернистая кислота
В свободном состоянии не выделена. Очень непрочное соединение. Образуется при растворении SO2 в воде. Обладает свойствами слабой кислоты.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 4745; Нарушение авторских прав?; Мы поможем в написании вашей работы!