
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример 1. Составьте молекулярное и ионное уравнение реакции взаимодействия нитрата серебра с хлоридом калия
|
|
|
|
Решение:
Составим молекулярное уравнение реакции:
AgNO3+KCl = AgCl 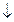 + KNO3
+ KNO3
По таблице растворимости устанавливаем, что AgNO3, КСl, KNO3 — растворимые соединения, AgCl — нерастворимое вещество.
Составляем ионное уравнение реакции с учетом растворимости соединений:
Ag+ + NO-3 + K+ + Сl- = AgCl 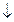 + К+ + NO-3
+ К+ + NO-3
Исключаем из правой и левой частей уравнения одинаковые ионы и получим краткое ионное уравнение:
Ag+ + Cl- = AgCl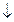
Краткое ионное уравнение раскрывает сущность происходящего химического превращения. Видно, что фактически приняли участие в реакции лишь ионы Ag+ и Сl-. Остальные ионы остались без изменения.
Пример 2. Составьте молекулярное и ионное уравнение реакции между: а) хлоридом железа (III) и гидроксидом калия; б) сульфатом калия и иодидом цинка.
Решение:
а) Составляем молекулярное уравнение реакции между FeCl3 и КОН:
FeCl3+3KOH =Fe (OH)3 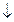 + 3KCl
+ 3KCl
По таблице растворимости устанавливаем, что из полученных соединений нерастворим только гидроксид железа Fe(OH)3. Составляем ионное уравнение реакции:
Fe 3+ +3Cl -+3K+ +3OH- =Fe (OH)3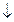 + 3K++3Сl-
+ 3K++3Сl-
В ионном уравнении показано, что коэффициенты 3, стоящие в молекулярном уравнении, в равной степени относятся к ионам. Это общее правило составления ионных уравнений. Изобразим уравнение реакции в краткой ионной форме:
Fe 3+ +3OH- = Fe(OH)3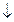
Это уравнение показывает, что в реакции принимали участие лишь ионы Fe3+ и ОН-.
б) Составим молекулярное уравнение для второй реакции:
K2SO4+ZnI2 = 2KI+ZnSO4
Из таблицы растворимости следует, что исходные и полученные соединения растворимы, поэтому реакция обратима, не доходит до конца. Действительно, здесь не образуется ни осадка, ни газообразного соединения, ни малодиссоциированного соединения. Составим полное ионное уравнение реакции:
2К++SO2-4+Zn2+ +2I- + 2К+ + 2I- +Zn 2+ +SO2-4
Пример 3. По ионному уравнению: Cu2+ +S2- -= CuS составить молекулярное уравнение реакции.
Решение:
Ионное уравнение показывает, что в левой части уравнения Должны быть молекулы соединений, имеющих в своем составе ионы Cu 2+ и S2-. Эти вещества должны быть растворимы в воде.
По таблице растворимости выберем два растворимых соединения, в состав которых входят катион Cu2+ и анион S2-. Составим молекулярное уравнение реакции между данными соединениями:
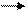 CuSO4+Na2S CuS+Na2SO4
CuSO4+Na2S CuS+Na2SO4
|
|
|
|
|
Дата добавления: 2014-10-22; Просмотров: 3317; Нарушение авторских прав?; Мы поможем в написании вашей работы!