
- Р Р‡.МессенРТвЂВВВВВВВВжер
- ВКонтакте
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ
- РњРѕР№ Р В Р’В Р РЋРЎв„ўР В Р’В Р РЋРІР‚ВВВВВВВВРЎР‚
- LiveJournal
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутренняя энергия системы. Энтальпия
|
|
|
|
Параметры состояния. Термодинамические процессы. Термодинамические функции.
Состояние системы определяется ее параметрами. В химической термодинамике рассматривают термодинамические параметры состояния: давление (P), объем (V), температуру (T) и концентрацию (C). Термодинамические параметры могут быть непосредственно измерены. Набор параметров P, V, T называют состоянием системы.
Изменение состояния системы называется термодинамическим процессом. В зависимости от условий протекания, процессы могут быть:
- изохорные - протекают при постоянном объеме системы (V = const);
- изобарные - протекают при постоянном давлении (P = const);
- изотермические - протекают при постоянной температуре (T = const):
- изохорно-изотермические (V = const и T = const);
- изобарно-изотермические (Р = const и T = const);
- адиабатические (теплота Q = 0), отсутствует теплообмен системы с окружающей средой.
Оценить ход процесса можно по изменению свойств системы или термодинамических параметров. При этом изменяются термодинамические функции, которые характеризуют процесс или состояние системы, т.е. термодинамические функции делятся соответственно на функции процесса и функции состояния.
К функциям процесса относятся теплота Q и механическая работа A, изменение которых зависит от условий и пути протекания процесса.
Теплота Q - это количественная мера хаотического движения частиц системы или тела. Энергия более нагретого тела передается в форме теплоты к менее нагретому. При этом переноса вещества не происходит.
Работа A - это количественная мера энергии, передаваемой от одной системы к другой за счет перемещения вещества под действием каких-либо сил.
К термодинамическим функциям состояния относятся: внутренняя энергия U, энтальпия H, энтропия S, энергия Гиббса G. Изменение этих функций зависит только от начального и конечного системы и не зависит от пути и способа проведения процесса. Величину термодинамических функций относят к 1 моль вещества.
Один из самых общих законов природы – закон сохранения энергии говорит, что энергия не возникает из ничего и не исчезает, она может лишь превращаться из одного вида в другой. Поэтому в изолированной системе запас энергии постоянен, независимо от протекающих в ней процессов.
Каждая система (тело, вещество, совокупность тел или веществ) обладает определенным запасом внутренней энергии U. Внутренняя энергия системы складывается из кинетической и потенциальной энергии частиц. Кинетическая энергия – это энергия поступательного, колебательного и вращательного движения частиц. Потенциальная энергия обусловлена силами притяжения и отталкивания между частицами. Во внутреннюю энергию системы не входят кинетическая энергия всей системы в целом и потенциальная энергия положения системы.
Внутреннюю энергию системы нельзя измерить. Она представляет собой способность системы к совершению работы или передаче теплоты. Можно определить ее изменение при переходе из начального состояния 1 в конечное состояние 2, т.е.
ΔU = U2 – U1,
где U2 и U1 – внутренняя энергия системы в конечном и начальном состояниях.
Так как химический процесс представляет собой превращение одних веществ в другие, запас внутренней энергии системы в ходе химического процесса должен меняться.
Если система получит из внешней среды теплоту Q и перейдет при этом из состояния 1 в состояние 2, то теплота будет расходоваться на изменение внутренней энергии ΔU и совершение системой работы против внешних сил А:
- математическое выражение первого закона термодинамики (частный случай закона сохранения энергии): Q = ΔU + А
Для химических реакций работой против внешних сил является работа против внешнего давления. Обычно она совершается за счет расширения системы, например, при выделении газа в ходе реакции (рис. 2).
Большинство химических реакций протекает при постоянном давлении (изобарный процесс) в открытом сосуде, поэтому реагирующие вещества могут расширяться. Поскольку увеличению объема системы препятствует внешнее давление Р, система должна совершать работу против внешнего давления:
А = p ΔV, где ΔV = V2 - V1, т.е. А = p(V2 - V1)
Тогда количество теплоты, полученное системой,
Qp = ΔU + pΔV; Qp = (U1 - U2) + p(V2 - V1) = (U2 + pV2) – (U1 + pV1)
Введем обозначение U + pV = Н, тогда
Qp= Н2 - Н1 = ΔН
Величину H = U + pV называют энтальпией.
Энтальпия системы – это теплосодержание или энергосодержание системы, численно она равна сумме внутренней энергии и произведения давления на объем.
Таким образом, для изобарного процесса выделение или поглощение теплоты равно изменению энтальпии системы: Qp = Δ H.
При изохорном процессе (V = const, Δ V = 0) изменения объема системы не происходит. Таким образом, для изохорных процессов теплота, сообщенная системе, расходуется только на изменение внутренней энергии системы:
Qv = U2 – U1= ΔН и, следовательно, изменение энтальпии и изменение внутренней энергии равны ΔН = ΔU.
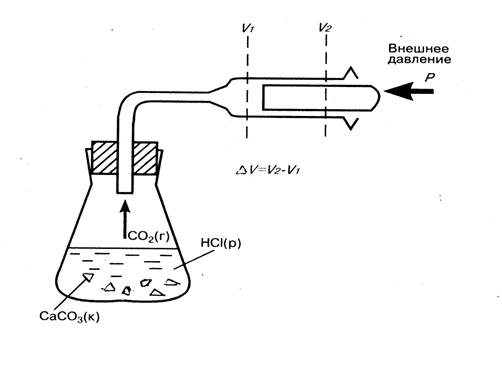
Рис. 2. Работа системы против внешнего давления
При изотермическом процессе температура системы остается постоянной, значит, изменения внутренней энергии не происходит ΔU = 0. При изотермическом процессе поглощенная теплота расходуется только на совершаемую системой механическую работу: Qt = A = p ΔV.
При адиабатном процессе теплообмена системы с окружающей средой не происходит, ΔQ = 0; тогда механическая работа будет совершаться только за счет убыли внутренней энергии системы: А = – ΔU.
|
|
|
Дата добавления: 2014-10-23; Просмотров: 1236; Нарушение авторских прав?; Мы поможем в написании вашей работы!