
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Количественное определение. Раствор формальдегида
|
|
|
|
Раствор формальдегида
Solutio Formaldehydi
Formalinum
Формалин
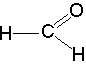
Метаналь
| М. м. 30,03 |
Получение. По методу Орлова – восстановлением метилового спирта, для чего пары спирта пропускают через раскаленную медную трубку, затем растворяют в воде до концентрации 36,5 – 37,5% (40% раствор формальдегида).
CH3OH + O → HCOH + H2O
Описание. Прозрачная бесцветная жидкость своеобразного острого запаха. Смешивается во всех соотношениях с водой и спиртом. Стабилизируют прибавлением метилового спирта, не более 1,0%.
Подлинность.
1) Реакция «серебряное зеркало»: к 2 мл раствора нитрата серебра прибавляют 10 — 12 капель раствора аммиака и 2 – 3 капли препарата, нагревают на водяной бане с температурой 50—60°; выделяется металлическое серебро в виде зеркала или серого осадка.
2) Реакция конденсации: к раствору 0,02—0,03 г салициловой кислоты в 5 мл концентрированной серной кислоты прибавляют 2 капли препарата и нагревают; появляется красное окрашивание.
Плотность 1,078—1,093.
Йодометрический метод, основанный на окислении формальдегида йодом: точную навеску помещают в колбу с притертой пробкой, прибавляют избыток 0,1М раствора йода и 1М раствор едкого натра, взбалтывают и оставляют в темном месте на 10 минут. Затем прибавляют 1М раствор серной кислоты и выделившийся йод титруют 0,1М раствором тиосульфата натрия до обесцвечивания (индикатор—крахмал).
J2 + 2NaOH = NaJ + NaJO + H2O
HCOH + NaJO + NaOH = HCOONa + NaJ + H2O
NaJO + NaJ + H2SO4 = J2 + Na2SO4 + H2O
J2 + 2Na2S2O3 = 2NaJ + Na2S4O6
УЧ = 1/2, формула обратного титрования
HCOH должно быть 36,5 – 37,5%
Хранение. В хорошо укупоренных склянках, в защищенном от света месте, при температуре не ниже 9°. При более низкой температуре формальдегид легко полимеризуется, образуя параформ,
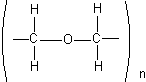
который выпадает в виде белого осадка. Параформ теряет фармакологическое действие формальдегида.
Применение. Антисептическое средство, наружно как дезинфицирующее для обработки рук, хирургического инструментария, спринцеваний, в качестве консерванта анатомических препаратов. Действие формальдегида основано на способности свертывать белок. Белковые вещества бактерий свертываются под влиянием HCOH, что приводит к их гибели. Являясь протоплазматическим ядом раствор формальдегида не может назначаться внутрь.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 6663; Нарушение авторских прав?; Мы поможем в написании вашей работы!