
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Мыс электролизі 3 страница
|
|
|
|
Сондықтан полярографиялық анализде қаныққан токтың мәні тек қана анықтайтын бөлшектердің концентрациясына тәуелді болуы үшін диффузиялық коэффициент пен капиллярдың сипаттамасы өзгермейтін жағдай жасау қажет. Кей жағдайда вольтамперлік қисықтың қаныққан токқа ауысқан жерінде токтың күрт өсуі байқалады, бұны полярографиялық максимум деп атайды (14.45-сурет).
Полярографиялық максимумның пайда болу себебі ретінде:
- сынаптың беті біркелкі поляризацияланбауын;
- сынап тамшысы айналасындағы ерітіндінің тамшы қозғалысына байланысты араласуын (яғни анықтайтын ионның электрод бетіне келу жылдамдығының артуын) айтуға болады.
| - E, B |
| I, MкА |
Полярографиялық максимумды жою үшін ерітіндіге органикалық беттік активті заттардың (БАЗ) аз мөлшерін қосады. Мысалы: желатин, агар-агар, столярлы клей, тағы басқалары.
Полярографиялық толқын теңдігі
Бұл теңдікті қисықтың АВ бөлігін (14.43-сурет) қолданып қорытып шығаруға болады. Бұл бөлікте Hg – электродының потенциалы мен ток күші бір-біріне байланысты екенін көруге болады. Потенциал теріс мәнге ауысқан сайын ток күші артады.
Егер электродта металл ионы тотықсызданса және бұл процесс қайтымды болса, электрохимиялық реакцияны былай жазуға болады:
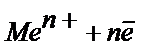
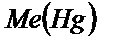
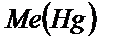 – металл амальгамасы. Егер бұл реакцияның жылдамдығы металл иондарының электрод бетіне тасымалдану жылдамдығына тең болса, онда ток күшінің мәні тотықсызданатын бөлшектердің концентрациясына тәуелді болады. Бұл жағдайда АВ – бөлігінің кез келген нүктесіне сәйкес потенциал:
– металл амальгамасы. Егер бұл реакцияның жылдамдығы металл иондарының электрод бетіне тасымалдану жылдамдығына тең болса, онда ток күшінің мәні тотықсызданатын бөлшектердің концентрациясына тәуелді болады. Бұл жағдайда АВ – бөлігінің кез келген нүктесіне сәйкес потенциал: 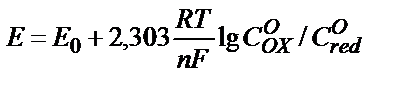
Нернст теңдігімен анықталады.
Бұндағы: 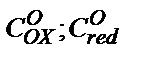 - тамшылы сынап электродының беткі қабатындағы анықтайтын ионның тотыққан және тотықсызданған түрлерінің концентрациялары.
- тамшылы сынап электродының беткі қабатындағы анықтайтын ионның тотыққан және тотықсызданған түрлерінің концентрациялары.
Полярографиялық толқынның АВ бөлігінде 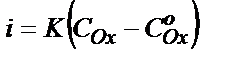 ал қаныққан токтың мәні I = K·COх. Осы теңдіктерден:
ал қаныққан токтың мәні I = K·COх. Осы теңдіктерден: 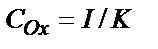 ; ал
; ал 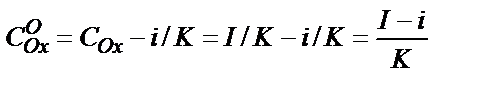 .
.
Екінші жағынан, полярографиялық толқынның кез келген нүктесінде ток күші заттың тотықсызданған түрінің концентрациясына тікелей пропорционалды: 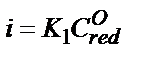 , бұдан
, бұдан 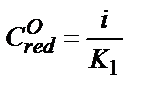 . Енді
. Енді 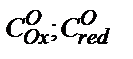 мәндерін Нернст теңдігіне қойып мынадай теңдік алсақ:
мәндерін Нернст теңдігіне қойып мынадай теңдік алсақ: 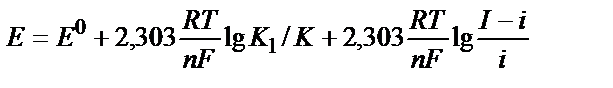 . K, K1 – анықтайтын заттың тотыққан және тотықсызданған түрлеріне сәйкес Илькович константалары.
. K, K1 – анықтайтын заттың тотыққан және тотықсызданған түрлеріне сәйкес Илькович константалары.
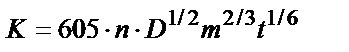

D – деполяризатордың тотыққан түрінің, ал D1 – деполяризатордың тотықсызданған түрінің диффузиялық коффициенттері. Яғни, басқаша айтқанда D1 – металл атомдарының сынаптағы, ал D – металл иондарының ерітіндідегі диффузиялық коэффициенттері.
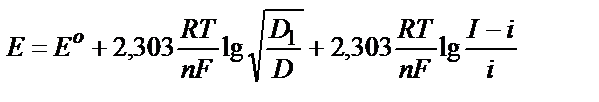
Полярографиялық толқындағы қаныққан токтың жартысына (i=I/2) сәйкес нүктені жартылай толқын потенциалы деп атайды.
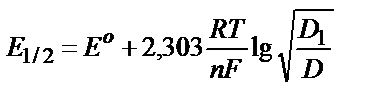 .
.
Жартылай толқын потенциалының мәні деполяризатор концентрациясына да, ток күшіне де тәуелді емес.
Сонымен полярографиялық толқын теңдігі:
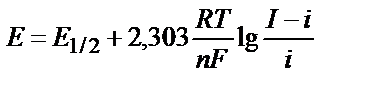 .
.
Оны график түрінде былай көрсетуге болады (14.47-сурет).
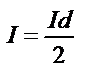
|
| I, МкА |
| E 1/2 |
| - E, B |
| a) |
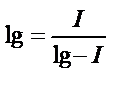
|
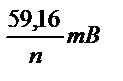
|
| E1/2 |
| + 1 |
| -1 |
| - E, B |
б)
14.47-сурет. Жартылай толқын потенциалын полярограммадан (а) және полярографиялық толқын теңдігі (б) бойынша анықтау
Е1/2 – жартылай толқын потенциалын сапалық анализде қолданады. Сандық поярографиялық анализді әртүрлі әдістермен жүргізуге болады. Полярографиялық жолмен заттың 10–3 – 10–6 моль/л мөлшерін анықтайды.
1) Градуирлеу графигін қолдану әдісі.
Бұл әдісте анықтайтын концентрацияны өлшенген диффузиялық токтың мәнінен градуирлі графикті қолданып табады. Градуирлі график алу үшін бірнеше стандартты ерітінді дайындап, олардың полярографиялық қисығын алады (14.48-сурет, а)). Әр концентрацияға сәйкес диффузиялық токтың мәнін табады. Содан соң абсцисса өсіне концентрацияның мәнін, ал ордината өсіне әр концентрацияға сәйкес диффузиялық токтың мәнін салып, диффузиялық ток – концентрация графигін алады. Бұл график координат осінің О – нүктесінен өтетін түзу сызық (14.48-сурет, б)).
| H, MM |
| с·104, М |
| а) |
| б) |
14.48-сурет. Стандартты ерітінділерді қолданып концентрацияны анықтаудың градуирленген графигі
2) Стандартты ерітінді әдісі. Бұл әдіс анализдейтін заттың концентрациясын оның диффузиялық тогын концентрациясы белгілі стандартты ерітіндінің (Сст) диффузиялық тогымен салыстырып табады. Ол үшін екі ерітіндінің поляризациялық қисығын бірдей жағдайда алады, яғни: бірдей капилляр, бірдей фон, to= const және гальванометрдің сезімталдығы да тұрақты болуы қажет. Сст -ға сәйкес диффузиялық ток – Iст, ал Сх –қа сәйкес диффузиялық ток – Iх болса, онда Сх=Iх·Cст/Iст.
3) Стандартты қосу әдісі.
Алдымен анализдейтін ерітіндінің полярографиялық қисығын алады, содан соң осы ерітіндіге концентрациясы белгілі анықтайтын заттың қаныққан токты екі есе арттыратындай мөлшерін қосып, екінші поляризациялық қисықты алады. Бұл жағдайда алғашқы қаныққан токтың мәні (I) қосылған стандарттың концетрациясына (DС) пропорционалды (D I) өседі. Осындай D I / I =DС/С; С=DС· I /D I – анықтайтын заттың концентрациясын табады.
Полярографиялық анализді жүргізу үшін әртүрлі полярографтар ППТ–1, ПУ–1 қолданады.
14.5.2 Амперометриялық титрлеу әдісі
Амперометриялық титрлеу әдісі – бұны анализдің титрлеу әдісі деп те немесе полярографиялық әдістің бір түрі деп те айтса болады. Амперометриялық әдіс – ток күшінің ерітіндідегі электрохимиялық реакцияға қатысатын иондар концентрациясына тәуелділігіне негізделген. Амперометриялық титрлеу мен полярография арасындағы байланысты былай көрсетуге болады (14.49-сурет).
| • • |
| I, мкA |
| Е1 Е, В |
| С1 С2 С3 С4 |
| V, мл |
| а) |
| б) |
14.49-сурет. Электрактивті заттың С1 > С2 > С3 > С4 концентрацияларына сәйкес вольтамперограммалары (а) және (б) электродтық потенциалдың Е1 мәніндегі осы заттың амперометриялық титрлеу қисығы
Амперометриялық титрлеуде әртүрлі реакциялар қолданылады: 1) тұндыру реакциялары, мысалы: калий ферроцианидімен титрлеу; 2) тотығу-тотықсыздану реакциясы, мысалы: ванадат иондарын екі валентті темір иондарымен титрлеу; 3) комплекс түзу реакциялары, мысалы: Ca2+ ионын натрийдің этилендиаминтетраацетаты (ЭДТА) – ерітіндісімен титрлеу.
Амперометриялық әдісте электрохимиялық реакцияға анықталатын реагент пен титранттың біреуінің қатысуы жеткілікті. Осыған байланысты әртүрлі титрлеу қисықтарын алуға болады.
Егер электрохимиялық реакцияға анықталатын ион қатысатын болса, титрант қосқан кезде тұнба немесе нашар диссоциацияланатын заттар түзіліп, анықталатын зат концентрациясы кемиді. Осыған байланысты I – күші де кемиді (14.50-сурет (а)). Мысалы:
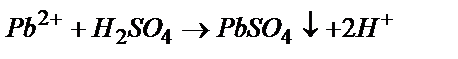
Анықталатын зион электродта тотығу-тотықсыздану реакциясына қатыспайтын жағдайда электродта тотығып немесе тотықсызданатын титрант қолданылады. Мысалы:
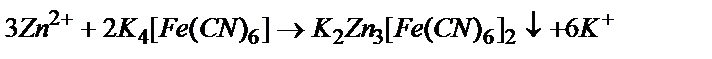
Бұл жағдайда титрлеу қисығының түрі төмендегідей болады (14.50-сурет (б)).
Кейде анықталатын ионда, титрантта электрохимиялық реакцияға қатысуы мүмкін. Бұндай жағдайда ток күші алдымен кемиді де, эквиваленттік нүктеден кейін ток күші қайтадан өсе бастайды (14.50-сурет (в)). Мысалы,
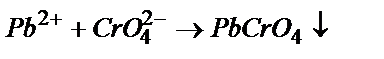
| I, мкA |
| I, мкA |
| V, мл |
| V, мл |
| а) |
| б) |
| в) |
| I, мкA |
| V, мл |
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 1223; Нарушение авторских прав?; Мы поможем в написании вашей работы!