
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вопросы и задачи для самостоятельной работы. 1. Составьте формулы оксидов лития, кальция, алюминия, кремния,
|
|
|
|
1. Составьте формулы оксидов лития, кальция, алюминия, кремния,
азота (V), серы (VI), хлора (VII), хрома (VI), железа (II), железа (III), азота (II), азота (I) и укажите, к какому типу оксидов они относятся?
2. Дайте химические названия оксидов: B2O3, K2O, CrO3, CrO, P2O5, Cu2O, PbO2, NiO, CO2, Ag2O.
3. Сравните химические свойства оксидов:
а) CO и CO2 б) Na2O и MgO в) FeO и Fe2O3
Ответ подтвердите составлением соответствующих уравнений реакций.
4. Какие кислоты соответствуют следующим кислотным оксидам: SiO2, P2O5, N2O5, N2O3?
5. Приведите примеры бескислородных и кислородных кислот. Дайте химические названия следующих кислот:
HCl, H2CO3, H2CrO4, H2SO3, H2SiO3, H2S.
6. С какими из указанных веществ будет реагировать серная кислота:
Ca(OH)2, CO2, K2O, BaCl, Cu(NO3)2, H3PO4, Fe2O3?
Составьте уравнения протекающих реакций.
7. Укажите, какие из указанных оснований являются растворимыми, а какие – труднорастворимыми в воде: KOH, Ba(OH)2, Al(OH)3, Mg(OH)2, Fe(OH)2, Cr(OH)3, NH4OH, Zn(OH)2. Какие основания называются щелочами? Какие из указанных оснований к ним относятся?
8. Напишите уравнения реакций получения NаОН, Ba(OH)2, исходя:
1) из металлов натрия и бария;
2) из их оксидов.
9. Составьте уравнения реакций между соответствующими кислотами и основаниями (или амфотерными гидроксидами), приводящие к образованию следующих солей:
PbI2, KHCO3, CaHPO4, MgSO4, AlOHCl2, (MgOH)2CO3.
10. Составьте уравнения перевода нижеследующих кислых солей в средние: Mg(HCO3)2, K2HPO4, KH2PO4, NaHS.
11. Как перевести основные соли в средние соли:
CuOHCl, FeOHNO3, MgOHBr, Al(OH)2Cl? Напишите уравнения реакций.
12. Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) BaO → Ba(OН)2 → BaCl2 → Ba(NO3)2 → BaSO4 → H2[Ba(SO4)2],
б) Fe → Fe2O3 → FeCl3 → Fe(NO3)3 → Fe(OH)3 → Fe2O3 → NaFeO2,
в) Cu ← CuO → CuSO4 → Cu(OH)2 → CuО → K2CuO2 → CuСl2,
г) K → KOH → KHS → K2S → FeS → SO2 → KHSO3,

 д) CaO → CaCl2
д) CaO → CaCl2


 Ca
Ca
Ca(OH)2 → Ca(NO3)2.
13. Напишите полные и краткие ионные уравнения следующих реакций:
а) Ca(NO3)2 + K2CO3 → CaCO3 + 2KNO3,
б) 2HNO3 + Ba(OH)2 → Ba(NO3)2 + 2H2O,
в) Ba(NO3)2 + K2SO4 → BaSO4 + 2KNO3,
г) K2CO3 + 2HCl → 2KCl + H2O + CO2,
д) Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2,
е) 2NaOH + Fe(NO3)2 → Fe(OH)2 + 2NaNO3,
ж) Pb(NO3)2 + K2SO4 → PbSO4 + 2KNO3,
з) Na2SiO3 + Ba(OH)2 → BaSiO3 + 2NaOH,
и) FeCl3 + 3CsOH → Fe(OH)3 + 3CsCl,
к) 3FeSO4 + 2Na3PO4 → Fe3(PO4)2 + 3Na2SO4.
14. Составьте молекулярные и ионные уравнения реакций между веществами:
| a) KOH и MgCl2, | е) Pb(OH)2 и HNO3, |
| б) NaOH и H2SO3, | ж) Na2SO4 и BaCl2, |
| в) K2S и HCl, | и) Na2CO3 и HCl, |
| г) CH3COOК и H2SO4, | к) H2SiO3 и KOH, |
| д) KHCO3 и H2SO4, | л) Fe(OH)Cl и HNO3. |
15. Составьте молекулярные уравнения реакций по кратким ионным уравнениям:
а)  ; ;
| е)  ; ;
|
б)   ; ;
| ж)  ; ;
|
в)   ; ;
| и)  ; ;
|
г)   ; ;
| к)  ; ;
|
д)  ; ;
| л)  . .
|
16. Закончите уравнения реакций: Напишите в молекулярной и ионной форме уравнения реакций:
| 1) CO2 + NaOH → _________________, | 6) CaCl2 + Na2CO3 → ______________, |
| 2) P2O5 + NaOH → ________________, | 7) Pb(NO3)2 + 2KI → _______________, |
| 3) HNO2 + O2 → __________________, | 8) BaCl2 + Na2CrO4 → _____________, |
| 4) MnCl2 + Na2S → ________________, | 9) KH2PO4 + HCl → _______________, |
| 5) H3PO4 + 3NaOH → ______________, | 10) Fe(OH)Cl2 + KOH → ___________. |
17. Определите тип солей и дайте им названия:
Na3PO4; FeCl2; Na2HPO4; FeOHCl; NaH2PO4; Fe(OH)2NO3; Na2CO3; (CuOH)2CO3; NaHCO3; NiSO4; PbI2; NaHS; Cr2S3; K4[Fe(CN)6]; [Al(OH2)6]Cl3.
18. Напишите формулы солей: сульфат калия; гидросульфат натрия; метасиликат натрия; гидроксохлорид цинка; гидроксокарбонат магния; сульфат алюминия; гидроксосульфат алюминия; сульфат аммония железа (ΙΙΙ).
19.Составьте уравнения реакций, протекающих в следующей цепи превращений:
 K[Fe(OH)4]
K[Fe(OH)4]
↑
Fe → FeCl3 → Fe(OH)Cl2 → Fe(OH)3 → Fe2O3 → Fe2(SO4)3 → FeSO4 → Fe.
20. Амфотерность указанных ниже гидроксидов проявляется в том, что они:
| 1) гидроксида бериллия | а) взаимодействуют с растворами щелочей |
| 2) гидроксида цинка | б) при прокаливании превращаются в амфотерные оксиды |
| 3) гидроксида алюминия | в) взаимодействуют с растворами кислот и щелочей |
| 4) гидроксида олова (ΙΙ) | г) взаимодействуют с растворами кислот |
| 5) гидроксида свинца (ΙΙ) | д) растворяются в воде |
| 6) гидроксида хрома (ΙΙΙ) | е) проявляют кислотные свойства |
| 7) гидроксида меди (ΙΙ) | |
| 8) гидроксида железа (ΙΙΙ) | |
| 9) гидроксида титана (ΙV) | |
| 10) гидроксида марганца (ΙV) |
21. Напишите уравнения диссоциации электролитов:
| 1) H3BO3; Be(OH)2; Cu(OH)Cl, | 6) H2CO3; Al(OH)3; KHCO3, |
| 2) H3PO4; KH2PO4; Ca(OH)2, | 7) H4SiO4; Na2HPO4; Ni(OH)2, |
| 3) Ba(OH)2; H2S; MgOHCl, | 8) KHS; NaHSO3; H2SO4, |
| 4) Mn(OH)2; H2CO3; KHCO3, | 9) CuCl2; CuOHCl; Fe(OH)3, |
| 5) KH2PO4; H2S; Fe(OH)3, | 10) Al(OH)2Cl; K2HPO4; H3BO3. |
22. Вычислите эквивалент кислот и оснований в следующих уравнениях реакций:
1) H2SO4 + KOH → KHSO4 + H2O,
2) H2SO4 + Ca(OH)2 → CaSO4 + 2H2O,
3) Al(OH)3 + HCl → Al(OH)2Cl + H2O,
4) Al(OH)3 + H2SO4 → Al(OH)SO4 + 2H2O,
5) Al(OH)3 + H3PO4 → AlPO4 + 3H2O,
6) H3PO4 + Ba(OH)2 → BaHPO4 + 2H2O,
7) H3PO4 + KOH → KH2PO4 + H2O,
8) Mg(OH)2 + HNO3 → Mg(OH)NO3 + H2O,
9) Mg(OH)2 + H2CO3 → MgCO3 + 2H2O,
10) Fe(OH)3 + 2HNO3 → Fe(OH)(NO3)2 + 2H2O.
 2.8 Входной тестовый контроль
2.8 Входной тестовый контроль
Вариант № 1
Дополните:
1. Оксидами называются _____________________________________________
2. Кислые соли состоят _______________________________________________
3. Щелочи можно получить ___________________________________________
Выберите правильный ответ:
4. Ряд, в котором представлены только соли ____________________________
1) KMnO4; H2SO4; K[Al(OH)4],
2) KClO4; Mn(NO3)2; Pb(OH)2,
3) Na3PO4; K2[Zn(OH)4]; MnCl2,
4) Ca(OH)2; KMnO4; NaClO.
5. Число кислот среди перечисленных веществ: H2[PtCl6]; KH2PO4; HClO; Na4SiO4; H2CO3; H3AsO4; NaH; HCl равно:
1) 2; 2) 3; 3) 4; 4) 5.
6. К кислотным оксидам относятся 1) CO2; PbO; 3) Mn2O7; SO2;
2) SO3; CrO3; 4) CaO; MnO.
7. Оксид алюминия относится к _____________________________________
1) основным оксидам; 3) амфотерным оксидам;
2) кислотным оксидам; 4) безразличным оксидам.
8. Установите соответствие между названием вещества и его принадлежностью
к определенному классу неорганических соединений:
| Название | Класс |
| А) сероводород | 1) простое вещество |
| Б) гашеная известь | 2) бинарное соединение |
| В) питьевая сода | 3) оксид |
| Г) медный купорос | 4) гидроксид |
| 5) соль | |
| 6) основание |
9. Слабыми кислотами являются _______________________________________
1) HClO; 2) HMnO4; 3) CH3COOH;
4) HClO4; 5) H2CO3; 6) H2SO4.
10. Для осуществлений цепочки превращений
Ca → CaO → Ca(OH)2 → CaCl2 → Ca3(PO4)2 → P → P2O3 необходимо последовательно использовать следующие вещества:
1) H2O; K3PO4; SiO2 и C; O2; HCl.
Составьте уравнения протекающих реакций.
Вариант № 2
Дополните:
1. Гидроксиды – это _________________________________________________
2. Основные соли состоят _____________________________________________
3. Основания можно получить _________________________________________
Выберите правильный ответ:
4. Ряд, в котором представлены только основания _______________________
1) Ca(OH)2; Pb(OH)2; H2SO4;
2) KMnO4; HClO4; PbCl2;
3) HClO4; Al(OH)3; KNO3;
4) Mn(OH)2; Ba(OH)2; Fe(OH)2.
5. Число гидроксидов среди перечисленных веществ: HClO; Mn(OH)2; (CuOH)2CO3; KH; Al(OH)3; H2[Ba(SO4)2]; PbCO3; Ba(OH)2; HCl равно:
1) 3; 2) 5; 3) 7; 4) 9.
6. К амфотерным гидроксидам относятся:
1) Al(OH)3; Ba(OH)2; 3) Zn(OH)2; KOH;
2) Pb(OH)2; Cu(OH)2; 4) Be(OH)2; Cr(OH)3.
7. Гидроксид бария проявляет только _________________________________
1) основные свойства; 3) амфотерные свойства;
2) кислотные свойства; 4) не проявляет кислотно-основных свойств.
8. Установите соответствие между формулой вещества и его принадлежностью
к определенному классу неорганических соединений:
| Название | Класс |
| А) KHCO3 | 1) бинарное соединение |
| Б) CrO3 | 2) кислота |
| В) Ba(OH)2 | 3) кислая соль |
| Г) HClO3 | 4) оксид |
| 5) щелочь | |
| 6) амфотерный гидроксид |
9. Термически неустойчивы и разлагаются при нагревании ________________
1) K2CO3; 2) KNO3; 3) K[Al(OH)4];
4) Cu(OH)2; 5) HCl; 6) Cr(OH)3.
10. В схеме превращений
K 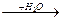 X1
X1  X2
X2 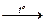 X3
X3 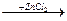 X4
X4 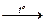 Х5 являются ___________
Х5 являются ___________
1) вода; 2) оксид кальция; 3) щелочь; 4) оксид углерода (ΙV);
5) кислая соль; 6) карбонат кальция.
Составьте уравнения протекающих реакций.
Вариант № 3
Дополните:
1. Основными оксидами называются __________________________________
2. Двойные соли состоят ______________________________________________
3. Кислородные кислоты можно получить _______________________________
Выберите правильный ответ:
4. Ряд, в котором представлены только гидроксиды _____________________
1) НClO4; Al(OH)3; Вa(OH)2;
2) H2SO4; K[Al(OH)4]; MnCl2;
3) H2CO3; BaCO3; Al(OH)3;
4) НClO3; Fe(OH)3; PbSO4.
5. Число солей среди перечисленных веществ: HClO; K[Al(OH)4]; MnO2; Na2SO4; KH2PO4; Pb(OH)2; (CuOH)2CO3; Ca(OCl)Cl; BaO равно:
1) 3; 2) 5; 3) 7; 4) 9.
6. К основным оксидам относятся 1) CaO; MgO; 3) SnO; SO2;
2) MnO; PbO; 4) BaO; MnO.
7. Гидроксид бериллия проявляет только ______________________________
1) основные свойства; 3) амфотерные свойства;
2) кислотные свойства; 4) свойства сильных электролитов.
8. Установите соответствие между названием вещества и его принадлежностью
к определенному классу неорганических соединений:
| Название | Класс |
| А) оксид азота (ΙΙΙ) | 1) основной оксид |
| Б) гидроксид аммония | 2) кислотный оксид |
| В) хлорид бария | 3) основная соль |
| Г) сероводород | 4) средняя соль |
| 5) щелочь | |
| 6) бинарное соединение |
9. Продуктами реакции, протекающей между ортофосфорной кислотой и гидроксидом калия являются __________________________________________
1) K3PO4; 2) H2O; 3) KH2PO4; 4) K2HPO4;
5) H2; 6) O2; 7) P2O5; 8) KCl.
10. В схеме превращений РН3 → Х → КРО3 → Н3РО4 → Са(РО4)2 → Р
пропущеновещество Х, которое называется _____________________________
1) оксид фосфора (ΙΙΙ); 2) оксид фосфора (V);
3) фосфор; 4) фосфид водорода.
Составьте уравнения протекающих реакций.
Вариант № 4
Дополните:
1. Основаниями называются _________________________________________
2. Смешанные соли состоят ___________________________________________
3. Амфотерные гидроксиды можно получить ____________________________
Выберите правильный ответ:
4. Ряд, в котором представлены только кислые соли _____________________
1) KHCO3; CaSO4; K[Al(OH)4];
2) NaH2PO4; KHS; Mn(HCO3)2;
3) KHS; НClO4; Ca(OH)2;
4) KНCO3; K2[Zn(OH)4]; MnCl2.
5. Число щелочей среди перечисленных веществ: K2O2; NH4OH; Mg(OH)2; KClO; Ba(OH)2; Mn(OH)2; NaOH; CaCO3 равно:
1) 3; 2) 4; 3) 5; 4) 8.
6. К амфотерным оксидам относятся _________________________________
1) MgO; ВaO; 2) SO3; СO2;
3) Al2O3; ВеO; 4) PbO; ZnO.
7. Оксид серы (VΙ) проявляет только _________________________________
1) основные свойства; 3) амфотерные свойства;
2) кислотные свойства; 4) свойства безразличного оксида.
8. Установите соответствие между формулой вещества и его принадлежностью
к определенному классу неорганических соединений:
| Название | Класс |
| А) K[Al(OH)4] | 1) двойная соль |
| Б) MgNH4PO4 | 2) основная соль |
| В) (CuOH)2CO3 | 3) средняя соль |
| Г) KH2PO4 | 4) кислая соль |
| 5) комплексная соль | |
| 6) смешанная соль |
9. Хлорид железа (ΙΙΙ) получают реакцией _______________________________
1) Fe + Cl2 2) Fe + HCl 3) Fe2O3 + H2O
4) FeO + HCl 5) Fe2O3 + KOH 6) Fe2O3 + HCl
10. Конечным веществом в цепочке превращений на основе азота:
HNO3 (конц.)  Х1
Х1  Х2
Х2  Х3
Х3  является ___________
является ___________
1) нитрит калия; 2) оксид азота (Ι);
3) оксид азота (ΙV); 4) гидроксид аммония.
Составьте уравнения протекающих реакций.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 2875; Нарушение авторских прав?; Мы поможем в написании вашей работы!