
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термины и определения в химии
|
|
|
|
(номенклатура неорганических соединений ИЮПАК)
(глоссарий)
| Термин | Определение |
| Аллотропия | Способность атомов одного и того же элемента к образованию нескольких простых веществ |
| Атом | Электронейтральная частица, состоящая из положительно заряженного атомного ядра и отрицательно заряженных электронов |
| Гидроксиды | Сложные вещества – продукты взаимодействия оксидов с водой (это условное определение, т.к. большинство основных оксидов с водой не взаимодействуют) |
| Бинарные соединения | Сложные вещества, молекулы которых состоят из атомов двух элементов, кроме оксидов |
| Ионные реакции | Реакции, протекающие между ионами |
| Кислоты | Сложные вещества, состоящие из водорода и кислотного остатка. Электролиты, дающие при диссоциации в качестве катионов только катионы водорода 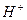
|
| Металлические вещества | Простые вещества, которые в химических реакциях проявляют свойства восстановителей (или восстановительные свойства), отдавая электроны |
| Моль вещества | Количество вещества, содержащее столько молекул, атомов, ионов, электронов или других структурных единиц, сколько содержится атомов в 12 г (0,012 кг) изотопа углерода 12С |
| Молярная масса | Величина, равная отношению массы вещества к количеству вещества |
| Неметаллические вещества | Простые вещества, которые в химических реакциях проявляют свойства, как окислителя, так и восстановителя, т.е. они способны как принимать, так и отдавать электроны |
| Необратимые химические реакции | Химические реакции, которые протекают в одном направлении и завершаются полным превращением исходных реагирующих веществ в конечные вещества (образующиеся продукты уходят из сферы реакции – выпадают в виде осадка, выделяются в виде газа, образуются малодиссоцированное соединение или реакция сопровождается большим выделением энергии) |
| Обратимые химические реакции | Химические реакции, которые одновременно протекают в двух взаимно противоположных направлениях |
| Оксиды | Сложные вещества, молекулы которых состоят из атомов двух элементов, один из которых кислород в степени окисления (– 2) |
| Продолжение приложения Д | |
| Основания | Соединения, в которых положительно заряженный ион металла связан с отрицательно заряженным одним или несколькими гидроксид – ионами. Электролиты при диссоциации которых в качестве анионов образуют только гидроксид – ионы |
| Относительная атомная масса элемента, Аr | Величина равная отношению массы атома данного элемента к 1/12 массы изотопа углерода 12С |
| Относительная молекулярная масса вещества, Мr | Величина равная отношению массы молекулы данного вещества к 1/12 массы изотопа углерода 12С |
| Простые вещества | Вещества, молекулы которых состоят из атомов одного элемента |
| Реакции замещения | Реакции между простыми и сложными веществами, в результате которых атомы простого вещества замещают атомы сложного вещества |
| Реакция нейтрализации | Реакция между кислотой и основанием |
| Реакции обмена | Реакции, в результате которых два вещества обмениваются своими ионами, образуя два новых вещества |
| Реакции разложения | Реакции, в результате которых из одного вещества образуется несколько новых |
| Реакции соединения | Реакции, в результате которых из двух или нескольких веществ образуется одно новое вещество |
| Сложные вещества | Вещества, молекулы которых состоят из атомов двух или более элементов |
| Соли | Продукты полного или частичного замещения водорода в кислотах на ион металла; или полного или частичного замещения гидроксид – ионов в основаниях или амфотерных гидроксидах на кислотные остатки |
| Соли средние (или нормальные) | Продукты полного замещения катионов водорода в молекуле кислоты на ионы металла, или продукты полного замещения гидроксильных групп в молекуле основания (амфотерного гидроксида) на кислотные остатки |
| Соли кислые | Продукты неполного замещения атомов водорода в молекулах многоосновных кислот на ионы металла |
| Соли основные | Продукты неполного замещения гидроксид-ионов в многокислотных основаниях (или амфотерных гидроксидов) на кислотные остатки |
| Соли двойные | Состоят из ионов двух различных металлов и кислотных остатков одной и той же кислоты |
| Соли смешанные | Состоят из катионов одного металла и кислотных остатков двух различных кислот и могут быть образованы при взаимодействии солей двух различных кислот одного и того же металла |
| Комплексные соли | Состоят из сложного комплексного иона – внутренней сферы, которая заключена в квадратные скобки, и внешней сферы |
| Степень окисления | Условный заряд, который приписывается атому, исходя их предположения, что молекула соединения состоит только из ионов, и при этом электронейтральна. |
| Продолжение приложения Д | |
| Химические реакции |  Химические взаимодействия веществ Химические взаимодействия веществ
|
| Химические уравнения | Изображение реакций при помощи химических формул и математических знаков |
| Химический элемент | Вид атомов, характеризующихся определенной совокупностью свойств |
| Щелочи | Растворимые в воде основания |
| Эквивалент | Реальная или условная частица вещества, которая в данной реакции эквивалентна атому или иону водорода, т.е. соединяется с одним атомом или ионом водорода либо замещает его |
| Эквивалентная масса (молярная масса эквивалента вещества) | Масса одного эквивалента данного вещества |
| Экзотермические химические реакции (∆Н < 0) | Химические реакции, происходящие с выделением теплоты (энергии), теплосодержание системы уменьшается |
| Эндотермические химические реакции (∆Н > 0) | Химические реакции, происходящие с поглощением теплоты (энергии), теплосодержание системы возрастает |
Учебное издание
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 1110; Нарушение авторских прав?; Мы поможем в написании вашей работы!