
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные реакции алициклических углеводородов
|
|
|
|
Некоторые способы получения циклоалканов
| Название реакции | Примеры |
| 1. Действие цинковой пыли на спиртовый раствор дигалогенпроизводного алкана 2. Пиролиз кальциевых солей двухосновных кислот 3. Гидрирование бензола и его гомологов 4. Присоединение этилена или ацетилена к алкадиену 5. Пиролиз циклоалкенов | ClH2C – CH2 – CH2Cl + Zn → ZnCl2 +

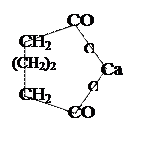   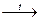 CaCO3+ CaCO3+

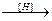 C5H10
циклопентан
С6Н5 – СН3 C5H10
циклопентан
С6Н5 – СН3 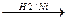 С6Н11СН3
метилциклогексан
СН=СН2 СН2
│ + ║ С6Н11СН3
метилциклогексан
СН=СН2 СН2
│ + ║ 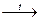 С6Н10
СН=СН2 СН2
циклогексан
С5Н8 С6Н10
СН=СН2 СН2
циклогексан
С5Н8 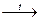 С5Н6 + Н2
циклопентен циклопентадиен С5Н6 + Н2
циклопентен циклопентадиен
|
Таблица 10
| Название реакции | Примеры |
| 1. Раскрытие циклов 2. Замещение 3. Окисление 4. Каталитическая дегидрогенизация (реакция Зелинского) |    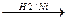 СН3 – СН2 –СН3
циклопропан СН3 – СН2 –СН3
циклопропан
 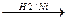 СН3–СН2–СН2–СН3
циклобутан
C5H10 + Br2 → C5H9Br + HBr СН3–СН2–СН2–СН3
циклобутан
C5H10 + Br2 → C5H9Br + HBr
 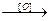 СН2 – СН2 – СООН
циклогексан │ + Н2О
СН2 – СН2 – СООН
адипиновая кислота
С6Н11СН3 СН2 – СН2 – СООН
циклогексан │ + Н2О
СН2 – СН2 – СООН
адипиновая кислота
С6Н11СН3 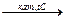 С6Н5СН3 + 3Н2
метилциклогексан толуол С6Н5СН3 + 3Н2
метилциклогексан толуол   
|
Ненасыщенные (непредельные) углеводороды ряда этилена (алкены)
Углеводороды, в молекулах которых атомы углерода связаны друг с другом двойной связью, называются ненасыщенными или непредельными углеводородами ряда этилена (олефинами, алкенами). Общая формула этиленовых углеводородов CnH2n. Атомы углерода в таких углеводородах находятся во втором валентном состоянии, которому соответствует sp2- гибридизация.
Двойная связь (С=С) состоит из одной простой (σ-связи) и одной π-связи. Простая связь расположена в плоскости, в которой находятся все ядра атомов углерода и водорода. Вторая связь (π-связь) образуется за счёт перекрывания двух негибридизированных 2р-электронных облаков атомов углерода и лежит в плоскости, перпендикулярной плоскости π-связи.
Ненасыщенные соединения, содержащие в молекуле две двойные связи, называются диеновыми углеводородами (алкадиенами, или диолефинами). Общая формула таких соединений CnH2n-2. Если двойные связи расположены рядом (при одном атоме углерода), то такие диеновые углеводороды называются кумулированнми или алленовыми, например, СН2=С=СН2 – пропадиен (аллен).
Если двойные связи разделены одной простой, то углеводороды называются сопряжёнными или кумулированными: СН2=СН – СН=СН2 – бутадиен -1,3 (дивинил).
Если двойные связи разделены двумя или несколькими простыми связями, то непредельные углеводороды называются изолированными или несопряжёнными:
СН2=СН – СН2 – СН2 – СН =СН2 гексадиен -1,5.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 738; Нарушение авторских прав?; Мы поможем в написании вашей работы!