
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Конспект лекційного заняття. Окси- , альдегідо- і кетокислоти
|
|
|
|
Основні поняття
Окси-, альдегідо- і кетокислоти. Таутомерія. Оптична ізомерія.
Оксиальдокислоти, оксикетокислоти, таутомерія, оптична ізмерія, L – ізомери, D – ізомери, a – ізомери, b – ізомери.
План лекційного заняття:
1. Класифікація оксикислот.
2. Властивості оксикислот.
3. Добування та застосування.
4. Стереохімія вуглецю.
5. Оптична ізомерія.
Література:
1. Ластухін Ю.О., Воронов С.А. Органічна хімія. – Львів: Центр Європи, 2001. – С. 71-127, 190-200.
2. Нейланд О.Я. Органическая химия. – М.: Высшая школа, 1990. – С. 9-13, 22-38, 59-61, 81-85, 86-89, 92-95, 103-105, 130, 145, 177-179, 225-228.
3. Перекалин В.В., Зонис С.А. Органическая химия. – М.: Просвещение, 1972. – С. 6-17, 18-25, 29-38, 47-48, 54-58, 76, 78-79, 105, 160-161, 177-179.
4. Петров А.А., Бальян Х.В., Трощенко А.Б. Органическая химия. – М.: Высшая школа, 1973. – С. 5-11, 20-43, 44-48, 64-65, 248-257.
5. Чирва В.Я., Ярмолюк С.М., Толкачова Н.В., Земляков О.Є. Органічна хімія. – Львів: БаК, 2009. – С. 81-131.
Оксикислотами називаються похідні вуглеводнів, маючі у молекулі два види
О
½½
функціональних груп: гідроксильні ОН та карбоксильні - С - ОН -. У залежності від кількості карбоксильних груп відрізняють одно-, двух- та багатоосновні оксикислоти, а від числа гідроксильних груп - двух-, трьох- та багатоатомні оксикислоти.
По будові вуглецевого радикалу, з яким пов'язані оксі- та карбрксильні групи, оксикислоти діляться на аліфатичні (насичені та ненасичені), ароматичні, гетероцекличні та інші:
НО-СН2-СООН гліколева, оксіоцтова (одноосновна, двуатомна оксикислота)
ОН
½
СН3-СН-СООН молочна (одноосновна, двуатомна оксикислота)
НООС-СН-СН2-СООН яблучна (двухосновна, трьохатомна оксикислота)
½
ОН
НООС-СНОН-СНОН-СООН винна (двухосновна, чотирьохатомна оксикислота)
СООН галлова (одноосновна, чотирьохатомна ароматична оксикислота)
 ½
½
 | |||||
 |  |
 НО ОН
НО ОН
ОН
ОН
½
НООС-СН2-С-СН2-СООН лимонна (трьохосновна, чотирьохатомна оксикислота)
½
СООН
Фізичні властивості. Оксикислоти - безбарвні тягучі рідини чи кристалічні речовини. Нижчі добре розчинні у воді, зі збільшенням молекулярної маси розчинність зменшується.
Хімічні властивості. Оксикислоти взаємодіють з багатьма хімічними реакціями, характерних для кислот (присутність групи СООН) та спиртів (присутність групи ОН). Будова вуглецевого радикалу теж оказується на їх хімічній поведінці - ароматичні оксикислоти вступають у перетворення, характерні для відповідних похідних бензолу. У одних хімічних реакціях кожна з функціональних груп може приймати участь незалежно друг від друга. а в інших хід реакції та характер продуктів, які утворилися, залежить від їх взаємного впливу, у деяких випадках оксі- та карбоксильні групи можуть взаємодіяти між собою.
Кислотні властивості. Введення у молекулу кислоти оксігрупи підвищує силу кислоти: оксикислоти - більш сильні, чим відповідні їм карбонові кислоти.
Вони можуть утворювати солі, складні ефіри, аміди, галогенангідріди. У реакції з РСІ5 може взаємодіяти і спиртова група.
Спиртові властивості. Можливо окиснення вторинної спиртової групи з утворенням кетокислоти (1); заміна спиртової групи на атом галогену (2); утворення простих ефірів (3); складних ефірів (4):
О
½½

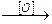 СН3-С-СООН (1)
СН3-С-СООН (1)
 СН3-СН-СООН (2)
СН3-СН-СООН (2)
½
СІ
ОН
½
 СН3-СН-СООН
СН3-СН-СООН  СН3-СН-СООН (3)
СН3-СН-СООН (3)
½
ОСН3
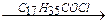 СН3-СН-СООН (4)
СН3-СН-СООН (4)
½
ОСОС17Н35
Різниця у поведінці a-,b-,g - та d-оксикислот.
а) Дегідратація a- оксикислот. При нагріванні a- оксикислот виділяється вода та утворюється циклічний складний ефір - лактид:
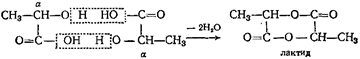
Лактиди - кристалічні речовини, які розлагаються при кип’ятінні у присутності кислот та лугів на вихідних продуктах.
б) b- Оксикислоти при нагріванні втрачають воду з утворенням неприцільних кислот:
b a
СН3-СН-СН2-СООН  СН3-СН=СН-СООН
СН3-СН=СН-СООН
½
ОН
b-оксимасленна кислота кротонова кислота
в) g - та d- Оксикислоти при нагріванні утворюють внутрішні складні ефіри - лактони:
g b a ¤¤ О

 СН3-СН-СН2-СН2-СООН
СН3-СН-СН2-СН2-СООН  СН3-СН-СН2-СН2-С
СН3-СН-СН2-СН2-С
½

 ОН О
ОН О
g-оксивалерьянова кислота лактон g-оксивалерьянової кислоти
Окремі представники. Молочна кислота СН3-СНОН-СООН. Існує у природі у виді двух- оптичних антиподів та рацемат. Гігроскопічна сіропоподібна рідини. Найбільш важливий спосіб добування - молочнокислого бродіння:
С6Н12О ® 2СН3-СНОН-СООН
гексоза молочна кислота
При молочнокислому бродінні сахарів утворюється рацемічна форма молочної кислоти. Молочнокисле бродіння грає велике значення у виробництві молочнокислих продуктів, при виробництві рідких дріжджів для хлібопечення, квашення капусти, огірків.
Молочну кислоту добувають синтетичним шляхом із оцтового альдегіду:
¤¤ О
 СН3-С
СН3-С  СН3-СН-СN
СН3-СН-СN  ® СН3-СН-СООН
® СН3-СН-СООН
Н ½ ½
ОН ОН
оцтовий альдегід молочна кислота
Молочна кислота використовується у шкіряній промисловості при обробці шкіри, текстильній як протрави та в медицині. Велике використання вона знайшла у харчовій промисловості при виробництві цукерок, безалкогольних напоїв.
Яблучна кислота НООС-СН2-СНОН-СООН. Зустрічається у виді двох оптичних антиподів і рацемата. У рослинному мирі широко розміщена ліворухома L-яблучна кислота. Є одною із головних органічних кислот у яблуках, рябині, груші, кізилі. Добувають гідролізом бромянтарної кислоти:
НООС-СН2-СНВr-СООН 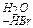 ® НООС-СН2СНОН-СООН
® НООС-СН2СНОН-СООН
Використовується у харчовій промисловості в виробництві кондитерських виробів та безалкогольних напоїв.
Винна кислота НООС-СНОН-СНОН-СООН. Зустрічається у виді двох оптичних антиподів, рацемата і мезовиної кислоти.
У природі зустрічається право рухома кислота, має назву виннокам’яна, так як вона була добута із "винного каменя" - залишок, добутого при виробництві та видержці виноградних вин.
Винна кислота у харчовій промисловості використовується при виробництві фруктових вод, хімічних розпушувачів тіста, у аналітичній хімії для визначення іонів калію, у медицині.
СООН
½
Лимона кислота СООН-СН2-С-СН2СООН. Основна органічна кислота плодів
½
НО
цитрусових, у лимонах її міститься біля 9% на суху масу. Кристалічна речовина, добре розчинна у воді. Лимону кислоту добувають із листків махорки, лимонів та біохімічним шляхом за допомогою гриба Aspergillus niger. Використовується у харчовій промисловості при виробництві цукерок, кремів, безалкогольних напоїв, у текстильній промисловості при фарбуванні тканин та медицині.
Стереохімія вуглецю. У органічній хімії відомі два основних види ізомерії - структурна та просторова. До просторової ізомерії відносяться:
1) геометрична (цис- і трас-ізомерія);
2) оптична;
3) поворотна ізомерія.
Розділ органічної хімії, який вивчає просторову будову молекул, його вплав на властивості речовин, на напрямок та швидкість органічних реакцій, називається стереохімією. Перший із перелічених видів просторової ізомерії - геометрична ізомерія - був розглянутий у розділі алкенів, а також карбонових кислот та у інших розділах.
Оптична ізомерія. У 1815р. французький хімік Біо знайшов, що деякі органічні речовини у рідкому та розчиненому стані здібні рухати площину плоскополяризованого світла. Раніше ця особливість була відзначена для кристалів кварцу - при проходженні через них поляризованого струменю відбувається рух площини поляризації, одні кристали рушать її у право, інші - вліво. У 1848р. Л.Пастер знайшов ці здібності у винних кислот. Це явище, назване оптичною активністю, знайшло пояснення у роботах Вант-Гоффа та Ле Беля. Вант-Гофф висказав предположення, що оптична активність органічних сполук пов'язана з присутністю у їх молекулах асиметричного атому вуглецю. Для більшості оптично активних сполук це предположення є вірним.
Присутність асиметричного атому вуглецю у молекулі молочної кислоти приводить до утворення двох просторових ізомерів, які відрізняються друг від друга як несиметричний предмет від свого зображення у дзеркалі. Звідси інша назва оптичної ізомерії - дзеркальна ізомерія. Подібні просторові ізомери називаються дзеркальними ізомерами (енантиометрія) чи оптичними антиподами.
Оптична неактивна модифікація, складена із рівних кількостей двох антиподів, називається рацематом. Рацемати утворюються по ходу хімічної реакції, коли імовірність утворення кожного із оптичних антиподів однакова. Рацемат може уявлювати суміш двох антиподів чи їх молекулярних сполук.
По більшості хімічних та фізичних властивостей оптичні антиподи не відрізняються друг від друга. Різниця лиш у тім, що один із них ліво-, інший праворухомий, та у їх здібності кристальозуватися у енантиоморфні форми.
Рацемическі сполуки відрізняються по своїм фізичним властивостям від енантиомерів.
У останній час молекули органічних сполук, проявляючи оптичну активність та здібних до існування у виді пари енантиомерів, називають хоральними. Хоральні молекули не мають ні центру, ні площини симетрії, но можуть мати ось симетрії. Якщо молекули не мають і осі симетрії, то вони є асиметричними. Асиметричний атом получив назву хорального атому чи хорального центру.
ЛЕКЦІЯ №13.
|
|
|
|
|
Дата добавления: 2014-11-09; Просмотров: 700; Нарушение авторских прав?; Мы поможем в написании вашей работы!