
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Альдегіди. Номенклатура, властивості і добування
|
|
|
|
Конспект лекційного заняття
Основні поняття
Аліфатичні альдегіди. Аліфатичні кетони
Альдегіди, кетони.
План лекційного заняття:
1. Будова, номенклатура, ізомерія альдегідів.
2. Властивості і добування альдегідів.
Література:
1. Ластухін Ю.О., Воронов С.А. Органічна хімія. – Львів: Центр Європи, 2001. – С. 71-127, 190-200.
2. Нейланд О.Я. Органическая химия. – М.: Высшая школа, 1990. – С. 9-13, 22-38, 59-61, 81-85, 86-89, 92-95, 103-105, 130, 145, 177-179, 225-228.
3. Перекалин В.В., Зонис С.А. Органическая химия. – М.: Просвещение, 1972. – С. 6-17, 18-25, 29-38, 47-48, 54-58, 76, 78-79, 105, 160-161, 177-179.
4. Петров А.А., Бальян Х.В., Трощенко А.Б. Органическая химия. – М.: Высшая школа, 1973. – С. 5-11, 20-43, 44-48, 64-65, 248-257.
5. Чирва В.Я., Ярмолюк С.М., Толкачова Н.В., Земляков О.Є. Органічна хімія. – Львів: БаК, 2009. – С. 81-131.
Карбонільні сполуки містять у молекулі карбонільну групу 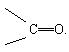 . Карбонільні сполуки поділяютьнаальдегіди і кетони.
. Карбонільні сполуки поділяютьнаальдегіди і кетони.
У молекулах альдегідів карбонільна група сполучена з вуглеводневим радикалом і атомом водню (або з двома атомами водню), тобто загальна формула цих сполук
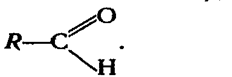
Номенклатура. Назви альдегідів за замісниковою номенклатурою згідно з правилами IUРАК будують з назви відповідного вуглеводню з додаванням закінчення -аль. Перед коренем назви записують бічні замісники, зазначаючи їх положення і кількість. Нумерацію атомів вуглецю починають з вуглецевого атома карбонільної групи. Приклади:
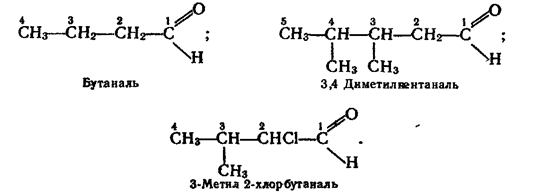
Для альдегідів широко використовують тривіальні назви, які аналогічні назвам відповідних органічних кислот. У табл. наведено назви за замісниковою номенклатурою та тривіальні назви деяких насичених альдегідів.
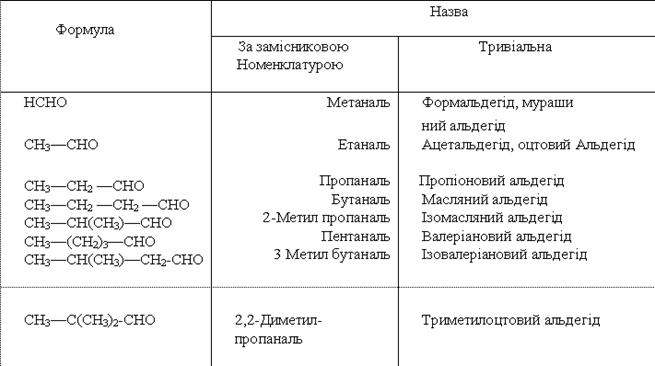
Властивості. Перший член гомологічного ряду насичених альдегідів НСНО — безбарвний газ, кілька наступних альдегідів — рідини. Вищі альдегіди — тверді речовини.
У карбонільній групі зв'язок між атомами кисню і вуглецю сильно полярний: електронна густина зміщена в бік атома кисню 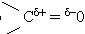 . Для карбонільних сполук характерні реакції нуклеофільного приєднання. В цих реакціях нуклеофільні агенти (негативно заряджені частинки) приєднуються до атома вуглецю карбонільної групи, а електрофільні агенти (позитивно заряджені частинки) приєднуються до атома кисню.
. Для карбонільних сполук характерні реакції нуклеофільного приєднання. В цих реакціях нуклеофільні агенти (негативно заряджені частинки) приєднуються до атома вуглецю карбонільної групи, а електрофільні агенти (позитивно заряджені частинки) приєднуються до атома кисню.
Вплив атома кисню в карбонільних сполуках передається по ланцюгу. Наприклад, у сполуці, що має фрагмент 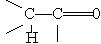 , внаслідок зміщення електронної густини до кисню атом водню, сполучений з другим вуглецевим атомом, виявлятиме підвищену рухливість — його легко відірвати або замістити.
, внаслідок зміщення електронної густини до кисню атом водню, сполучений з другим вуглецевим атомом, виявлятиме підвищену рухливість — його легко відірвати або замістити.
Отже, карбонільна група обумовлює високу реакційну здатність альдегідів.
1. Реакції приєднання. Альдегіди легко приєднують ціановодень НСN і гідросульфіт натрію NaНSО3:
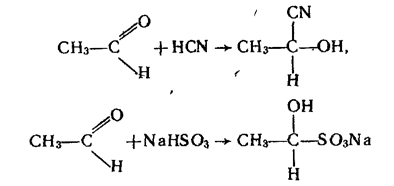
Продукти приєднання NаНSO3 — кристалічні речовини, розчинні у воді. При нагріванні з кислотами вони розпадаються з утворенням вихідного альдегіду. Тому останню реакцію використовують для очистки альдегідів.
При наявності нікелевих або платинових каталізаторів альдегіди приєднують водень і відновлюються до первинних спиртів, наприклад:
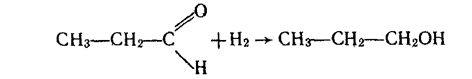
Приєднуючи спирти, альдегіди утворюють сполуки, що мають назву а ц е т а л і в. Реакція відбувається при наявності кислот:
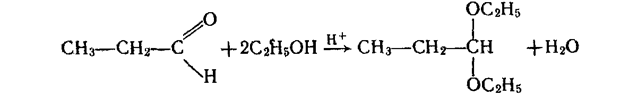
Ацеталі — це прості ефіри двохатомного спирту. Вони легко гідролізуються з утворенням вихідних речовин.
2. Реакції полімеризації і конденсації. Ці реакції характерні для альдегідів і обумовлені реакційною здатністю карбонільної групи. Процеси полімеризації розглядаються далі, при вивченні властивостей формальдегіду і ацетальдегіду.
Дві молекули альдегіду можуть сполучатися одна з одною при наявності лугу з утворенням сполуки з довшим вуглецевим ланцюгом, яка містить альдегідну і гідроксильну групи:
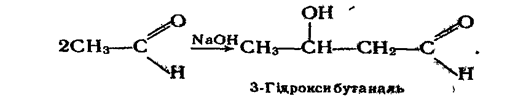
Таку речовину називають альдолем. При відщепленні молекули води від гідроксибутаналю утворюється альдегід, що містить подвійний зв'язок у ланцюгу:
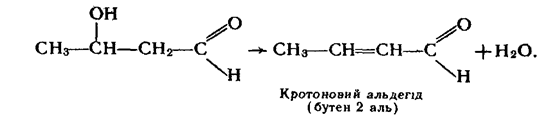
Подібні реакції конденсації альдегідів називаються реакціями альдольно-кротонової конденсації. При конденсації інших альдегідів реакція також завжди відбувається з участю другого вуглецевого атому однієї з молекул, наприклад:
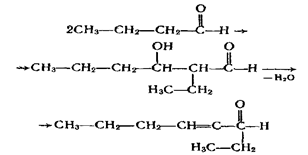
3. Окислення. Під час окислення альдегідів, яке відбувається дуже легко, утворюються органічні кислоти або їхні солі. Наприклад, під час окислення оцтового альдегіду утворюється оцтова кислота:
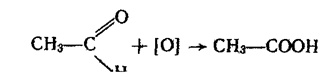
Н
Якісною реакцією на альдегіди є реакція срібного дзеркала — окислення їх аміачним розчином оксиду срібла при нагріванні:
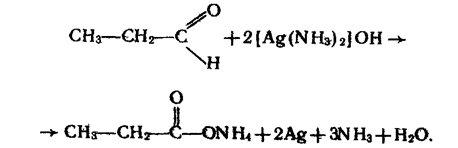
Металічне срібло, яке виділяється, вкриває стінки посудини тонким блискучим шаром.
Альдегіди окислюються також гідроксидом міді (II), який відновлюється до червоно-коричневого оксиду міді (І):

4. Заміщення кисню карбонільної групи. Атом кисню в молекулі альдегіду може бути заміщений на галоген під дією галогенідів фосфору РС15 або РВr5, наприклад:
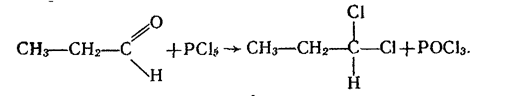
Під дією гідроксиламіну NH2ОНна альдегіди карбонільний кисень заміщується на оксімідну групу = N - ОН:
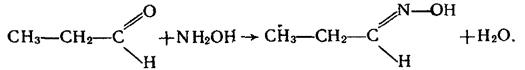
Азотовмісна органічна сполука, що утворюється, належить до о к с и м і в.
5. Взаємодія з галогенами. Як уже зазначалось, атом водню біля другого вуглецевого атома вуглеводневого ланцюга альдегідів має підвищену рухливість. Під час взаємодії альдегідів з хлором чи бромом цей водневий атом легко заміщується на галоген, наприклад:
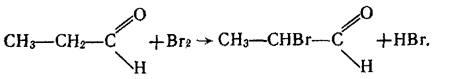
Добування. 1. Альдегіди утворюються під час окислення або каталітичного дегідрування (відщеплення водню) первинних спиртів:
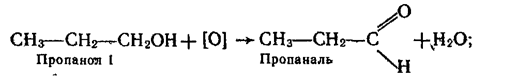
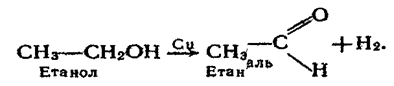
Каталітичне дегідрування спирту відбувається при наявності металічної міді.
2. Альдегіди можна добути гідролізом дигалогенопохідних алканів, наприклад:
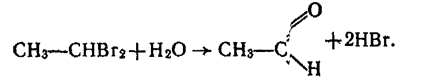
3. Альдегіди утворюються під час взаємодії алкенів з оксидом вуглецю (II) і воднем (оксосинтез):
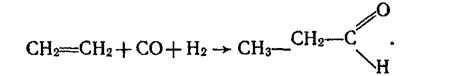
Оксосинтез відбувається при наявності каталізаторів — комплексних сполук кобальту під тиском 5-10 МПа.
ЛЕКЦІЯ №11.
|
|
|
|
|
Дата добавления: 2014-11-09; Просмотров: 8006; Нарушение авторских прав?; Мы поможем в написании вашей работы!