
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Дослід 96. Трифенілметанові барвники
|
|
|
|
Реактиви: кристалічний фіолетовий, фенолфталеїн (1%-й спиртовий розчин), фталевий ангідрид, фенол, 2 н. розчин гідроксиду натрію, 2 н. розчин хлоридної кислоти, концентрована сульфатна кислота, 2 н. розчин карбонату натрію, концентрований розчин КОН, диметилформамід (ДМФА).
Обладнання: піпетки, фільтрувальний папір, водяні бані, хімічні стакани (100-150 мл).
а) Властивості барвника кристалічного фіолетового. В пробірці розчиняють дуже невелику кількість кристалічного фіолетового (розчин повинен бути прозорим). Розчин барвника переливають в стакан і піпеткою по краплям додають при перемішуванні розчин хлоридної кислоти. Колір розчину барвника спочатку стає синьо-зеленим, потім зеленим, а при додаванні надлишку кислоти – світло-жовтим. При додаванні до одержаного розчину краплями концентрованого розчину лугу колір змінюється в зворотньому порядку.
Поясніть зміну кольору барвника при зміні рН середовища.
б) Одержання індикатору фенолфталеїну. В пробірці змішують при струшуванні 0,05-0,1 г дрібно розтертого фталевого ангідриду з подвійною кількістю фенолу, а потім до суміші додають 1-2 краплі концентрованої сульфатної кислоти. Вміст пробірки обережно нагрівають в полум’ї пальника протягом 2-3 хвилин до розтоплення суміші і утворення темно-червоного забарвлення. До маси, що охолонула, приливають при струшуванні 5 мл гарячої води.
Відбирають піпеткою 3-5 крапель одержаного розчину, переносять його в другу пробірку і додають 2 н. розчин гідроксиду натрію. З’являється малинове забарвлення. При додаванні надлишку розчину лугу забарвлення зникає. Якщо до сильно лужного безбарвного розчину додавати по краплям розчин хлоридної кислоти, розчин спочатку знову стає малиновим, а при надлишку кислоти – знебарвлюється.
Напишіть рівняння реакції конденсації фталевого ангідриду з фенолом.
в) Властивості фенолфталеїну. В чотири пробірки наливають по 3-5 мл: 2 н. розчину карбонату натрію, концентрованого розчину гідроксиду калію, концентрованої сульфатної кислоти і диметилформаміду. В пробірку з диметилформамідом вносять 4-5 гранул твердого КОН і нагрівають до кипіння при струшуванні. Потім в кожну пробірку додають по 3-4 краплі спиртового розчину фенолфталеїну. В пробірці з розчином карбонату натрію утворюється стійке малинове забарвлення; в пробірці з концентрованим розчином лугу малинове забарвлення з’являється, але з часом зникає; в пробірці з концентрованою сульфатною кислотою з’являється оранжеве забарвлення, а в пробірці з розчином гідроксиду калію в диметилформаміді з’являється фіолетове забарвлення.
В слабо лужному середовищі (а також в сильно кислому середовищі) в молекулі фенолфталеїну утворюється потужна система спряження за рахунок переходу центрального атому карбону в sp2-стан. В сильно лужному середовищі цей атом карбону знову переходить в стан sp3-гібридизації. Система спряження зникає, а з нею зникає і колір:

В сильно кислому середовищі також виникає система спряження:
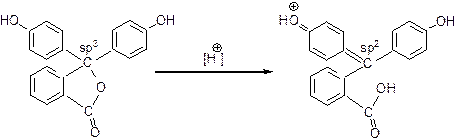
Фіолетовий колір фенолфталеїну в середовищі ДМФА пояснюється впливом сольватної оболонки, яку створюють для іону фенолфталеїну молекули диметилформаміду.
|
|
|
|
|
Дата добавления: 2014-11-09; Просмотров: 901; Нарушение авторских прав?; Мы поможем в написании вашей работы!